-
银镜反应是检验醛基的重要反应,教材对该实验的操作条件只是粗略的描述。某同学进行如下研究:
(1)在干净试管中加入2ml2%________,然后,________得到银氨溶液,分装入5支试管,编号为1#.2#.3#.4#.5# 。
(2)依次滴加2%.5%.10%.20%.40%的乙醛溶液4滴,快速振荡后置于60℃~70℃的水浴中。3分钟后,试管1#未形成大面积银镜,试管5# 的银镜质量差有黑斑, 试管4# 产生的银镜质量一般,试管2#.3# 形成光亮的银镜。
该研究的目的是:________。
(3)乙醛发生银镜反应的化学方程式为:________,
(4)有文献记载:在强碱性条件下,加热银氨溶液可能析出银镜。验证和对比实验如下。
| 装置 | 实验序号 | 试管中的药品 | 现象 |
| 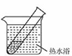
| 实验Ⅰ | 2mL银氨溶液和数滴较浓NaOH溶液 | 有气泡产生: 一段时间后,溶液逐渐变黑:试管壁附着银镜 |
| 实验Ⅱ | 2mL银氨溶液和 数滴浓氨水 | 有气泡产生:一段时间后,溶液无明显变化 |
该同学欲分析实验Ⅰ和实验Ⅱ的差异,查阅资料后,得知:
a.Ag(NH3)2++2H2O Ag++2NH3·H2O b.AgOH不稳定,极易分解为黑色Ag2O
Ag++2NH3·H2O b.AgOH不稳定,极易分解为黑色Ag2O
经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O。产生Ag2O的原因是:
________。
(5)用湿润的红色石蕊试纸检验NH3产生的现象是 。用稀HNO3清 洗试管壁上的Ag,该反应的化学方程式是 ________ 。
(6)该同学对产生银镜的原因提出假设:在NaOH存在下,可能是NH3还原Ag2O。如果该假设成立,则说明检验醛基时,银氨溶液不能呈强碱性,因为:
-
甲、乙两位学生分别做淀粉水解产物检验的实验,操作如下:学生甲在一支试管中放入0.5 g淀粉后,再加入质量分数为20%的硫酸溶液,加热10 min后,再将溶液一分为二,其中一份溶液做银镜反应实验,结果无银镜出现,另一份溶液加入碘水,结果无蓝色出现;学生乙在一支试管中放入0.5 g淀粉后,再加入质量分数为20%的硫酸溶液少许,加热45 min后,加入过量的NaOH溶液中和硫酸,再将溶液一分为二,其中一份溶液做银镜反应实验,结果有银镜产生,另一份溶液中加入少量碘水,未出现蓝色。试回答:
(1)学生甲的实验操作不正确的地方是_____________________________________。
根据甲的实验现象,淀粉的水解情况是________。
A.完全水解 B.部分水解 C.没有水解 D.不能准确判断
(2)学生乙的实验操作不正确的地方是_____________________________________。
根据乙的实验现象,淀粉的水解情况是________。
A.完全水解 B.部分水解 C.没有水解 D.不能准确判断
-
某小组探究清洗试管(内壁附着银镜)的反应原理,进行下列实验。
I.初步探究
(1)将稀硝酸加入附着银镜的试管中,记录现象如下:
| 实验Ⅰ | 实验操作 | 实验现象 |
| 
| 银镜上出现气泡,在液面下方为无色气体,在试管口附近......;试管内壁上的银逐渐溶解。 |
①补全反应中的实验现象___。
②实验Ⅰ中银镜消失发生反应的化学方程式为____。
(2)为消除实验Ⅰ中氮氧化物的污染,将双氧水溶液加入附着银镜的试管中。
| 实验Ⅱ | 实验操作 | 实验现象 |
| 
| 剧烈反应,有大量无色气体产生,该气体可以使带火星的木条复燃;试管内壁上的银逐渐溶解。 |
①由现象推测H2O2将Ag氧化为Ag+,但通过实验排除了这种可能。该实验方案是:在反应后的液体中,加入___。
②查阅资料发现:该实验中银镜溶解后最终产物为颗粒很小(直径在1~100nm之间)的Ag,其分散在液体中,肉眼无法识别。该同学通过实验证实了这种可能性。他的操作及现象是:___。
③写出该实验Ⅱ中发生反应的化学方程式:___。
II.查阅资料,继续探究
查阅文献:Ag2O+4NH3•H2O=2[Ag(NH3)2]++2OH-+3H2O
(3)探究Ag 2O在H 2O 2分解反应中的作用,进行如下实验。
| 实验Ⅲ | 实验操作 | 实验现象 |
| 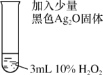
| 剧烈反应,产生大量的无色气体,同时在试管底部仍有少量黑色固体 |
根据实验Ⅲ的现象猜想:Ag 2O在反应中作氧化剂。继续实验,在实验Ⅲ反应后的试管中加入足量的溶液x后,固体仍有剩余。由此验证了该猜想的正确。
①在实验中加入足量的溶液x是____。
②实验Ⅲ中发生反应的化学方程式为___。
-
某小组探究清洗试管(内壁附着银镜)的反应原理,进行下列实验。
I.初步探究
(1)将稀硝酸加入附着银镜的试管中,记录现象如下:
| 实验Ⅰ | 实验操作 | 实验现象 |
| 
| 银镜上出现气泡,在液面下方为无色气体,在试管口附近......;试管内壁上的银逐渐溶解。 |
①补全反应中的实验现象___。
②实验Ⅰ中银镜消失发生反应的化学方程式为____。
(2)为消除实验Ⅰ中氮氧化物的污染,将双氧水溶液加入附着银镜的试管中。
| 实验Ⅱ | 实验操作 | 实验现象 |
| 
| 剧烈反应,有大量无色气体产生,该气体可以使带火星的木条复燃;试管内壁上的银逐渐溶解。 |
①由现象推测H2O2将Ag氧化为Ag+,但通过实验排除了这种可能。该实验方案是:在反应后的液体中,加入___。
②查阅资料发现:该实验中银镜溶解后最终产物为颗粒很小(直径在1~100nm之间)的Ag,其分散在液体中,肉眼无法识别。该同学通过实验证实了这种可能性。他的操作及现象是:___。
③写出该实验Ⅱ中发生反应的化学方程式:___。
II.查阅资料,继续探究
查阅文献:Ag2O+4NH3•H2O=2[Ag(NH3)2]++2OH-+3H2O
(3)探究Ag 2O在H 2O 2分解反应中的作用,进行如下实验。
| 实验Ⅲ | 实验操作 | 实验现象 |
| 
| 剧烈反应,产生大量的无色气体,同时在试管底部仍有少量黑色固体 |
根据实验Ⅲ的现象猜想:Ag 2O在反应中作氧化剂。继续实验,在实验Ⅲ反应后的试管中加入足量的溶液x后,固体仍有剩余。由此验证了该猜想的正确。
①在实验中加入足量的溶液x是____。
②实验Ⅲ中发生反应的化学方程式为___。
-
下列说法正确的是( )
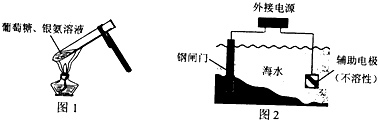
A.实验室利用图1操作进行银镜反应,试管内壁可以生成光亮银镜
B.图2所示钢闸门的防腐办法中,钢闸门应与外接电源的正极相连
C.用NaOH溶液除去乙酸乙酯中的乙酸
D.鸡蛋清溶液中加入浓硝酸有白色沉淀,加热,沉淀变黄色
-
(14分)MnO2是一种重要的催化剂。某研究性学习小组设计了将粗MnO2(含有较多MnO和MnCO3)样品转化为纯MnO2的实验,其流程如下:
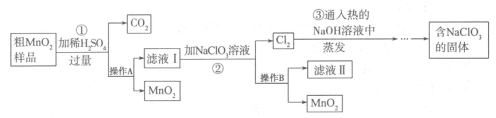
(1)检验操作A所得的MnO2是否洗涤干净的方法是 。
(2)第②步反应的离子反应方程式为 。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、 、 、玻璃棒。
(4)上述流程中可用于循环使用的物质是 (填化学式)。
(5)MnO2不仅可作催化剂还可作氧化剂,写出1个用二氧化锰作氧化剂的化学反应方程式 。
(6)若粗MnO2样品的质量为24.28g,第①步反应后,经过滤得到18.35g MnO2,并收集到0.672 LCO2(标准状况下),则样品中所含的MnO质量为 g。
-
全世界每年因生锈损失的钢铁约占世界钢铁年产量的1/4。某学生想探究铁生锈的条件,他将干净的铁钉分别同时入放A、B、C三支试管中进行研究。
(1)请你帮助该学生完成下列实验设计的内容:
| 编号 | 操作方法 | 实验目的 |
| A | | 探究铁在干燥空气中的生锈情况 |
| B | 放入铁钉,注入蒸馏水浸没铁钉,并用植物油液封 | |
| C | | 探究铁在有空气和水封时的生锈情况 |
(2)一周后,编号为________的试管中的铁钉最易生锈。
(3)用相同材料制作,经过相同时间防锈处理的铁栏杆,安装在南方比安装在北方更易生锈,其原因是_______________________________________。
(4)在焊接铁管时,为了使接口更加牢固,常用稀盐酸清洗接口处的铁锈,该反应的化学方程式为________________________________。
-
(15分)有文献记载:在强碱条件下,加热银氨溶液可能析出银镜。某同学进行如下验证和对比实验。
| 装置 | 实验序号 | 试管中的药品 | 现象 |
| 
| 实验Ⅰ | 2mL银氨溶液和数 滴较浓NaOH溶液 | 有气泡产生: 一段时间后,溶液 逐渐变黑:试管壁 附着银镜 |
| 实验Ⅱ | 2mL银氮溶液和 数滴浓氨水 | 有气泡产生: 一段时间后,溶液 无明显变化 |
该同学欲分析实验Ⅰ和实验Ⅱ的差异,查阅资料:
a.Ag(NH3)2++2H2O=Ag++2NH3+H2O
b.AgOH不稳定,极易分解为黑色Ag2O
(I)配制银氨溶液所需的药品是________。
(2)经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O.
①用湿润的红色石蕊试纸检验NH3,产生的现象是________。
②产生Ag2O的原因是。
(3)该同学对产生银镜的原因提出假设:可能是NaOH还原Ag2O。实验及现象:向AgNO3
溶液中加入________,出现黑色沉淀;水浴加热,未出现银镜。
(4)重新假设:在NaOH存在下.可能是NH3,还原Ag2O。用右图所示装置进行实验。现象:出现银镜。在虚线框内画出用生石灰和浓
氨水制取NH3的装置简图(夹持仪器略)。

(5)该同学认为在(4)的实验中会有Ag(NH3)2OH生成。由此又提出假设:在NaOH存在下,可能是Ag(NH3)2OH也参与了NH3还原Ag2O的反应.进行如下实验:

①有部分Ag2O溶解在氨水中,该反应的化学方程式是________。
②实验结果证实假设成立,依据的现象是________。
(6)用HNO3消洗试管壁上的Ag,该反应的化学方程式是________。
-
某学习小组进行如下课外活动,邀请你参与:
(1)研究水溶液中复分解型离子反应的发生条件,设计如下方案:
| 实验设计及操作 | 离子方程式 |
| Ⅰ.向盛有2mlCuSO4溶液的试管里加入2mlNaOH溶液,观察现象 | Cu2++2OH-═Cu(OH)2↓ |
| Ⅱ.向盛有2mL pH=1的HCl溶液的试管里慢慢滴入18mL(已足量)CH3COONH4溶液(查资料知CH3COONH4,溶液呈中性 )震荡摇匀,测得pH≈3.7 | |
| Ⅲ向盛有2mLNaHCO3溶液的试管里加入2mL H2SO4溶液,观察现象 | HCO3- +H+═H2O+CO2↑ |
| Ⅳ向盛有2mL 稀Na2SO4溶液的试管里加入2mL稀KCl溶液,观察无明显现象 | 
|
①写出II实验中发生反应的离子方式_____________________;
②根据实验发现只要有___________________,等物质生成,水溶液中复分解型离子反应就可以发生。
③经过小组同学积极思考、讨论交流发现在生成三类物质后,导致一个共同的结果,于是得出结论:溶液中复分解型的离子反应总是向着某些______________的方向进行(与溶液混合的瞬间相比).
④小组同学进一步深入思考,发现上述问题其实质是化学反应进行的方向问题.请你结合化学反应原理的相关知识对③中的结论作出合理解释_____________________;
(2)如何研究H2SO4、KC1、NaHSO4、NaN03、Na2C03、NH4C1、NaOH的性质?设计方案为:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验,具体如下:
①根据方案进行分类时,经实验测得KC1、NaN03,溶液的pH=7;
H2SO4、NaHSO4、NH4Cl溶液的pH<7;
Na2C03、NaOH溶液的pH>7.
由此有的同学按分类法思想把H2SO4、NaHSO4、NH4Cl都划分为酸类,请你运用中学化学相关理论判断这样划分是否合理?并简要说明理由.______________、______________;
②向NaHS04、NaN03的混合溶液中,滴加Na2S溶液产生黄色沉淀和无色气体,写出反应的离子方程式:____________________;反应中若生成标准状况下的无色气体1.12L,则被氧化的物质为__________mol,转移电子的物质的量为__________mol。
③某同学在用H2S04鉴别NaN03、Na2C03、NaOH溶液时,Na2C03很容易鉴别,但鉴别NaN03和NaOH时却陷入了困境.限用上述另外六种物质,请你设计一个现象明显的实验方案帮忙解决这一难题_____________。
-
有文献记载:在强碱性条件下,加热银氨溶液可能析出银镜.某同学进行如下验证和对比实验.
| 装置 | 实验序号 | 试管中的药品 | 现象 |
 | 实验I | 2mL银氨溶液和数滴较浓NaOH溶液 | 有气泡产生;
一段时间后,溶液逐渐变黑;
试管壁附着有银镜 |
| 实验II | 2mL银氨溶液和数滴浓氨水 | 有气泡产生;
一段时间后,溶液无明显变化 |
该同学欲分析实验Ⅰ和实验Ⅱ的差异,查阅资料:
a.Ag(NH3)2++2H2O⇌Ag++2NH3+H2O
b.AgOH不稳定,极易分解为黑色Ag2O
(1)配制银氨溶液所需的药品是______.
(2)经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O.
①用湿润的红色石蕊试纸检验NH3,产生的现象是______.
②产生Ag2O的原因是______.
(3)该同学对产生银镜的原因提出瑕设:可能是NaOH还原Ag2O.实验及现象:向AgNO3溶液中加入______,出现黑色沉淀;水浴加热,未出现银镜.
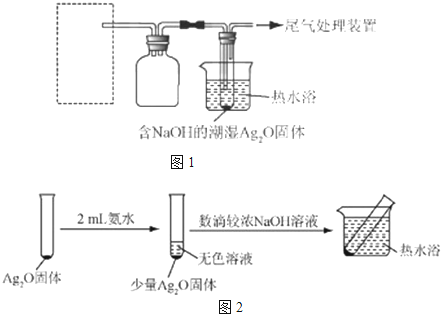
(4)重新假设:在NaOH存在下,可能是NH3还原Ag2O.用图1所示装置进行实验.现象:出现银镜.在虚线框内画出用生石灰和浓氨水制取NH3的装置简图(夹持仪器略).
(5)该同学认为在(4)的实验中会有Ag(NH3)2OH生成.由此又提出假设:在NaOH存在下,可能是Ag(NH3)2OH也参与了NH3还原Ag2O的反应.进行如图2实验:
①有部分Ag2O溶解在氨水中,该反应的化学方程式是______.
②实验结果证实假设成立,依据的现象是______.
(6)用HNO3清洗试管壁上的Ag,该反应的化学方程式是______.
Ag++2NH3·H2O b.AgOH不稳定,极易分解为黑色Ag2O









