-
锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231 ℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:

①步骤Ⅰ加入Sn粉的作用:__________________及调节溶液pH。
②步骤Ⅱ用到的玻璃仪器有烧杯、________________________。
③步骤Ⅲ生成SnO的离子方程式:__________________________。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是:______________________,证明已洗净。
⑤步骤Ⅴ操作依次为____________、____________、过滤、洗涤、低温干燥。
(2)某化学兴趣小组对用于微电子器件生产的锡粉进行了纯度测定:①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1 000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。
①写出步骤②加入Fe2(SO4)3发生反应的离子方程式:____________________;
②此锡粉样品中锡的质量分数为:__________________。
-
(18分)锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为_________。
(2)用于微电子器件生产的锡粉纯度测定:①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。步骤②中加入Fe2(SO4)3的作用是___________;此锡粉样品中锡的质量分数_____________。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
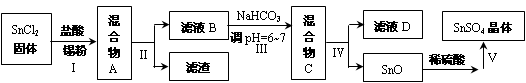
①步骤Ⅰ加入Sn粉的作用: ________________________________及调节溶液pH。
②步骤Ⅱ用到的玻璃仪器有烧杯、_______________、______________。
③步骤Ⅲ生成SnO的离子方程式:____________________________________。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是______________________________,证明已洗净。
⑤步骤Ⅴ操作依次为 _____________、____________、过滤、洗涤、低温干燥。
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为__________________。
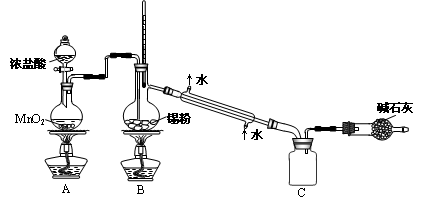
实验室欲用下图装置制备少量SnCl4 (夹持装置略),该装置存在明显缺陷,改进方法是__________。
利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是_____________________________________。
-
锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231 ℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为________。
(2)用于微电子器件生产的锡粉纯度测定:①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1 000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。步骤②中加入Fe2(SO4)3的作用是_____________________;此锡粉样品中锡的质量分数: ____________。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
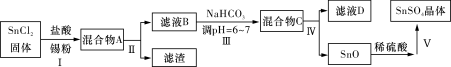
①步骤Ⅰ加入Sn粉的作用: _____________________及调节溶液pH。
②步骤Ⅱ用到的玻璃仪器有烧杯、________________________。
③步骤Ⅲ生成SnO的离子方程式:________________________________。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是__________________________,证明已洗净。
⑤步骤Ⅴ操作依次为________________________、过滤、洗涤、低温干燥。
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为:___________________。
实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是_________________。
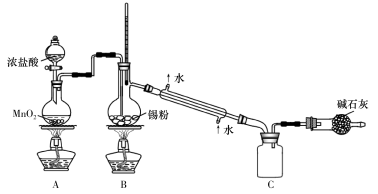
(5)利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是________________________。
-
锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231 ℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为________。
(2)用于微电子器件生产的锡粉纯度测定:
①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
②加入过量的Fe2(SO4)3;
③用0.1 000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。步骤②中加入Fe2(SO4)3的作用是__________________;此锡粉样品中锡的质量分数:____________。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
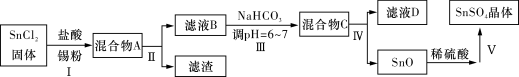
①步骤Ⅰ加入Sn粉的作用:____________________及调节溶液pH。
②步骤Ⅱ用到的玻璃仪器有烧杯、________________________。
③步骤Ⅲ生成SnO的离子方程式:__________________________。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是___________________,证明已洗净。
⑤步骤Ⅴ操作依次为___________________、过滤、洗涤、低温干燥。
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为:_____________。实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是_______________
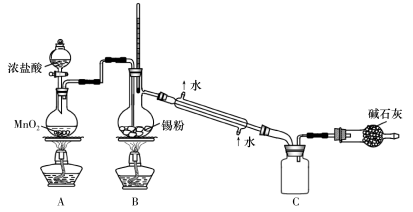
(5)利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是______________________。
-
锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33℃、沸点为114℃。
2H++SnO22- Sn(OH)2
Sn(OH)2 Sn2++2OH-
Sn2++2OH-
请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为_______。
(2)用于微电子器件生产的锡粉纯度测定:
① 取1.19g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
② 加入过量的Fe2(SO4)3;③ 用0.1000 mol/LK2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。
步骤② 中加入Fe2(SO4)3的作用是_______;此锡粉样品中锡的质量分数________。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如图所示:

① 步骤I加入Sn粉的作用:___________及调节溶液pH。
② 步骤Ⅲ生成SnO的离子方程式:____________________。
③ 以锡单质为阳极,铁片为阴极,SnSO4溶液为电解质溶液,在铁片上镀锡,阴极反应式是____________,镀锡铁破损后在潮湿的环境中容易发生腐蚀的原因是_________,若是在较弱的酸性环境中发生腐蚀,正极反应式是____________。
(4)SnCl4蒸气遇水汽呈浓烟状,因而叮制作烟幕弹, 其反应的化学方程式为___________。
(5)锡的+2价化合物应具有较强的还原性,已知Sn2+的还原性比 Fe2+的还原性强,PbO2的氧化性比Cl2的氧化性强。试写出下列反应的化学方程式:
① 将SnCl4溶液蒸干灼烧得到的固体物质是________;
② 若用SnCl2溶液与过量的碱溶液反应制Sn(OH)2,该碱溶液可选用________。
-
锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33℃、沸点为114℃。
2H++SnO22- Sn(OH)2
Sn(OH)2 Sn2++2OH-
Sn2++2OH-
请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为_______。
(2)用于微电子器件生产的锡粉纯度测定:
① 取1.19g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
② 加入过量的Fe2(SO4)3;③ 用0.1000 mol/LK2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。
步骤② 中加入Fe2(SO4)3的作用是_______;此锡粉样品中锡的质量分数________。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如图所示:
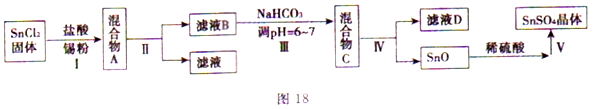
① 步骤I加入Sn粉的作用:___________及调节溶液pH。
② 步骤Ⅲ生成SnO的离子方程式:____________________。
③ 以锡单质为阳极,铁片为阴极,SnSO4溶液为电解质溶液,在铁片上镀锡,阴极反应式是____________,镀锡铁破损后在潮湿的环境中容易发生腐蚀的原因是_________,若是在较弱的酸性环境中发生腐蚀,正极反应式是____________。
(4)SnCl4蒸气遇水汽呈浓烟状,因而叮制作烟幕弹, 其反应的化学方程式为___________。
(5)锡的+2价化合物应具有较强的还原性,已知Sn2+的还原性比 Fe2+的还原性强,PbO2的氧化性比Cl2的氧化性强。试写出下列反应的化学方程式:
① 将SnCl4溶液蒸干灼烧得到的固体物质是________;
② 若用SnCl2溶液与过量的碱溶液反应制Sn(OH)2,该碱溶液可选用________。
-
锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为_______________。
(2)用于微电子器件生产的锡粉纯度测定:①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。步骤②中加入Fe2(SO4)3的作用是__________________;此锡粉样品中锡的质量分数_____________。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
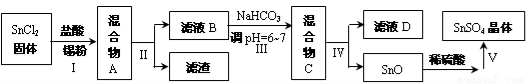
①步骤Ⅰ加入Sn粉的作用: __________________及调节溶液pH。
②步骤Ⅱ、步骤Ⅴ的操作名称为________________,写出该过程用到的一种玻璃仪器的名称:_______________。
③步骤Ⅲ生成SnO的离子方程式:__________________。
④步骤Ⅴ操作依次为 _____________、____________、过滤、洗涤、低温干燥。
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为__________________。
-
锡及其化合物在生产、生活中有着重要的用途。已知: Sn2+易水解、易被氧化;SnCl4极易水解。请按要求回答下列相关问题:
(1)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
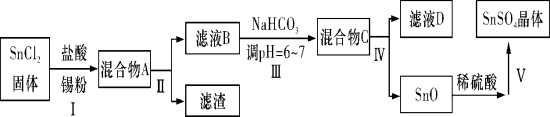
①步骤Ⅰ加入Sn粉的作用: __________________及调节溶液pH。
②步骤Ⅲ生成SnO的离子方程式:____________________________。
③步骤Ⅳ中检验SnO是否洗涤干净的操作是____________ ______,证明已洗净。
④步骤Ⅴ操作依次为____________、____________、过滤、洗涤、低温干燥。
(2)SnCl4蒸气遇氨气及水蒸气呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为:_____________________。
-
锡及其化合物在生产、生活中有着重要的用途。己知:酸性条件下,锡在水洛液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化、易水解生成碱式氯化亚锡(Sn(OH)Cl);SnCl4极易水解。请按要求回答下列相关问题:
(1)锡原子的核电荷数为50,锡的原子结构示意图为________________。
(2) SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因____________。
SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为______________。
(3)硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:
①操作Ⅰ是___________。
②加入Sn粉的作用有两个:a.调节溶液pH; b.__________.
③反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是______________。
(4)锡粉可用于微电子器件生产,该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将1.2g试样溶于盐酸中,发生的反应为:Sn+2HCl=SnCl2+H2↑;②加入过量的FeCl3;③用0.1 mol/L的K2Cr2O7滴定生成的Fe2+ (己知酸性环境下,Cr2O72-可被还原为Cr3+),共用去K2Cr2O7溶液32mL。则锡粉中锡的质量分数是_____________。
-
某化学兴趣小组拟探究锡及锡的化合物的部分性质。经查阅资料知:Sn的熔点231℃;SnC12易被氧化,且易水解;Sn(OH)2常温下易分解,SnCl4常温下为无色液体,熔点-33℃,沸点114.1℃,请回答下列问题:
(1)该小组用以下流程制备SnSO4晶体。

①操作Ⅱ所需的实验仪器为__________。
②过滤操作中玻璃棒的使用的注意事项为__________。
③操作I为沉淀的洗涤。请简述如何判断沉淀是否洗涤干净__________。
(2)用熔融的锡与干燥的氯气制备SnCl4,提供的装置如下:
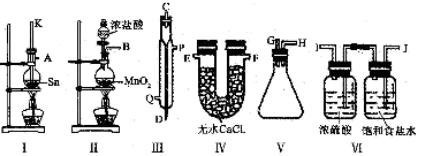
①装置Ⅲ为冷凝管,则水流从__________进入。
②请用大写英文字母按从左到右顺序连接组装仪器__________。
③有同学指出②中连接的实验装置存在不足,不足之处为__________。
(3)测定锡粉质量分数的步骤为:取锡粉1.226g溶于盐酸中,加入过量的FeCl3溶液,再用0.1000 mol/L K2Cr2O7溶液滴定Fe2+,消耗K2Cr2O7溶液32.00 mL,发生的反应为:6FeC12+ K2Cr2O7 +14HC1=6 FeC13+2KC1 +2Cr C13+7H2O。则锡粉的质量分数为(杂质不参与反应) __________ 。













