-
下表为元素周期表的短周期部分。请填空。
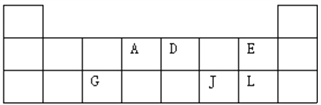
(1)写出 A 原子的最外层电子的轨道表示式___________,G、J、L 三种元素形成的简单离子中, 离子半径最小的是___________,D 元素的气态氢化物的电子式为___________;
(2)A 元素可形成化合物 Fe(AO)5,该物质常温下呈液态,熔点为-20.5℃,沸点为 103℃,易溶于 非极性溶液,据此可判断 Fe(AO)5 晶体属于______________(填晶体类型);
(3)将 G 元素的最高价氧化物对应的水化物溶解在稀硫酸中,写出反应的离子方程式___________;当足量的铁和 2mol 单质 L 发生反应时,电子转移了___________mol;
(4)J 与 L 分别与氢元素形成的气态氢化物的稳定性关系为:___________>___________(填化学式)。
高三化学填空题中等难度题查看答案及解析
-
下表为元素周期表的短周期部分。请填空。
A
D
E
G
J
L
(1)写出A原子的最外层电子的轨道表示式________,G、J、L三种元素形成的简单离子中,离子半径最小的是__________;
(2)A元素可形成化合物Fe(AO)5,该物质常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(AO)5晶体属于________(填晶体类型);
(3)将D元素的气态氢化物通入稀硫酸中,写出反应的离子方程式_____________________;
(4)M与E同主族且核外电子比E多三个电子层,M位于元素周期表_______周期______族,有研究显示HMO具有两性,则HMO与盐酸反应化学方程式为_________________。
高三化学填空题中等难度题查看答案及解析
-
砷(As)是第四周期VA族元素,可以形成As2S3、H3AsO3、H3AsO4等化合物,用途广泛。
完成下列填空:
(1)砷原子核外有__个电子层,最外层有__个电子,写出砷原子最外层电子的轨道表示式:__。
(2)将砷与VA族所有短周期元素的原子半径,按从小到大的顺序排列:__(用元素符号表示)。
(3)溴位于VIIA族且与砷同周期,比较溴、砷最高价氧化物对应水化物酸性的强弱:__强于__(填物质的化学式)。
(4)周期表中,铝和砷都在金属和非金属过渡线附近,举一例说明铝元素具有非金属性:__。
(5)已知:稀Na3AsO3溶液、稀碘水和稀NaOH溶液混合,发生如下反应:AsO33-(aq)+I2(aq)+2OH-
AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43-)与反应时间(t)的关系如图所示。

①写出该反应平衡常数的表达式K=___。
②不能判断反应达到平衡状态的是___(选填编号)。
A.溶液的pH不再变化
B.v(I-)=2v(AsO33-)
C.c(AsO33-)/c(I-)不再变化
D.c(I-)=2ymol·L-1
高三化学填空题中等难度题查看答案及解析
-
氮及其化合物在工农业生产中具有重要作用。
完成下列填空:
(1)如图所示为元素周期表中氮元素部分信息,数据“14.01”表示的是____________;氮原子最外层电子有________种不同的能量,有_______种不同运动状态。
(2)NH3可以作制冷剂,是因为________________NH4Cl溶液与NaOH溶液混合至中性,则c(Na+)_______c(NH3•H2O)(填“<,>”或“=”)
(3)写出一个能比较氮、氧两种元素非金属性强弱的事实:________________
研究NO2、SO2、CO等大气污染物的处理具有重要意义。NO2可用下列反应来处理:
(4)写出上述反应的平衡常数表达式_______________增大该反应平衡常数的措施有__________(填编号)
A. 增压 B. 增加NH3的浓度 C. 降温 D. 及时移走产物
(5)一定条件下上述反应在某体积固定的密闭容器中进行,能说明该反应已经达到平衡状态的是__________。(填编号)
A. c(NO2) : c(NH3)=3:4 B.
C. 容器内气体总压强不再变化 D. 容器内气体密度不再变化
(6)某温度下,在一个容积为2升的反应容器内,上述反应2分钟后达到平衡,测试NO2减少了0.75mol,则在2分钟内NH3的平均反应速率为:
=_____________
高三化学简答题中等难度题查看答案及解析
-
下表为周期表的一部分,其中的编号代表对应的元素。

试填空。
(1)写出上表中元素I的基态原子的电子排布式和价层电子排布图: 。
元素C、D、E、F的第一电离能由大到小的顺序是 (用元素符号表示)。
(2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙。下列有关叙述不正确的有 。
A.甲、乙和丙分子的空间构型分别为正四面体形、三角锥形、V形
B.甲、乙和丙分子中,中心原子均采取sp3的杂化方式
C.三种分子中键角由大到小的顺序是丙>乙>甲
D.甲、乙和丙分子均为由极性键构成的极性分子
(3)由元素J、C、E组成一种化学式为J(CE)5的配位化合物,该物质常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂。据此可判断:
①该化合物的晶体类型为 。
②该化合物的晶体中存在的作用力有 。
A.离子键
B.极性键
C.非极性键
D.范德华力
E.氢键
F.配位键
③根据共价键理论和等电子体理论分析,CE分子中σ键与π键的数目比为 。
(4)在测定A与F形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是 。
(5)某些不同族元素的性质也有一定的相似性,如表中元素G与元素B,原因是 。
高三化学填空题困难题查看答案及解析
-
(10分)第4周期的A、B、C、D四种元素,其价电子数依次为1、2、2、7。其原子序数按A、B、C、D顺序增大,已知A与B的次外层电子数为8,而C与D次外层电子数为18,根据结构填空:
(1)写出元素名称:A________,B________,C________,D________。
(2)D的简单离子是________。
(3)元素的氢氧化物碱性最强的是________。
(4)B与D二原子间能形成化合物的化学式是________。
(5)写出A、B的电离能顺序________。
(6)写出C基态原子的电子排布式________。
高三化学填空题简单题查看答案及解析
-
下表为元素周期表的一部分。
氮
Y
X
硫
Z
完成下列填空:
(1)氮原子的电子排布式为__,Z元素在元素周期表中的位置为__。
(2)上表中原子半径最大的元素是(写元素符号)__,该原子的核外最外层电子占有__个轨道。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是__。
A.Y单质与H2S溶液反应,溶液变浑浊
B.在氧化还原反应中,1molY单质比1mol硫单质得电子多
C. Y的气态氢化物比硫的气态氢化物熔沸点高
(4)X与Z两元素的单质反应生成0.1molX的最高价化合物,恢复至室温,放热68.7 kJ,已知该化合物的溶、沸点分别为-69℃和58℃,写出该反应的热化学方程式:__。
(5)简述碳的同素异形体中某种单质的用途,并从晶体类型角度分析原因。___。
高三化学综合题中等难度题查看答案及解析
-
“椅子形状”的图包含了元素周期表前四周期的部分元素,其中A、B、C、D四种元素原子序数之和为77。
(1)写出A、B、C的价电子构型的电子排布式________。
(2)G原子的最外层电子占有________种能量不同的轨道。
(3)F形成的气态氢化物的电子式________。E和F简单气态氢化物的稳定性较强的是(写化学式)。
(4)A、B两元素都可以与氧元素形成化合物OA2、B2O,其分子的空间构型为折线型分子,对它们分子极性的判断正确的是( )。
a.都为非极性分子 b.都为极性分子 c.无法确定
在两种化合物中元素A、B的化合价分别为A,B________。
(5)气态原子失去一个电子所需要吸收的
能量叫做第一电离能(I)。G、E、D、B四种
原子的第一电离能大小变化如右图所示:
同一周期元素的气态原子的第一电离能
与原子半径的关系________。
高三化学填空题中等难度题查看答案及解析
-
现有部分短周期元素的原子结构如下表:
(1)写出X的元素符号:________,元素Y的最简单氢化物的化学式为________.元素符 号 元素原子结构
X原子结构示意图为 Y 最外层电子数是次外层电子数的2倍
Z
原子核内含有12个中子,且其离子的结构示意图为
(2)Z元素原子的质量数为________.
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为________.高三化学填空题中等难度题查看答案及解析
-
[物质结构与性质,13分]
(1)与铜同周期、基态原子最外层电子数相同的过渡元素,其基态原子的电子排布式 。
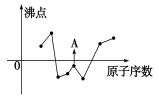
(2)下图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系。其中A点表示的单质是 (填化学式)。
键长/(pm)
B—F
B—Cl
B—Br
计算值
152
187
199
实测值
130
175
187
(3)三氟化硼分子的空间构型是 ;三溴化硼、三氯化硼分子结构与三氟化硼相似,如果把B-X键都当作单键考虑来计算键长,理论值与实测键长结果如右表。硼卤键长实测值比计算值要短得多,可能的原因是 。
(4)海产品添加剂多聚磷酸钠是由Na+与多聚磷酸根离子组成的,某种多聚磷酸根的结构如图。
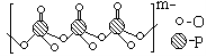
①磷原子的杂化类型为 。
②这种多聚磷酸钠的化学式为 。
(5)已知HF与F-通过氢键结合成HF
。判断HF
和HF
微粒间能否形成氢键,并说明理由。
。
高三化学填空题困难题查看答案及解析