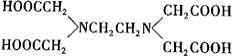-
[物质结构与性质,13分]
(1)与铜同周期、基态原子最外层电子数相同的过渡元素,其基态原子的电子排布式 。
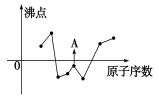
(2)下图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系。其中A点表示的单质是 (填化学式)。
| 键长/(pm) | B—F | B—Cl | B—Br |
| 计算值 | 152 | 187 | 199 |
| 实测值 | 130 | 175 | 187 |
(3)三氟化硼分子的空间构型是 ;三溴化硼、三氯化硼分子结构与三氟化硼相似,如果把B-X键都当作单键考虑来计算键长,理论值与实测键长结果如右表。硼卤键长实测值比计算值要短得多,可能的原因是 。
(4)海产品添加剂多聚磷酸钠是由Na+与多聚磷酸根离子组成的,某种多聚磷酸根的结构如图。
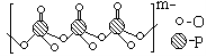
①磷原子的杂化类型为 。
②这种多聚磷酸钠的化学式为 。
(5)已知HF与F-通过氢键结合成HF 。判断HF
。判断HF 和HF
和HF 微粒间能否形成氢键,并说明理由。
微粒间能否形成氢键,并说明理由。
。
-
(8分)【化学-物质结构与性质】
A、B、C、D是四 种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。
回答下列问题:
(1)写出下列元素的符号:B________、C________。
(2)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是________,电负性最大的元素是________。
(3)已知元素周期表可按电子排布分为s区、q区等,则E元素在________区。
(4)画出A的核外电子排布式________。
-
化学选修:物质结构与性质分W、X、Y、M、Z为元素周期表中前四周期元素,且原子序数依次增大。W的基态原子中占据哑铃形原子轨道的电子数为3,X2+与W3-具有相同的电子层结构;W与X的最外层电子数之和等于Y的最外层电子数;Z元素位于元素周期表的第11列,M是第四周期中核外未成对电子数最多的元素。
请回答:
(1)Z的基态原子M层的电子排布式为 ;
(2)W的简单氢化物分子中W原子的 轨道与H原子的 轨道重叠形成W-Hσ键。(填轨道名称)
(3)比较Y的含氧酸酸性:HYO2 HYO(填“>”或“<”),原因为 。
(4)强酸条件下,M2O72-离子能与乙醇反应生成M3+离子,该反应的离子方程式为 。
(5)关于Z的化合物[Z(EDTA)]SO4(EDTA的结构简式如图)的说法正确的是( )
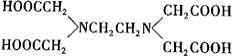
A.[Z(EDTA)]SO4中所含的化学键有离子键、共价键和配位键和氢键
B.EDTA中碳原子的杂化轨道类型为sp2、sp3
C.[Z(EDTA)]SO4的组成元素中第一电离能最大的是氧元素
D.[Z(EDTA)]SO4的外界离子的空间构型为正四面体
(6) ①离子型氢化物XH2的晶胞如图所示,其中阴离子的配位数为 。
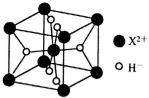
②XH2是一种储氢材料,遇水会缓慢反应,该反应的化学方程式为 。
③若该晶胞的密度为ρg.cm-3,则晶胞的体积为 nm3。
-
(化学——选修3:物质结构与性质)A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中第一电离能最大的是_________(填元素符号),其中C原子的核外电子排布式为:_________________;
(2)A有两种同素异形体,其中沸点较高的是______(填分子式),B的氢化物所属的晶体类型为___________;
(3)化合物CD3中心原子的杂化轨道类型为_________________;
(4)化合物D2A的立体构型为____________,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_________________________________________;
(5)CuSO4溶液可用作C4中毒的解毒剂,反应可生成C的最高价含氧酸和铜,该反应的化学方程式为:________________________________________;
(6)A和B形成化合物F,晶胞结构如图所示,晶胞参致a=0.566nm,晶胞中A原子的配位数为_________,列出晶体F的密度(g·cm-3)计算式________________________。(阿伏加德罗常数的值为NA)
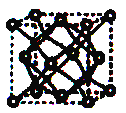
-
【化学—选修2:物质结构与性质】A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是________(填元素符号),其中C原子的核外电子排布式为________;
(2)单质A有两种同素异形体,其中沸点高的是________(填分子式),原因是________;A和B的氢化物所属的晶体类型分别为______和_______;
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为________,中心原子的杂化轨道类型_______;
(4)化合物D2A的立体构型为________,中心原子的价层电子对数为________,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_______;
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为________,晶胞中A原子的配位数为_______;列式计算晶体F的密度_______。
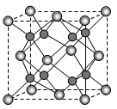
-
【化学—选修3:物质结构与性质】A、B、C、D为原子序数依次增大的四种元素,A2﹣和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是 (填元素符号),其中C原子的核外电子排布式为 ;
(2)单质A有两种同素异形体,其中沸点高的是 (填分子式),原因是 ,A和B 的氢化物所属的晶体类型分别为 和 ;
(3)C和D反应可生成组成比为1︰3的化合物E, E的立体构型为 ,中心原子的杂化轨道类型为 ;
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a = 0.566 nm,F的化学式为 ,列式计算晶体F的密度(g.cm-3) 。
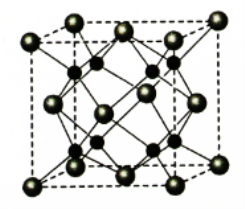
-
[化学—选修3:物质结构与性质]A、B、C、D为原子序数依次增大的四种元素,A2-和B2+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是 (填元素符号),其中C原子的次外层电子排布式为 。
(2)单质A有两种同素异形体,其中沸点高的是 (填分子式),原因是 ;B的氢化物所属的晶体类型是 ,B单质所形成的晶体,一个晶胞平均含有 个原子。
(3)C和D反应可生成组成比为1:5的化合物E,E的分子式为 ,已知该分子的空间构型为三角双锥,则其中两个Cl原子被F原子所替代得到的产物结构有 种。
(4)化合物D2A的立体构型为 ,中心原子的价层电子对数为 ,单质D与Na2SO3溶液反应,其离子方程式为 。
(5)A和B能够形成化合物F,F晶体中的B2+离子的排列方式如图所示,
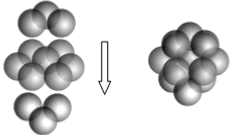
①每个B2+周围最近的等距离的B2+离子有 个。
②已知F的晶胞参数是a0=0.54nm,它的密度为 (只列式不作计算,阿伏加德罗常数为6.02×1023mol-1)。
-
[化学—选修3:物质结构与性质] A、B、C、D为原子序数依次增大的四种元素,A2-和B2+具有相同的电子构型;C、 D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是________(填元素符号),其中C原子的次外层电子排布式为_____________________________。
(2)单质A有两种同素异形体,其中沸点高的是______(填分子式),原因是___________________;B的氢化物所属的晶体类型是_____________,B单质所形成的晶体,一个晶胞平均含有_____________个原子。
(3)C和D反应可生成组成比为1:5的化合物E, E的分子式为_______,已知该分子的空间构型为三角双锥,则其中两个Cl原子被F原子所替代得到的产物结构有________种。
(4)化合物D2A的立体构型为______________,中心原子的价层电子对数为_______,单质D与Na2SO3溶液反应,其离子方程式为__________________________________________。
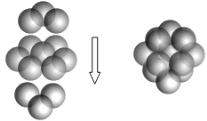
(5)A和B能够形成化合物F,F晶体中的B2+离子的排列方式如下图所示,
①每个B2+周围最近的等距离的A2-离子有_____________个。
②已知F的晶胞参数是a0=0.54nm,它的密度为________________________(只列式不作计算,阿伏加德罗常数为6.02×1023mol-1)。
-
(选做题)(物质结构与性质)(8分)已知A、B、C、D、E、F都是短周期的元素,它们的原子序数依次递增。A原子的电子层数与它的核外电子总数相同,而B原子的最外层电子数是次外层的2倍,C的氢化物可使湿润的红色石蕊试纸变蓝,B和D可以形成两种气态化合物,E原子核外电子总数比B的2倍少1,F在本周期元素中原子半径最小。则:
(1)A、B、C、D、E、F的名称分别是________。
(2)在A至F中任选元素,写出一种含极性键的非极性分子的分子式,写出一种含非极性键的离子化合物的电子式________。
(3)由B和D组成,且B和D的质量比为3∶8的化合物的结构式是 ,
该化合物分子中B原子的杂化方式为
(4)E和F形成的化合物为________晶体 。
-
[化学—选修3:物质结构与性质]
A、B、C、D、E为原子序数依次增大的前四周期的元素,A的核外电子总数与其周期数相同。B是同周期元素未成对电子数最多的元素,C的最外层电子数为其电子层数的3倍,B与D同族;回答下列问题:
(1).D的一种单质,难溶于水,较易溶于苯且易自燃,其立体结构为_______________,D原子的杂化类型为_______________。
(2).A和B的单质反应可生成化合物M,常温下M为气态,易液化可作制冷剂。A和D的单质反应得到化合物N,M的沸点________(填“大于”、“小于”、或“等于”)N的沸点,原因是_______________。
(3).已知N可以与E的一种盐溶液反应,生成红色固体单质和两种高沸点酸。E原子的外围电子排布图为____________________。写出相应的化学反应方程式:____________________。
(4).将M通入E的硫酸盐溶液中,可得到深蓝色透明溶液,再向溶液中加入一定量的乙醇,有深蓝色晶体析出。写出离子反应方程式:__________________,加入乙醇的作用是________________。
(5).E和C能形成化合物G,其晶体结构如图25所示,G的化学式为__________。若两个氧原子间最短距离为apm,列式计算晶体G的密度_______g.cm-3



。判断HF
和HF
微粒间能否形成氢键,并说明理由。
 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。