-
BaCl2·xH2O中结晶水数目可通过重量法来确定:
①称取1.222g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;
②过滤并洗涤沉淀;
③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧到恒重,称得沉淀质量为1.165g。
回答下列问题:
(1)在操作②中,需要先后用稀硫酸和____________ 洗涤沉淀;检验沉淀中氯离子是否洗净的方法是____________ 。
(2)计算BaCl2·xH2O中的x=__________ 。
(3)操作③中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原为BaS,这使x的测定结果__________ (填“偏低”、“偏高”或“不变”)。
高一化学简答题困难题查看答案及解析
-
长期存放的亚硫酸钠可能会被部分氧化,现通过实验来测定某无水亚硫酸钠试剂的纯度。实验步骤如下:
①称量ag样品,置于烧杯中。
②加入适量蒸馏水,使样品溶解。
③加入稀盐酸,使溶液呈强酸性,再加过量的BaCl2溶液。
④过滤,用蒸馏水洗涤沉淀。
⑤加热干燥沉淀物。
⑥将沉淀物冷却至室温后,称量。
⑦重复⑤、⑥操作直到合格,最后得到bg固体。
回答下面问题:
(1)本实验中是否能用Ba(NO3)2代替BaCl2?________;其理由是________。
(2)步骤③中加盐酸使溶液呈强酸性的目的是_____________________。
(3)步骤⑦的“合格”标准是:_____________________。
(4)实验测得样品中无水亚硫酸钠占原有样品的质量分数是_____________________。(列出算式,不需化简)
高一化学实验题简单题查看答案及解析
-
某化学兴趣小组测定某FeCl3样品(含有少量FeCl2杂质)中铁元素的质量分数,实验时按以下步骤进行:
①称量ag样品,置于烧杯中,
②加入适量的蒸馏水,使样品溶解,然后准确配制成250mL溶液
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全
⑤过滤,洗涤沉淀
⑥将沉淀声称到坩埚内加热,搅拌直到固体全部由红褐色变为红棕色后在干燥器中冷却到室温后,称量
⑦…根据上面叙述,回答
(1)如图所示仪器中,本实验步骤①②中必须用到的仪器是______.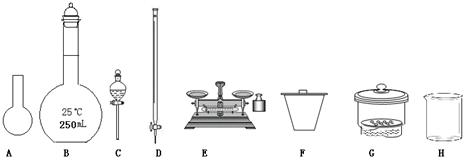
(2)写出步骤③和④中发生反应的离子方程式______
(3)洗涤是洗去附着在沉淀上的______(写离子符号).洗涤沉淀的操作是______检验沉淀已洗净的方法是______
(4)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为______(列出算式,不需化简)
(5)该兴趣小组中甲学生认为:实验步骤中不加氯水,其余步骤不变,仍可达到实验目的,你认为甲学的观点是否正确______(填“正确”或“错误”)请说明理由(必要时可用化学方程式表示)______.高一化学解答题中等难度题查看答案及解析
-
为测定碳酸钠纯度(只含有少量氯化钠),学生设计了如下两个实验方案。
[方案1]称取
样品,置于小烧杯中,加适量水完全溶解;向小烧杯中加入足量氢氧化钡溶液,过滤,洗涤、干燥沉淀,称量沉淀的质量为19.700克,计算。
(1)写出生成沉淀的反应方程式__________________。
(2)过滤操作需要的玻璃仪器__________________。
(3)计算碳酸钠的质量分数为______________(保留两位小数)。
[方案2]用下图装置,排液法测定
的体积,并根据样品质量和
的体积计算
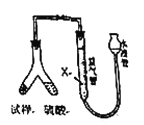
(4)为了减小测定
的体积误差,量气管中加入的液体
为______(填化学式)。
(5)通过实验,测得该试样中碳酸钠的质量分数偏高,产生这种现象的原因可能是______。
A.测定气体体积时未冷却至室温
B.气体进入量气管前未用浓硫酸干燥
C.
型管中留有反应生成的气体
D.反应结束后读数时水准管的水面高于量气管的水面
高一化学实验题中等难度题查看答案及解析
-
一种由CuO和KHC2O4溶液反应的到的蓝色结晶[KaCub(C2O4)c•dH2O]。为测定其组成,进行了如下实验:
步骤1称取3.5400 g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100 mL溶液A.
步骤2量取20.00 mLA溶液,滴加0.2000 mol• L-1 KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00 mL。
步骤3另取20.00 mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16 g。
己知:步骤2 中发生反应:2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ +10CO2↑ + 8H2O。
(1)步骤1中配制溶液A时,需要用到的玻璃仪器有烧杯、玻璃棒、_____。
(2)3.5400 g 该样品中含 n(C2O42-)= ____mol。
(3)3.5400 g 该样品中含 n(Cu2+)= ____mol。
(4)通过计算确定该蓝色晶体的化学式__________(计算过程)。
高一化学计算题困难题查看答案及解析
-
一种由CuO和KHC2O4溶液反应的到的蓝色结晶[KaCub(C2O4)c•dH2O]。为测定其组成,进行了如下实验:
步骤1称取3.5400 g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100 mL溶液A.
步骤2量取20.00 mLA溶液,滴加0.2000 mol• L-1 KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00 mL。
步骤3另取20.00 mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16 g。
己知:步骤2 中发生反应:2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ +10CO2↑ + 8H2O。
(1)步骤1中配制溶液A时,需要用到的玻璃仪器有烧杯、玻璃棒、_____。
(2)3.5400 g 该样品中含 n(C2O42-)= ____mol。
(3)3.5400 g 该样品中含 n(Cu2+)= ____mol。
(4)通过计算确定该蓝色晶体的化学式__________(计算过程)。
高一化学计算题困难题查看答案及解析
-
确定某溶液中含有SO42-,下列方案中正确的是
A. 先加入BaCl2溶液产生白色沉淀,再加入足量稀盐酸沉淀不溶解
B. 先加入足量稀盐酸无沉淀,再加入BaCl2溶液产生白色沉淀
C. 先加入足量稀硝酸无沉淀,再加入Ba(NO3)2溶液产生白色沉淀
D. 先加入Ba(NO3)2溶液无沉淀,再加入足量稀硝酸产生白色沉淀
高一化学单选题困难题查看答案及解析
-
确定某溶液中含有SO42-,下列方案中正确的是
A.先加入BaCl2溶液产生白色沉淀,再加入足量稀盐酸沉淀不溶解
B.先加入足量稀盐酸无沉淀,再加入BaCl2溶液产生白色沉淀
C.先加入足量稀硝酸无沉淀,再加入Ba(NO3)2溶液产生白色沉淀
D.先加入Ba(NO3)2溶液无沉淀,再加入足量稀硝酸产生白色沉淀
高一化学选择题中等难度题查看答案及解析
-
确定某溶液中含有SO42-,下列方案中正确的是
A.先加入BaCl2溶液产生白色沉淀,再加入足量稀盐酸沉淀不溶解
B.先加入足量稀盐酸无沉淀,再加入BaCl2溶液产生白色沉淀
C.先加入足量稀硝酸无沉淀,再加入Ba(NO3)2溶液产生白色沉淀
D.先加入Ba(NO3)2溶液无沉淀,再加入足量稀硝酸产生白色沉淀
高一化学选择题困难题查看答案及解析
-
通过加入适量的化学药品,采用恰当的分离提纯方法,除去某溶液里溶解的杂质,下列做法中不正确 的是(括号内的物质为杂质)( )
A NaCl溶液(BaCl2) 加Na2CO3溶液,过滤,再加适量盐酸 B KNO3溶液(AgNO3) 加适量KCl溶液,过滤 C NaCl溶液(I2) 加酒精,分液 D KNO3溶液(I2) 加CCl4,分液
A.A
B.B
C.C
D.D高一化学选择题中等难度题查看答案及解析