-
(10分)已知X、Y、Z、W是短周期中四种非金属元素,它们的原子序数依次增大。X元素原子形成的离子只有一个质子;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;Y原子的最外层电子数是内层电子数的2倍。
(1)写出下列字母所代表元素的名称:X________;Y________;Z________;W________。
(2)X单质和Z单质在一定条件下反应生成化合物E,写出该反应的化学方程式(并注明反应条件);Y单质和W单质(足量)在加热条件下反应生成化合物F,则F分子的空间构型为,电子式为。
(3)这四种元素可组成X、Y、Z、W原子个数比为5∶1∶1∶3的化合物,该化合物的水溶液与足量浓NaOH溶液反应的离子方程式为:
___________________________________________________________________
高二化学填空题简单题查看答案及解析
-
X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。
下列说法正确的是 ( )
A. 五种元素的原子半径从大到小的顺序是:M﹥W>Z>Y>X
B. Z与同主族相邻元素的非金属性强弱,可通过它们的氧化物对应水化物的酸性强弱来判断
C. X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物
D. 用M单质的熔点高于其氧化物的熔点
高二化学单选题中等难度题查看答案及解析
-
结构决定性质,性质决定用途;已知X、Y、Z、W是元素周期表中短周期中的四种非金属元素,它们的原子序数依次增大,X元素的原子形成的阳离子就是一个质子,Z、W在元素周期表中处于相邻的位置,Z的单质在常温下均为无色气体,W原子的最外层电子排布是nSn npn+2,Y原子的最外层电子数是内层电子数的2倍。试回答:
(1)写出W元素的元素符号和该原子基态的电子排布式:__ _____
(2)写出Z元素的原子结构示意图和该原子基态的电子排布图:_ _____
(3)X单质和Z单质在一定条件下反应生成化合物E,则E的电子式是:________。E可以进行喷泉实验的主要原因是:________。
(4)仅由X、Z、W三种元素组成的某种盐是一种速效肥料,但长期施用会使土壤酸化,有关的离子反应方程式为___________ __________________ ________
(5)这四种元素可组成原子个数比为5∶1∶1∶3的化合物(按X、Y、Z、W的顺序)为(写名称)________,该化合物的浓溶液与足量NaOH热浓溶液反应的离子方程式为:____________ __ __
高二化学推断题困难题查看答案及解析
-
(15分)元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大。其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g·L—1,C元素原子的最外层电子数是其内层电子数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):
其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、
丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应。请回答下列问题:
(1)写出化合物甲的电子式:________________。
(2)写出化合物甲的水溶液与D元素对应的金属阳离子反应的离子方程式________;
写出均含有F元素的乙与丁在溶液中发生反应的离子方程式 ________________。
(3)由A、C元素组成化合物的戊和A、E元素组成的化合物己,式量均为34。其中戊的熔沸点高于己,其原因是:________。
(4)复盐是指由2种或2种以上阳离子和一种酸根离子组成的盐。请写出由A、B、C、E、F元素组成的一种具有还原性的复盐庚的化学式________。该复盐是一种重要的化学试剂,据中学课本介绍,工业上常用如下方法制取:将一定量的两种盐配成混合溶液,再加热浓缩混合溶液,冷却至室温则析出带有6个结晶水的该复盐晶体。写出相关反应的化学方程式________,析出该复盐晶体的原理是________ ________ 。
高二化学填空题简单题查看答案及解析
-
X、Y、Z、W、M五种短周期元素的原子序数依次增大.已知X元素的原子形成的离子就是一个质子,Z、W是同周期的相邻元素,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍. M是地壳中含量最高的金属元素.用化学用语回答下列问题:
(1)W的周期表位置为________;Z的最简气态氢化物的电子式________;
(2)M元素单质与同周期的最活泼金属的氢氧化物反应的离子方程式是________;
(3)X与Y形成的最简化合物的空间构型为________.高二化学填空题中等难度题查看答案及解析
-
五种短周期元素A、B、C、D、E的原子序数依次增大,其中只有C为金属元素。A和C同主族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是__________,非金属性最强的是__________(填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是__________(用化学式表示);
(3)D在周期表的位置为__________
(4)A和B形成的化合物与A和E形成的化合物反应,产物的化学式为__________,该化合物溶于水,显__________性(填“酸”、“碱”、“中”)原因是__________(用离子方程式表示);
(5)D和E可形成一种所有原子都满足8电子结构的化合物,其化学式为__________。
高二化学推断题困难题查看答案及解析
-
原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期,其中A原子核只有一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体型分子,D原子外围电子排布为3d104s1。
请回答下列问题:
(1)这四种元素中电负性最大的是________(填元素符号)、第一电离能最小的是________(填元素符号) ;
(2)C所在的主族元素气态氢化物中,沸点最低的是________(填化学式);
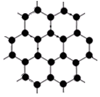
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为________;
(4)D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是________(填选项序号);
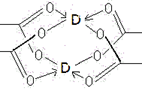
①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如下图:

已知D的硫化物为黑色难溶性物质,请书写第⑤反应的离子方程式:________。
高二化学填空题中等难度题查看答案及解析
-
A、B、C、D、E、F均为周期表中前四周期元素,其原子序数依次增大,其中A、B、C为短周期非金属元素。A是形成化合物种类最多的元素;B原子基态电子排布中只有一个未成对电子;C是同周期元素中原子半径最小的元素;D的基态原子在前四周期元素的基态原子中单电子数最多;E与D相邻,E的某种氧化物X与C的氢化物的浓溶液加热时反应常用于实验室制取气态单质C;F与D的最外层电子数相等。
回答下列问题(相关回答均用元素符号表示):
(1)D的基态原子的核外电子排布式是______________。
(2)B的氢化物的沸点比C的氢化物的沸点________(填“高”或“低”),原因是______________________。
(3)A的电负性________(填“大于”或“小于”)C的电负性,A形成的氢化物A2H4中A的杂化类型是________。
(4) X在制取C单质中的作用是________,C的某种含氧酸盐常用于实验室中制取氧气,此酸根离子中化学键的键角________(填“>”“=”或“<”)109°28′。

(5)已知F与C的某种化合物的晶胞结构如图所示,则该化合物的化学式是__________________,若F与C原子最近的距离为a cm,则该晶体的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数的数值为NA)。
高二化学填空题困难题查看答案及解析
-
Q、W、X、Y、Z五种短周期主族元素,它们的原子序数依次增大。 已知:X和X、W和Y 分别位于同主族且W、Y质子数之和是Q、X质子数之和的2倍。下列说法不正确的是
A. Q、W、Y不可能形成离子化合物
B. 在同周期元素形成的简单气态氢化物中,Z的氢化物沸点最高
C. 原子半径的大小顺序:X>Y>W
D. X的最高价氧化物对应水化物具有酸性
高二化学选择题中等难度题查看答案及解析
-
X、Y、Z、W是原子序数依次增大的四种短周期元素.其中只有一种是金属元素,X、W同主族且能形成一种离子化合物WX;Y的气态氢化物、最高价氧化物的水化物可反应生成一种盐;Z原子的最外层电子数与其电子总数之比为3︰4。下列说法中正确的是
A.原子半径:W>Z>Y>X
B.氢化物稳定性:Y>Z
C.WY3中只有离子键没有共价键
D.X与Z可形成l0电子分子和18电子分子
高二化学选择题困难题查看答案及解析