-
汽车在现代生活中扮演着越来越重要的角色,但其尾气(碳氢化合物、氮氧化物及一氧化碳等)带来的环境污染越来越明显,汽车尾气的治理已经迫在眉睫。
(1)尾气中的CO主要来自于汽油的不完全燃烧。
①有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g) ΔH= +221kJ·mol-1,简述该设想能否实现______(填“是”或“否”)依据是:_______________________________________。
②研究表明:反应CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
该反应的ΔH______0(填“>”或“<”)若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020mol·L﹣1,在该条件下达到平衡时,CO的转化率为 。
(2)用CO做燃料电池电解NaCl溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极,转移0.4mol e-后,断开K。
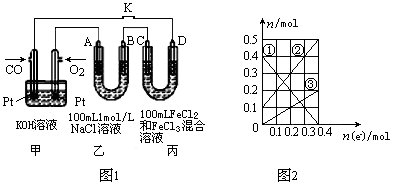
①乙中产生的气体在标准状况下的体积为 。
②丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要 mL 5.0mol·L﹣1 NaOH溶液。
(3)电解法处理氮氧化合物是目前大气污染治理的一个新思路,原理是将NOx在电解池中分解成无污染的N2和O2除去,如图示,两电极间是固体氧化物电解质,在一定条件下可自由传导O2-,电解池阴极反应为__________________。

(4)尾气中的碳氢化合物,如甲烷,可以用来制备氢气。其反应方程式为:
CH4(g)+H2O(g) CO(g)+3H2(g) ΔH = +206.2kJ/mol [其中投料比n(CH4):n(H2O)=1:1]。对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP,分压=总压×物质的量分数)。平衡时CH4的转化率与温度、压强(总压)的关系如图所示:
CO(g)+3H2(g) ΔH = +206.2kJ/mol [其中投料比n(CH4):n(H2O)=1:1]。对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP,分压=总压×物质的量分数)。平衡时CH4的转化率与温度、压强(总压)的关系如图所示:
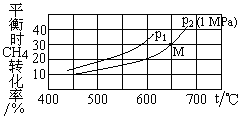
则p1__ p2 (填“>”或“<”),p2时M点的平衡常数KP=________(小数点后保留3位)。
-
汽车作为曾经推动人类文明向前跃进的现代社会产物,在给人类生活带来便捷舒适的同时,对自然生态环境的恶化也带来了害处,它是城市空气的重要污染源之一。
(1)汽车尾气中的大气污染物有(写化学式)________。
(2) 治理尾气的方法之一是在汽车的排气管上装一个“催化转化器”(用铂、钯合金制催化剂),它的作用是使CO和NO反应,生成两种气体,其中一种可以参与植物的光合作用,另一种是空气中含量最多的气体。请写出CO与NO反应的化学方程式 ________。
(3)氢气做燃料的三个十分突出的优点是__________________、__________________、___________,就目前情况看,氢气作燃料的汽车要投入使用前,你认为还要研究解决的问题________________________________。
-
随着经济发展现在汽车越来越多,同时也带来了交通拥挤和空气污染.汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )
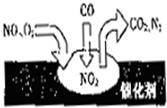
A.反应中NO为氧化剂、N2为氧化产物
B.汽车尾气的主要污染成分包括CO和NO
C.NO和O2必须在催化剂表面才能反应
D.催化转化总反应为NO+O2+CO2  CO+N2
CO+N2
-
(10分)(a)铁元素在人类生活中扮演着非常重要的角色,不仅仅是重要的建筑材料,也是人体必须的微量元素。每年钢铁的腐蚀带来巨大的经济损失。某校研究小组在实验室中模拟钢铁在自然环境下的腐蚀,设置如下装置,几天后观察结果:
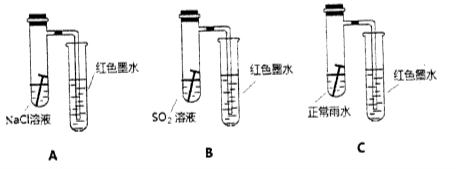
请回答下列问题:
(1)请比较以上三个装置中右侧导管中红墨水的高度: > > 。请写出A装置中,钢铁锈蚀时正极反应的电极反应式 。
(2)钢铁的防腐有重大的意义,生活中常将金属制品放在干燥处或者涂上矿物油予以保护,现请你从电化学角度设计一种方法保护下图中钢铁以免被腐蚀,请将下图完成:

(b)下面是一种常见补铁药品说明书中的部分内容:该药品含Fe2+:33%~36%,不溶于水但能溶于人体中的胃酸,与Vc(维生素C)同服可增加本品吸收。某乙同学采用在酸性条件下用高锰酸钾标准溶液滴定的方法测定该药品是否合格,反应原理为:
5 Fe2++8H++MnO4-=5 Fe3++Mn2++4H2O
准确称量上述药品10.00g,将其全部溶于试剂1中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
(3)该实验中的试剂1是 (填序号)。
A.蒸馏水 B.稀盐酸 C.稀硫酸 D.稀硝酸
(4)请简述判断滴定终点的现象: 。
(5)请通过计算,说明该药品含铁量是否合格 (填“合格”或“不合格”)(Fe的摩尔质量为56g/mol)
-
燃煤和汽车尾气是造成空气污染的原因之一,雾疆天气肆虐给人类健康带来了严重影响,化学在解决雾霾污染中发挥了重要作用。
(1)煤燃烧产生的烟气中含有氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
己知:
CH4(g)+2NO2(g)  N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1
N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1
2NO2(g)  N2O4(g) △H=-56.9kJ·mol-1
N2O4(g) △H=-56.9kJ·mol-1
H2O(g)=H2O(l) △H=-44.0kJ·mol-1
①写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式________________。
②反应CH4(g)+2NO2(g)  N2(g)+CO2(g)+2H2O(l)在恒温恒容容器中达到平衡,下列叙述不能作为判断该反应达到平衡状态标志的是___________。
N2(g)+CO2(g)+2H2O(l)在恒温恒容容器中达到平衡,下列叙述不能作为判断该反应达到平衡状态标志的是___________。
A.容器中的压强不变 B.混合气体的密度不变
C.2v正(NO2)= v 逆(N2) D.c(CH4)= c(N2)
(2)CO、CO2 是火力发电厂及汽车尾气的主要成分,为减少对环境造成的影响,采用以下方法将其资源化利用。
①以CO 为电极燃料,以熔融K2CO3为电解质,和O2组成燃料电池。请写出该电池的负极电极反应式_____________________。
②在铝矾土作催化剂、773K条件下,3molCO与1.5molSO2反应生成3molCO2和0.75mol硫蒸气,该反应可用于从烟道气中回收硫,写出该反应的化学方程式_______________。
③在汽车的排气管上增加一个补燃器,并不断补充O2使其浓度保持为4.0×10-4mol·L-1,发生反应2CO(g)+O2(g)  2CO2(g)。某温度下测得汽车尾气中CO、CO2 气体的浓度分别为2.0×10-6 mol·L-1、4.0×10-4 mol·L-1,则该条件下反应的平衡常数K=___________。
2CO2(g)。某温度下测得汽车尾气中CO、CO2 气体的浓度分别为2.0×10-6 mol·L-1、4.0×10-4 mol·L-1,则该条件下反应的平衡常数K=___________。
-
(13分)二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一。
(1)汽车尾气中主要含有CO、NO2、SO2、CO2气体,其中________能导致光化学烟雾的形成;
目前采用的是在汽车排气装置中安装一个净化器,可以有效的将尾气中的有害气体转化。如:CO(g)+NO2(g) NO(g)+CO2(g) △H=-akJ·mol—1(a>0)2CO(g)+2NO2(g) N2(g)+2CO2(g) △H=-bkJ·mol—1(b>0)
据此回答:若用标准状况下3.36升CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为mol,放出的热量为________kJ(用含有a和b的代数式表示)。
⑵新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为________(只要求写一种)。
(3)工业上生产硫酸时,将SO2氧化为SO3是关键一步。
①某温度下,SO2(g)+1/2O2(g) SO3(g);△H= —98 kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=________。
SO3(g);△H= —98 kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=________。
②一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:2SO2(g)+O2(g) 2SO3(g)达到平衡后改变下述条件SO3 的体积分数变大的是________
2SO3(g)达到平衡后改变下述条件SO3 的体积分数变大的是________
A.保持温度和容器压强不变,充入2mol SO3
B.保持温度和容器体积不变,充入2mol N2
C.保持温度和容器体积不变,充入0.5mol SO2和0.25mol O2
E.升高温度 F.移动活塞压缩气体
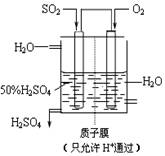
(4)某人设想以右上图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式:________
________。
-
二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一.
(1)汽车尾气中主要含有CO、NO2、SO2、CO2气体,其中______能导致酸雨的形成;目前采用的是在汽车排气装置中安装一个净化器,可以有效的将尾气中的有害气体转化.如:
CO(g)+NO2(g)═NO(g)+CO2(g)△H=-akJ•mol-1(a>0)
2CO(g)+2NO(g)═N2(g)+2CO2(g)△H=-bkJ•mol-1(b>0)
据此回答:若用标准状况下3.36升CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为______mol,放出的热量为______kJ(用含有a和b的代数式表示).
(2)在火力发电厂产生的废气中含有SO2、N2、CO等气体,为除去SO2,常用Ca(OH)2悬浊液洗涤废气,为了废物利用,再通入空气使反应产物转化为石膏.写出有关的化学反应方程式______.
(3)硫酸工业生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g) 2SO3(g)△H=-196.kJ•mol-1
2SO3(g)△H=-196.kJ•mol-1
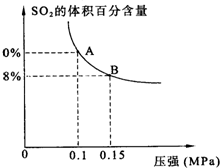
某温度下达到平衡时,SO2的体积百分含量与体系的总压强的关系如图所示:
据此图回答下列问题:
①平衡状态由A变到B时,反应体系______(填“吸收”或“释放”)能量.
②将5molSO2和7molO2通入10L密闭容器中,平衡时体系的总压强为0.1MPa.该反应在该温度下的平衡常数等于______.
-
化学在生产和生活中有着重要的作用,下列有关说法正确的是( )
A. 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的
B. 利用二氧化碳制造可降解塑料,可以减缓“白色污染”,减轻温室效应
C. 埃博拉病毒可用乙醇、次氯酸钠溶液、双氧水消毒,其消毒原理相同
D. 通过化学变化可以实现12C与14C间的相互转化
-
化学在人类生活中扮演重要角色,下列说法正确的是
A. 蔬菜和粗粮中富含纤维素,纤维素在人体中酶的作用下能水解成葡萄糖
B. 混凝法、中和法、沉淀法、氧化还原法是工业处理废水常用的方法
C. 可只用淀粉溶液检验食盐中是否加碘
D. 鸡蛋清溶液中加人饱和Na2SO4溶液,有沉淀生成是因为蛋白质变性
-
化学在人类生活中扮演重要角色,下列说法正确的是
A. 蔬菜和粗粮中富含纤维素,纤维素在人体中酶的作用下能水解成葡萄糖
B. 混凝法、中和法、沉淀法、氧化还原法是工业处理废水常用的方法
C. 装潢涂料用苯作溶剂比用水作溶剂好
D. 鸡蛋清溶液中加入饱和Na2SO4溶液,有沉淀生成是因为蛋白质变性
H2(g)+CO2(g)平衡常数随温度的变化如下表所示:

CO(g)+3H2(g) ΔH = +206.2kJ/mol [其中投料比n(CH4):n(H2O)=1:1]。对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP,分压=总压×物质的量分数)。平衡时CH4的转化率与温度、压强(总压)的关系如图所示:





