-
已知NH4Cl浓度小于0.1mol/L时,溶液PH>5.1现用0.1mol/L HCl溶液来滴定10mL 0.05mol/L氨水,用甲基橙作指示剂,达到终点时所用盐酸的体积( )
A.=10mL B.=5mL C.>5mL D.<5mL
高三化学选择题中等难度题查看答案及解析
-
已知当NH4Cl溶液的浓度小于0.1mol/L时,其pH>5.1。现用0.1mol/L的盐酸滴定l0mL0.05mol/L的氨水,用甲基橙作指示剂达到终点时所用盐酸的量应是()
A.10mL B.5mL C.大于5mL D.小于5mL
高三化学单选题简单题查看答案及解析
-
已知c(NH4Cl)≤0.1mol/L时,溶液pH>5.1。现用0.1mol/L盐酸滴定10mL0.05mol/L氨水,用甲基橙作指示剂,达到滴定终点,所用盐酸的体积为( )
A.10mL B.5mL C.大于5mL D.小于5mL
高三化学单选题中等难度题查看答案及解析
-
室温下,用0.1mol·L-1HCl溶液滴定某浓度的NaoH溶液,达到滴定终点时不慎多加1滴HCl溶液(1滴溶液的体积约为0.04mL),继续加水至40mL,所得溶液的pH是( )
A.1 B.2 C.4 D.7.2
高三化学选择题简单题查看答案及解析
-
用0.1 mol·L-1 NaOH溶液分别滴定体积均为20 mL、浓度均为0.1 mol·L-1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图:
(1)HX为 酸(填“强”或“弱”)。
(2)N点pH>7的原因是(用化学用语表示)______________。
(3)下列说法正确的是__________(填字母)。
a. M点c(HX)<c(X-)
b. M点c(Na+)>c(OH-)
c. P点c(Cl-)=0.05 mol·L-1
高三化学填空题简单题查看答案及解析
-
用0.1 mol·L-1 NaOH溶液分别滴定体积均为20 mL、浓度均为0.1 mol·L-1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图:
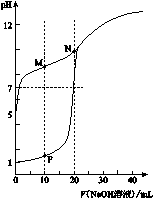
(1)HX为 酸(填“强”或“弱”)。
(2)N点pH>7的原因是(用化学用语表示)__________。
(3)下列说法正确的是_________(填字母)。
a. M点c(HX)<c(X-)
b. M点c(Na+)>c(OH-)
c. P点c(Cl-)=0.05 mol·L-1
高三化学填空题困难题查看答案及解析
-
用0.1mol•L-1NaOH溶液分别滴定体积均为20mL、浓度均为0.1mol•L-1HCl溶液和HX溶液,溶液的pH随加入的NaOH溶液体积变化如图。下列说法不正确的是( )
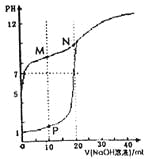
A.NaX溶液呈碱性 B.P点:c(Na+)>c(H+)
C.M点:c(HX)+c(X-)=2c(Na+) D.M点水电离程度小于N点
高三化学单选题中等难度题查看答案及解析
-
用0.1mol•L-1NaOH溶液分别滴定体积均为20mL、浓度均为0.1mol•L-1HCl溶液和HX溶液,溶液的pH随加入的NaOH溶液体积变化如图。下列说法不正确的是( )
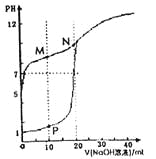
A.NaX溶液呈碱性 B.P点:c(Na+)>c(H+)
C.M点:c(HX)+c(X-)=2c(Na+) D.M点水电离程度小于N点
高三化学单选题中等难度题查看答案及解析
-
用0.1mol•L-1NaOH溶液分别滴定体积均为20mL、浓度均为0.1mol•L-1HCl溶液和HX溶液,溶液的pH随加入的NaOH溶液体积变化如图。下列说法不正确的是( )
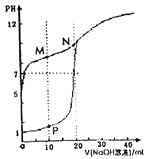
A.NaX溶液呈碱性 B.P点:c(Na+)>c(H+)
C.M点:c(HX)+c(X-)=2c(Na+) D.M点水电离程度小于N点
高三化学单选题中等难度题查看答案及解析
-
室温下,用0.1 mol·Lˉ1 NaOH溶液分别滴定体积均为20mL、浓度均为0.1 mol·Lˉ1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图,下列说法不正确的是
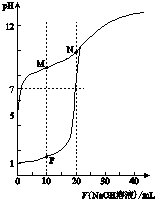
A.HX为弱酸
B.M点c(HX)—c(X-)﹥c(OH—)—c(H+)
C.将P点和N点的溶液混合,呈酸性
D.向N点的溶液中通入HCl至pH=7:c(Na+) ﹥c(HX) = c(Cl—) ﹥c(X—)
高三化学选择题困难题查看答案及解析