-
高纯度的氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如下:

已知1:溶液Ⅰ中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子
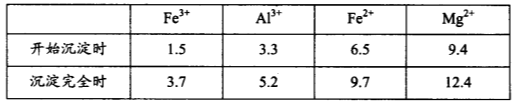
2:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
| Fe3+ | Al3+ | Fe2+ | Mg2+ |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)向溶液Ⅰ中加入X的作用是____________。
(2)向溶液Ⅰ中加入的两种试剂先后顺序是______________(填化学式)。
(3)加入H2O2溶液反应的离子方程式是__________________。
(4)下图是Mg2+转化率随温度t的变化示意图:
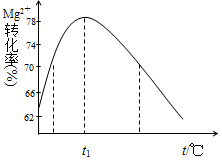
① t1前Mg2+转化率增大的原因是____________;t1后Mg2+转化率下降的原因是(用化学方程式表示)______________。
② 向溶液Ⅱ中加入氨水反应的离子方程式是_________。
-
高纯度的氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢
氧化镁,简要工艺流程如下:

己知1:溶液I中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子
2:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
(1)Mg在周期表中的位置________________,Si的原子结构示意图为______________。
(2)向溶液I中加入X的作用是________________________________。
(3)向溶液I中加入的两种试剂先后顺序是__________________(填化学式)。
(4)加入H2O2溶液反应的离子方程式是______________________。
(5)下图是溶液Ⅱ中Mg2+转化率随温度t的变化示意图:
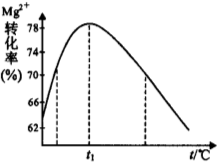
①向溶液Ⅱ中加入氨水反应的离子方程式是________________。
②t1前Mg2+转化率增大的原因是______________;t1后Mg2+转化率下降的原因是(用化学方程式表示)_____________________。
-
高纯度的氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如图所示。
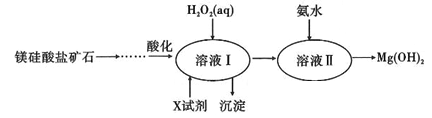
已知:①溶液I中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子;
②几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
| Fe3+ | A13+ | Fe2+ | Mg2+ |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)镁硅酸盐矿石中有一种俗称茧青石,化学式为Mg2Al4Si5018,它的氧化物形式为________。
(2)如何检验溶液I中的Fe2+?____________。
(3)向溶液I中加入X试剂的作用是________,加入的两种试剂的先后顺序是_______(填化学式)。
(4)从溶液I中得到沉淀的合理pH为________(填序号)。
A. 3.3 B. 3.7 C. 5.8 D.9.5
(5)加入H2O2溶液反应的离子方程式是__________。
(6)如图是溶液II充分反应时,Mg2+的转化率随温度T的变化示意图。
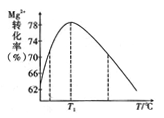
①向溶液II中加入氨水反应的离子方程式是____________。
②T1前Mg2+转化率增大的原因是___________; T1后Mg2+转化率下降的原因是__________(用化学方程式和文字表示)。
-
Ⅰ.高纯度氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如图所示:
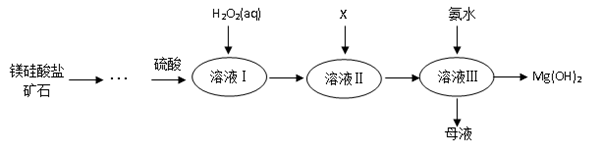
已知:
①溶液Ⅰ中除含Mg2+、SO42‒外,还含有少量Fe3+、Al3+、Fe2+等离子;
②常温下,几种金属离子开始沉淀和沉淀完全时的pH如下表所示:
| 金属离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ |
| 开始沉淀时的pH | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时的pH | 3.7 | 5.2 | 9.7 | 12.4 |
请回答下列问题:
(1)镁在元素周期表中的位置_______________;
(2)向溶液Ⅱ中加入试剂X是_____________,作用是_________________________;
(3)流程中不加H2O2引起的后果是___________________________________;
(4)说出母液的一种用途___________________;
(5)加入H2O2溶液发生反应的离子方程式是___________________;
Ⅱ.海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
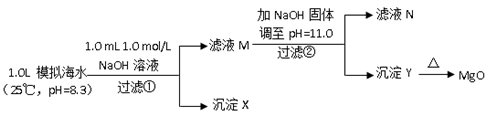
| 模拟海水中的离子浓度/ (mol/L) | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp [Ca(OH)2]=4.68×10-6;Ksp [Mg(OH)2]=5.61×10-12。请回答下列问题:
(6)沉淀物X为_____________;
(7)滤液N中Ca2+浓度为_______________;
(8)加NaO H固体调整pH=12.5是否可行______(填“是”“否”);原因是________。
H固体调整pH=12.5是否可行______(填“是”“否”);原因是________。
-
高纯度氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如图所示:
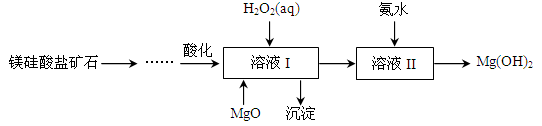
已知:①溶液I中除含Mg2+、SO42-外,还含少量Fe3+、Al3+、Fe2+等离子;
②Mg2+与氨水的反应为吸热反应。请回答下列问题:
(1)Mg在元素周期表中的位置为__________________。
(2)H2O2的电子式为________。溶液I中加入H2O2溶液发生反应的离子方程式是__________。
(3)向溶液I中首先加入的试剂是___________,产生沉淀的化学式为_________________。工业上有时只用一种含钠化合物替代H2O2和MgO,该试剂通常为___________(填化学式)。
(4)溶液II中Mg2+转化率随温度T的变化情况如图所示:

①向溶液II中加入氨水发生反应的离子方程式是______________________。
②T1前Mg2+转化率增大的原因是_________________;
-
氢氧化镁是已知用途广泛、极具开发前景的环保材料,广泛应用在阻燃、废水中和、烟气脱硫等方面。镁硅酸盐矿石[主要成分Mg3Si2O5(OH)4,含氧化铝、氧化铁、氧化亚铁等杂质]可用于生产氢氧化镁,简要工艺流程如下:
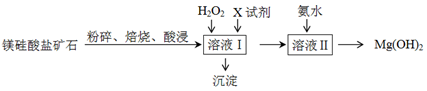
已知:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
| Fe3+ | Al3+ | Fe2+ | Mg2+ |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)对矿石焙烧的目的是_______________________。
(2)加入H2O2溶液反应的离子方程式是___________________。
(3)向溶液Ⅰ中加入的X可以是______________,作用是______________。
(4)加入氨水时,Mg2+转化率随温度t的变化如图所示:
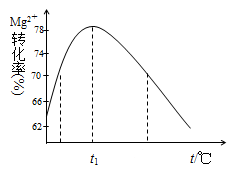
①溶液Ⅱ中发生反应的离子方程式是__________________。
②t1前Mg2+转化率增大的原因是__________________;t1后Mg2+转化率下降的原因是(用化学方程式表示)______________。
-
碳酸锂广泛应用于陶瓷和医药等领域。已 -锂辉石(主要成分为Li2O
-锂辉石(主要成分为Li2O Al2O3
Al2O3 4SiO2)为原材料制备Li2CO3的工艺流程如下:
4SiO2)为原材料制备Li2CO3的工艺流程如下:

已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和12.4;Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.7g和1.3g。
(1)步骤Ⅰ前,B-锂辉石要粉碎成细颗粒的目的是_____________.
(2)步骤Ⅰ中,酸浸后得到的酸性溶液中含有Li+、SO42-,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入_____________(填“石灰石”、“氯化钙”或“稀硫酸”)以调节溶液的pH到6.0~6.5,沉淀部分杂质离子,然后分离得到浸出液。
-
(19分)FeSO4·7H2O广泛用于医药和工业领域,实验室制备FeSO4·7H2O的流程如下:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是_________。
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;②_____________________。
(3)FeSO4·7H2O是某些补血剂的主要成分,实验室用KMnO4溶液通过氧化还原滴定测定某补血剂(1.500 g)中铁元素的含量。
①配制100 mL 1.200 × 10 —2 mol·L—1的KMnO4溶液时,将溶解后的溶液转移至容量瓶中的操作方法是__________________________;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是_________________。
a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
KMnO4溶液应盛装在__________滴定管中。滴定到终点时的现象为_____________________。滴定完毕,三次实验记录KMnO4标准溶液的读数如下。
| 滴定次数实验数据 | 1 | 2 | 3 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 |
| V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
| V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
该补血剂中铁元素的质量分数为_____________________。
(4)某实验小组用久置的FeSO4溶液和NaOH溶液制备Fe(OH)2,实验后没有得到预期的白色沉淀,于是采用下列试剂(已煮沸除氧)和装置进行实验:
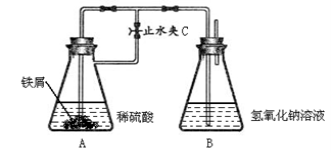
实验开始打开止水夹C,目的是_______________________。一段时间后,关闭止水夹C, B中观察到的现象是______________________。B中发生反应的离子方程式是___________________。
-
FeSO4·7H2O广泛用于医药和工业领域,实验室制备FeSO4·7H2O的流程如下:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是_________。
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;②_____________________。
(3)FeSO4·7H2O是某些补血剂的主要成分,将1.5 g某补血剂预处理,配成100mL溶液。实验室用KMnO4溶液通过氧化还原滴定测定该补血剂(1.5 g)中铁元素的含量,①配制100 mL 1.200 × 10 —2 mol·L—1的KMnO4溶液时,将溶解后的溶液转移至容量瓶中的操作方法是__________________________;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是_________________。
a. 稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
KMnO4溶液应盛装在__________滴定管中。滴定到终点时的现象为____________。
③滴定完毕,三次实验记录KMnO4标准溶液的读数如下。
| 滴定次数实验数据 | 1 | 2 | 3 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 |
| V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
| V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
该补血剂中铁元素的质量分数为_____________________。
-
铋(Bi)及其化合物广泛应用于电子、医药等领域。一种以含铋矿石辉铋矿(主要成分为Bi2S3,含少量杂质PbO2等)为原料,采用湿法冶金制备铋单质的工艺流程如下:
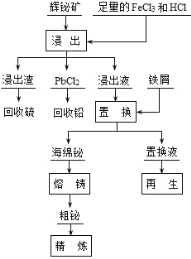
已知:PbCl2是一种难溶于冷水,易溶于热水的白色固体。 回答下列问题:
(1)铋(Bi)位于ⅤA族,铋的氢化物的热稳定性______氨气(填“大于”或“小于”)。
(2)“浸出”时,为了提高浸出速率,可采用的措施有______(任写一条)
(3)加热浸出时,PbO2 生成 PbCl2 和一种气体,此反应的化学方程式为______, 从产物中分离回收 PbCl2 的步骤是______、洗涤、干燥。从保护环境和原料循环利 用的角度,请指出上述工艺流程中可以采取的措施为______。
(4)电解精炼粗铋时必须补充含 Bi3+浓度高的电解液。可用粗铋、铅条作为两个电极,铅条外用素烧 的陶瓷坩埚作隔膜(Bi3+不能透过,H+能透过),电解液开始时为盐酸和食盐的混合液。则粗铋为电解池的 ______极,电解总反应为______。
(5)25℃时,向浓度均为 0.02mol·L-1 的 Cu2+、Bi3+的混合溶液中滴加 Na2S 溶液(设溶液体积增加 1倍),使 Cu2+恰好沉淀完全即溶液中 c(Cu2+)=1×10-5 mol·L-1,此时是否有 Bi2S3 沉淀生成______(列式计算说明)。(已知:25℃时,Ksp(CuS)=6.0×10-36、Ksp(Bi2S3)=1.8×10-99)