-
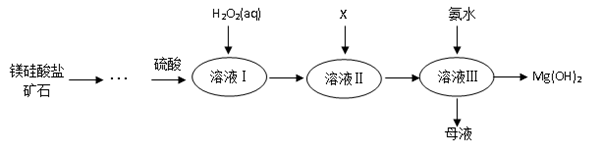
Ⅰ.高纯度氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如图所示:
已知:
①溶液Ⅰ中除含Mg2+、SO42‒外,还含有少量Fe3+、Al3+、Fe2+等离子;
②常温下,几种金属离子开始沉淀和沉淀完全时的pH如下表所示:
| 金属离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ |
| 开始沉淀时的pH | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时的pH | 3.7 | 5.2 | 9.7 | 12.4 |
请回答下列问题:
(1)镁在元素周期表中的位置_______________;
(2)向溶液Ⅱ中加入试剂X是_____________,作用是_________________________;
(3)流程中不加H2O2引起的后果是___________________________________;
(4)说出母液的一种用途___________________;
(5)加入H2O2溶液发生反应的离子方程式是___________________;
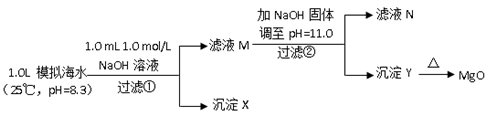
Ⅱ.海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
| 模拟海水中的离子浓度/ (mol/L) | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp [Ca(OH)2]=4.68×10-6;Ksp [Mg(OH)2]=5.61×10-12。请回答下列问题:
(6)沉淀物X为_____________;
(7)滤液N中Ca2+浓度为_______________;
(8)加NaO H固体调整pH=12.5是否可行______(填“是”“否”);原因是________。
H固体调整pH=12.5是否可行______(填“是”“否”);原因是________。
-
高纯度氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如图所示:
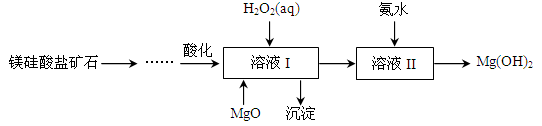
已知:①溶液I中除含Mg2+、SO42-外,还含少量Fe3+、Al3+、Fe2+等离子;
②Mg2+与氨水的反应为吸热反应。请回答下列问题:
(1)Mg在元素周期表中的位置为__________________。
(2)H2O2的电子式为________。溶液I中加入H2O2溶液发生反应的离子方程式是__________。
(3)向溶液I中首先加入的试剂是___________,产生沉淀的化学式为_________________。工业上有时只用一种含钠化合物替代H2O2和MgO,该试剂通常为___________(填化学式)。
(4)溶液II中Mg2+转化率随温度T的变化情况如图所示:

①向溶液II中加入氨水发生反应的离子方程式是______________________。
②T1前Mg2+转化率增大的原因是_________________;
-
高纯度的氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如图所示。
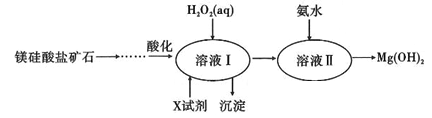
已知:①溶液I中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子;
②几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
| Fe3+ | A13+ | Fe2+ | Mg2+ |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)镁硅酸盐矿石中有一种俗称茧青石,化学式为Mg2Al4Si5018,它的氧化物形式为________。
(2)如何检验溶液I中的Fe2+?____________。
(3)向溶液I中加入X试剂的作用是________,加入的两种试剂的先后顺序是_______(填化学式)。
(4)从溶液I中得到沉淀的合理pH为________(填序号)。
A. 3.3 B. 3.7 C. 5.8 D.9.5
(5)加入H2O2溶液反应的离子方程式是__________。
(6)如图是溶液II充分反应时,Mg2+的转化率随温度T的变化示意图。
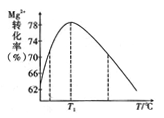
①向溶液II中加入氨水反应的离子方程式是____________。
②T1前Mg2+转化率增大的原因是___________; T1后Mg2+转化率下降的原因是__________(用化学方程式和文字表示)。
-
高纯度的氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如下:

已知1:溶液Ⅰ中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子
2:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
| Fe3+ | Al3+ | Fe2+ | Mg2+ |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)向溶液Ⅰ中加入X的作用是____________。
(2)向溶液Ⅰ中加入的两种试剂先后顺序是______________(填化学式)。
(3)加入H2O2溶液反应的离子方程式是__________________。
(4)下图是Mg2+转化率随温度t的变化示意图:
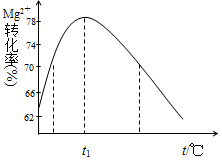
① t1前Mg2+转化率增大的原因是____________;t1后Mg2+转化率下降的原因是(用化学方程式表示)______________。
② 向溶液Ⅱ中加入氨水反应的离子方程式是_________。
-
高纯度的氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢
氧化镁,简要工艺流程如下:

己知1:溶液I中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子
2:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
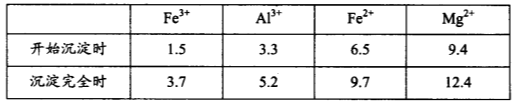
(1)Mg在周期表中的位置________________,Si的原子结构示意图为______________。
(2)向溶液I中加入X的作用是________________________________。
(3)向溶液I中加入的两种试剂先后顺序是__________________(填化学式)。
(4)加入H2O2溶液反应的离子方程式是______________________。
(5)下图是溶液Ⅱ中Mg2+转化率随温度t的变化示意图:
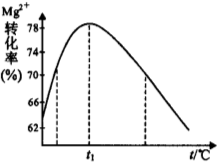
①向溶液Ⅱ中加入氨水反应的离子方程式是________________。
②t1前Mg2+转化率增大的原因是______________;t1后Mg2+转化率下降的原因是(用化学方程式表示)_____________________。
-
氢氧化镁是已知用途广泛、极具开发前景的环保材料,广泛应用在阻燃、废水中和、烟气脱硫等方面。镁硅酸盐矿石[主要成分Mg3Si2O5(OH)4,含氧化铝、氧化铁、氧化亚铁等杂质]可用于生产氢氧化镁,简要工艺流程如下:
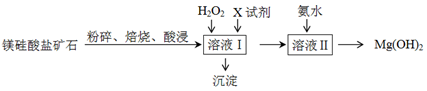
已知:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
| Fe3+ | Al3+ | Fe2+ | Mg2+ |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)对矿石焙烧的目的是_______________________。
(2)加入H2O2溶液反应的离子方程式是___________________。
(3)向溶液Ⅰ中加入的X可以是______________,作用是______________。
(4)加入氨水时,Mg2+转化率随温度t的变化如图所示:
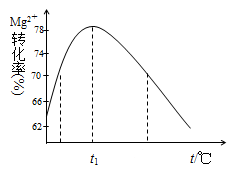
①溶液Ⅱ中发生反应的离子方程式是__________________。
②t1前Mg2+转化率增大的原因是__________________;t1后Mg2+转化率下降的原因是(用化学方程式表示)______________。
-
FeSO4·7H2O广泛用于医药和工业领域。
(1)下面是以工业废铁屑为原料生产FeSO4·7H2O的流程图。

请填写下列空白。
①加适量碳酸钠溶液的目的是______________,反应I需要加热数分钟,其原因是___________。
②判断反应Ⅱ完成的现象是__________。反应Ⅱ需要100mL1mol/L的稀硫酸,用98.3%,ρ=1.84g/cm3的浓硫酸配制。所用的仪器有量筒、烧杯、玻璃棒、胶头滴管及____________.
③测定FeSO4·7H2O产品中Fe2+含量的方法是用KMnO4溶液滴定法(5Fe2++ +8H+=5Fe3++Mn2++4H2O),步骤为:
+8H+=5Fe3++Mn2++4H2O),步骤为:
Ⅰ.称取2.8500g FeSO4·7H2O产品,配制成250mL溶液;
Ⅱ.量取25.00mL待测溶液于锥形瓶中;
Ⅲ.用硫酸酸化的0.01000moL/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。

某同学设计如图所示的滴定方式中,最合理的是____________(夹持部分略去)(填字母序号);判断此滴定实验达到终点的方法是____________;计算上述样品中FeSO4·7H2O的质量分数为________(用小数表示,保留三位小数);若用上述方法测定的样品中FeSO4·7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有_____________;______________。
(2)已知FeSO4·7H2O晶体在加热条件下发生如下反应:2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。
Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。

请填写下列空白。
①仪器的连接顺序为a接________、__________接_________、________接__________、__________接_____________。
②装置C中的X为______________;该装置中冷水的作用是_________________。
-
锑(Sb)广泛用于生产各种阻燃剂、陶瓷、半导体元件、医药及化工等领域。以辉锑矿为原料制备金属锑,其一种工艺流程如下:
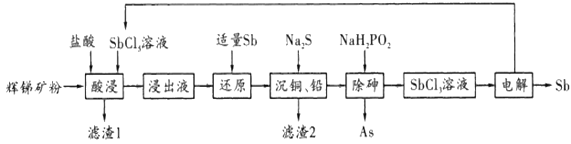
已知部分信息如下:
I.辉锑矿(主要成分为Sb2S3,还含有As2S5、PbS、CuO和SiO2等);
Ⅱ.浸出液主要含盐酸和SbCl3,还含SbCl2、CuCl2、AsCl3和PbCl2等杂质;
Ⅲ.常温下,Ksp(CuS)=1.0×10-36,Ksp(PbS)=9.0×10-29。
回答下列问题:
(1)NaH2PO2中P的化合价为___________。
(2)“酸浸”过程中SbCl3和Sb2S3反应有S生成,该反应的还原产物是___________(填化学式)。
(3)写出“还原”反应的化学方程式:_________________________________。
(4)已知:浸出液中C(Cu2+)=0.01mo/L、C(Pb2+)=0.1mo/L。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是______________________(填化学式);当CuS、PbS共沉时, ___________。
___________。
(5)在“除砷”过程中,氧化产物为H3PO4。该反应中氧化剂还原剂的物质的量之比为_______。常温下,SbCl2溶液的pH<7,用离子方程式表示其原因:_____________________。
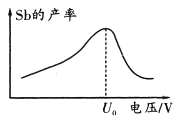
(6)在“电解”过程中,以惰性材料为电极,阴极的电极反应式为______________________;“电解”中锑的产率与电压大小关系如图所示。当电压超过U0V时,锑的产率降低的原因可能是______________________。
-
氟化钾是一种重要的无机氟化工产品,广泛应用于医药、农药和金属冶炼等领域。采用湿法磷酸副产物氟硅酸( ,含有少量
,含有少量 、
、 等)制备氟化钾的工艺流程如图所示(已知:
等)制备氟化钾的工艺流程如图所示(已知: ):
):
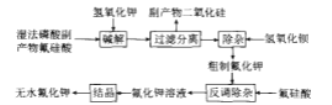
请回答下列问题:
(1)碱解过程主要反应的化学方程式为_____,其中要严格控制KOH用量,否则易生成副产物_____(填化学式)溶解在滤液中。
(2)碱解反应中温度对氟化钾收率的影响如图所示。由如图可知,实验选择适宜的反应温度为____;最高点后,随温度升高曲线下降的原因可能是_______。
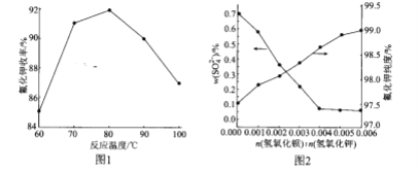
(3)Ba(OH)2加入量对 含量和氟化钾纯度的影响如图所示。当
含量和氟化钾纯度的影响如图所示。当 由0.004到0.005时,氟化钾的纯度升高,这是由于__。
由0.004到0.005时,氟化钾的纯度升高,这是由于__。
(4)Ba(OH)2和BaCO3是常见的除硫试剂。若使用BaCO3代替Ba(OH)2,当沉淀转化达到平衡时,滤液中 ___[已知
___[已知 ,
, ,保留小数点后三位]。
,保留小数点后三位]。
(5)浓度均为0.1mol/L的KF和HF的混合溶液中:2c(H+)-2c(OH-)____c(F-)-c(HF) (填“>”“<”或“=”)。
(6)1986年,化学家Karl Chrite用KMnO4和KF、HF混合溶液反应生成稳定配离子 ,该反应氧化产物是一种常见的无色无味气体单质,则该反应的离子方程式为_____。
,该反应氧化产物是一种常见的无色无味气体单质,则该反应的离子方程式为_____。
-
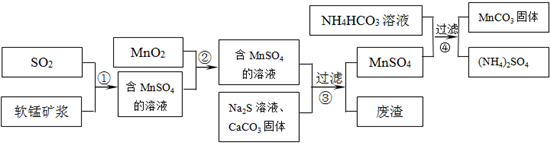
碳酸锰(MnCO3)是理想的高性能强磁性材料,也是制备Mn2O3、MnO2等锰的氧化物的重要原料,广泛用于电子、化工、医药等行业.一种制备MnCO3的生产流程如图所示.
已知生成氢氧化物的pH和有关硫化物的Ksp如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 |
| 物质 | MnS | CuS | PbS |
| Ksp | 2.5×10-13 | 6.3×10-36 | 8.0×10-28 |
软锰矿主要成分为MnO2,其中含有铁、铝、硅的氧化物和少量重金属化合物杂质,SO2来自工业废气.流程①中主要发生的反应有:MnO2+SO2=MnSO4 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
(1)流程①中所得MnSO4溶液的pH比软锰矿浆的pH______(填“大”或“小”),该流程可与______(填工业生产名称)联合,生产效益更高.
(2)反应②的目的是将溶液中的Fe2+氧化成Fe3+,其离子反应方程式为______,这样设计的目的和原理是______
(3)反应③中硫化钠的作用是使重金属离子转化为硫化物沉淀,碳酸钙的作用是______.
(4)反应④发生的化学反应为:MnSO4+2NH4HCO3=MnCO3↓+(NH4)2SO4+CO2↑+H2O.
反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4.加入稍过量的NH4HCO3的目的是______,溶液的pH不能过低的原因是______.
(5)软锰矿中锰的浸出有两种工艺:
工艺A:软锰矿浆与含SO2的工业废气反应 工艺B:软锰矿与煤炭粉混合,焙烧后加稀硫酸溶解.
其中工艺A的优点是______.(答对1个即可)


H固体调整pH=12.5是否可行______(填“是”“否”);原因是________。


















