-
(13分)按要求完成下列各小题。
(1)用CO2来生产燃料甲醇的反应原理:CO2(g)+3H2(g) CH3OH(g)+H2O(g),某些化学键的键能数据如下表:
CH3OH(g)+H2O(g),某些化学键的键能数据如下表:
| 化学键 | C-C | C-H | H-H | C-O | C=O | H-O |
| 键能/kJ·mol-1 | 348 | 413 | 436 | 358 | 750 | 463 |
计算反应上述反应的焓变△H=_______________________
写出上述反应的平衡常数表达式K=__________________,若升高温度,则平衡常数K________(填“增大”或“减小”或“不变”)。该反应的△S______0(填“>”或“<”或“=”),在 _________(填“较高”或“较低”)温度下有利于该反应自发进行。
(2)在25℃下,向浓度均为0.01 mol・L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为________________。
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34。)
(3)某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH=11。在此温度下,将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液为中性,则Va︰Vb= 。
(4)在25℃时,将cmol·L-1的醋酸溶液与0.02mol·L-1NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=____________________。
-
(15分)倡导“低碳经济”。降低大气中CO2的含量,有利于解决气候变暖的环境问题。
(1)工业上可用CO2来生产燃料甲醇。反应原理为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0.
CH3OH(g)+H2O(g) △H<0.
一定温度下,在体积为2L的恒容密闭容器中,充入2molCO2和6molH2.一定条件下发生反应:测得CO2和CH3OH的浓度随时间变化如图所示。
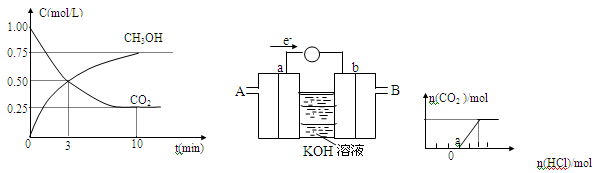
①达到平衡时,CO2的转化率= 。
②从反应开始到平衡。氢气的平均反应速率V(H2)= mol/(L·min)。
③容器内的平衡压强与起始压强之比为 。
④保持容器容积不变,下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来 D.再充入1molCO2和3molH2
⑤某同学依据甲醇燃烧的反应原理,设计如上图所示的电池装置,a、b均为惰性电极。使用时,空气从 口通入(填“A”或“B”):a极的电极反应式为 。
(2)将一定量的CO2气体通入NaOH溶液中,再向所得溶液中逐滴加入盐酸,边加边振荡至过量,产生的气体与HCl物质的量关系如上图所示(忽略气体的溶解和HCl的挥发)。请回答:O点溶液中溶质的化学式 ,a点溶液中各离子浓度由大到小的顺序是 。
-
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是,下列说法正确的是( )
①CH3OH(g)+H2O(l)=CO2(g)+3H2(g);△H=+93.0kJ•mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g);△H=-192.9kJ•mol-1.
O2(g)=CO2(g)+2H2(g);△H=-192.9kJ•mol-1.
A.CH3OH的燃烧热为192.9kJ•mol-1
B.CH3OH的燃烧热为764.7kJ•mol-1
C.CH3OH的燃烧热为392.7kJ•mol-1
D.不能算出其燃烧热
-
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种反应原理如下:CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1
下列说法正确的是( )
A.1 L CH3OH蒸汽与1 L水蒸气反应生成1 L CO2气体与3 L氢气吸收热量49.0 kJ
B.1个CH3OH分子与1个水分子反应生成1个CO2分子与3个H2分子吸收49.0 kJ热量
C.相同条件下1 mol CH3OH(g)与1 mol H2O(g)的能量总和小于1 mol CO2(g)与3 mol H2(g)的能量总和
D.1 mol CH3OH蒸汽与1 mol液态水反应生成1 mol CO2气体与3 mol氢气吸收的热量小于49.0 kJ
-
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种反应原理如下:
CH3OH(g) + H2O(g) → CO2(g) + 3H2(g) – 49.0 kJ
下列说法正确的是
A.1 LCH3OH蒸汽与1 L水蒸汽反应生成1 L CO2气体与3 L 氢气吸收热量49.0 kJ
B.1个CH3OH分子与1个水分子反应生成1个CO2分子与3个H2分子吸收49.0 kJ热量
C.相同条件下1molCH3OH(g)与1mol H2O(g)的能量总和小于1molCO2(g)与3 mol H2(g)的能量总和
D.1 molCH3OH蒸汽与1 mol液态水反应生成1mol CO2气体与3 mol 氢气吸收的热量小于49.0 kJ
-
.甲醇质子交换膜燃料电池中,将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+ H2O(g)=CO2 (g) + 3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+ 0.5O2 (g)=CO2 (g) + 2H2(g) △H=-192.9kJ/mol
下列说法正确的是
A.CH3OH的燃烧热是192.9kJ/mol
B.CH3OH转变成H2的过程一定要吸收能量
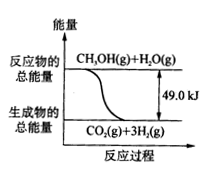
C.反应①中的能量变化如右图所示
D.根据反应①和②可推知:
2H2(g)+O2 (g)=2H2O (g) △H=-483.8kJ/mol
-
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g) → CO2(g)+3H2(g)-49.0 kJ
②CH3OH(g)+1/2O2(g)→ CO2(g)+2H2(g)+192.9 kJ
下列说法正确的是
A.1molCH3OH完全燃烧放出热量192.9 kJ
B.②中的能量变化如图所示,则Q=E3-E1

C.H2燃烧能放出大量的热,故CH3OH转变成
H2的过程必须吸收热量
D.根据②推知:在25 ℃,101 kPa时,1 mol
CH3OH(g)完全燃烧生成CO2和H2O放出的热量应大于192.9 kJ
-
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H=+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9 kJ/mol
下列说法错误的是
A.1mol CH3OH(g)完全燃烧放出的热量大于192.9 kJ
B. 根据反应①和②推知反应: H2(g)+1/2O2(g)=H2O(g)的△H=-241.9kJ/mol
C.CH3OH转变成H2的过程不一定要吸收能量
D. 反应①中的能量变化如图所示

-
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
 ①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ·mol-1
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9kJ·mol-1

下列说法正确的是
A.CH3OH的燃烧热为192.9kJ·mol-1
B.反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H>—192.9kJ·mol-1
-
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g);ΔH=+49.0 kJ/mol
②CH3OH(g)+O2(g)===CO2(g)+2H2(g);ΔH=-192.9 kJ/mol
下列说法正确的是
A.CH3OH的燃烧热为192.9 kJ/mol
B.反应①中的能量变化如下图所示

C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应CH3OH(l)+O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ/mol
CH3OH(g)+H2O(g),某些化学键的键能数据如下表:




 ①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ·mol-1
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ·mol-1
