-
化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)催化反硝化法中,H2能将NO3-还原为N2。25℃时,反应进行10min,溶液的pH由7变为12。
①N2的结构式为________。
②上述反应的离子方程式为________,其平均反应速率υ(NO3-)为 ________mol·L-1min-1。
③还原过程中可生成中间产物NO2-,写出3种促进NO2-水解的方法________。
(2)电化学降解NO3-的原理如图所示。
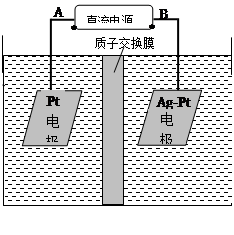
①电源正极为________(填A或B),阴极反应式为________。
②若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为________g。
-
化学在环境保护中起着十分重要的作用。催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)催化反硝化法中,H2能将NO3-还原为N2。25℃时,反应进行10 min,溶液的pH由7变为12。
①N2的结构式为________。
②上述反应离子方程式为____________________,其平均反应速率v(NO3-)为________mol·L-1·min-1。
③还原过程中可生成中间产物NO2-,写出3种促进NO2-水解的方法________。
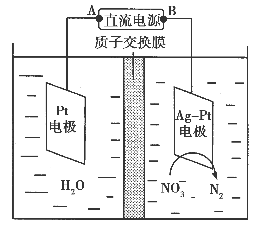
(2)电化学降解NO3-的原理如图所示。
①电源正极为________(填“A”或“B”),阴极反应式为______________。
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为________g。
-
化学在环境保护中起着十分重要的作用。催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)催化反硝化法中,H2能将NO3-还原为N2。25℃时,反应进行l0 min,溶液的pH由7变为l 2。
①N2的结构式为
②上述反应的离子方程式为 ,其平均反应速率v(NO3-)为 mol·L-1·min-1。
③还原过程中可生成中间产物NO2-,写出2种促进NO2-水解的方法 。
(2)电化学降解NO3-的原理如下图所示。

①电源正极为 (填“A”或“B”),阴极反应式为:
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为 g。
-
根据有关信息,写出符合要求的离子方程式
(1)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染。催化反硝化法中,H2能将NO 还原为N2。
还原为N2。
上述反应的离子方程式为______________________________________。
(2)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为_______________________________________________。
(3)某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等,正极材料可再生利用,其中一步工艺流程为用氢氧化钠溶液进行“正极碱浸”,发生反应的离子方程式____________________________。
(4)Fe的一种含氧酸根FeO 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是________________________________________________________________。
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是________________________________________________________________。
(5)向菱镁矿(主要成分为MgCO3,含少量FeCO3)中,首先加入稀硫酸,过滤后,再加入H2O2。
①MgCO3与稀硫酸反应的离子方程式为__________________________。
②加入H2O2氧化时,发生反应的化学方程式为_________________。
③硫与热的NaOH溶液反应,产物中元素的最高价态为+4价,写出该反应的离方程式__________________________________________________。
-
化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO3-的原理图所示。下列说法不正确的是:
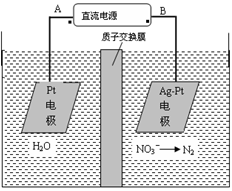
A.A为电源正极
B.阳极反应式为:2H2O-4e-=4H++O2↑
C.若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为10.4克
D.阴极反应式为:2NO3-+6H2O+10e-=N2↑+12OH-
-
电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO3-的原理如图所示,下列说法不正确的是( )
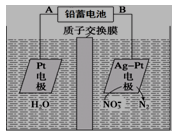
A.铅蓄电池的A极为正极,电极材料为PbO2
B.该电解池的阴极反应式为:2NO3- + 12H+ + 10e- = N2↑ + 6H2O
C.该电解池的总反应方程式为:2H2O + 4NO3-  2N2↑+ 5O2↑ + 4OH-
2N2↑+ 5O2↑ + 4OH-
D.若电解过程中转移2mol电子,则交换膜右侧电解液的质量减少5.6g
-
电化学降解法可用于治理水中硝酸盐的污染,电化学降解NO3-的原理如图所示,下列说法正确的是
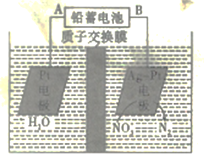
A.电源正极为B
B.H+由右侧通过交换膜移动到左侧
C.该电解池的阴极反应式为2NO3-+12H+ +10e-=N2↑+6H2O
D.标况下,若有2. 24LN2生成,理论上铅蓄电池中有20.7克Pb消耗
-
电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO的原理如图所示,下列说法不正确的是
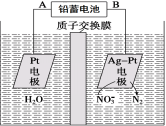
A.铅蓄电池的A极为正极,电极材料为PbO2
B.该电解池的总反应方程式为:2H2O + 4NO3-  2N2↑+ 5O2↑ + 4OH-
2N2↑+ 5O2↑ + 4OH-
C.该电解池的阴极反应式为:2NO3- + 12H+ + 10e- = N2↑ + 6H2O
D.若电解过程中转移2mol电子,则交换膜右侧电解液的质量减少5.6g
-
电化学降解法可用于治理水中硝酸盐的污染。降解NO3—的原理如图所示。下列说法不正确的是( )
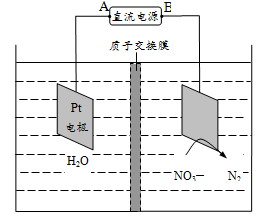
A.直流电源A为正极、B为负极
B.电解过程中质子从Pt电极向Ag-Pt电极移动
C.在阴极发生的电极反应:2NO3+10e-+12H+=N2↑+ 6H2O
D.当电解过程转移2mol电子时,阴极室质量减少5.6g
-
催化反硝化法可治理水中硝酸盐的污染,该方法是用H2将NO3-还原为N2,反应的化学方程式为:5H2+ 2 NO3- xOH-+ N2+4H2O。下列有关说法正确的是
xOH-+ N2+4H2O。下列有关说法正确的是
A.该反应为置换反应
B.每生成1mol N2,反应转移5mole-
C.x=2
D.反应过程中溶液pH减小







