-
已知NO2和N2O4可以相互转化:2NO2(g)⇌N2O4(g)(正反应为放热反应).现将一定量NO2 和N2O4 的混合气体通入一体积为1L的恒温密闭容器中,反应物的浓度随时间变化的关系曲线如图所示.请回答下列问题:
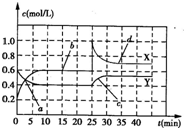
(1)图中共有两条曲线X和Y,其中曲线________表示NO2 浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是________.
(2)前10min内用NO2 表示的化学反应速率v(NO2 )=________mol/-1;反应进行至25min时,曲线发生变化的原因是________.
(3)若要达到与最后的平衡状态相同的化学平衡状态,在25min时还可以采取的措施是________(填序号)
①加入催化剂 ②缩小容器体积 ③升高温度 ④加入一定量的N2O4.
-
已知NO2和N2O4可以相互转化:2NO2(g)  N2O4(g)(正反应为放热反应)。现将一定
N2O4(g)(正反应为放热反应)。现将一定
量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示,回答下列问题:
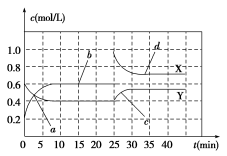
(1)图中共有两条曲线X和Y,其中曲线________表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是________。
(2)前10 min内用NO2表示的化学反应速率v(NO2)=________mol/(L·min);反应进行至25 min时,曲线发生变化的原因是________。
(3)若要达到与最后相同的化学平衡状态,在25 min时还可以采取的措施是________。
A.加入催化剂 B.缩小容器体积
C.升高温度 D.加入一定量的N2O4
-
已知NO2和N2O4可以相互转化:2NO2(g)
 N2O4(g);Q>0现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
N2O4(g);Q>0现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
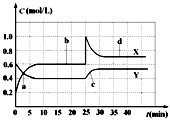
A.图中共有两条曲线X和Y,其中曲线y表示NO2浓度随时间的变化
B.a、b、c、d四个点中,表示化学反应处于平衡状态的点是b和c
C.反应进行至25min时,曲线发生变化的原因是加入0.4molN2O4
D.若要达到与d相同的状态,在25min时还能采取的措施是适当缩小容器体积
-
已知NO2和N2O4可以相互转化:2NO2  N2O4 △H<0。现将一定量NO2和N2O4的混合气体通入一体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。下列有说法正确的是
N2O4 △H<0。现将一定量NO2和N2O4的混合气体通入一体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。下列有说法正确的是
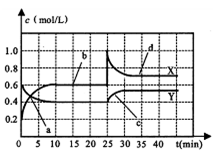
A.曲线Y表示NO2浓度随时间的变化
B.a点表示化学反应处于平衡状态
C.c点表示v生成(NO2)< v消耗(NO2)
D.25min时,曲线发生变化的原因是缩小了容器的体积
-
NO2和N2O4可相互转化:2NO2(g) N2O4(g) ΔH<0现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法中正确的是( )
N2O4(g) ΔH<0现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法中正确的是( )
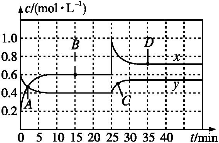
A.图中共有两条曲线x和y,其中曲线y表示NO2浓度随时间的变化
B.A、B、C、D四个点中,表示化学反应处于平衡状态的点是B和C
C.反应进行至25 min时,曲线发生变化的原因是加入0.4 mol N2O4
D.若要达到与D相同的状态,在25 min时还可采取的措施是适当缩小容器体积
-
NO2和N2O4可相互转化:2NO2(g)  N2O4(g) ΔH<0现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法中正确的是
N2O4(g) ΔH<0现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法中正确的是
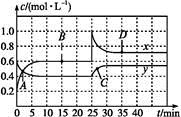
A.图中共有两条曲线x和y,其中曲线y表示NO2浓度随时间的变化
B.A、B、C、D四个点中,表示化学反应处于平衡状态的点是B和C
C.反应进行至25 min时,曲线发生变化的原因是加入0.4 mol N2O4
D.若要达到与D相同的状态,在25 min时还可采取的措施是适当缩小容器体积
-
已知NO2与N2O4 可相互转化: 2NO2( g) N2O4(g) △H=−24.2 kJ• mol−1,在恒温下, 将一定量和N2O4的混合气体充入体积为2 L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析不合理的是
N2O4(g) △H=−24.2 kJ• mol−1,在恒温下, 将一定量和N2O4的混合气体充入体积为2 L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析不合理的是
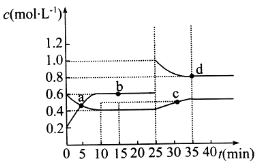
A.前10 min内,用v(NO2)表示的反应速率为0. 02 mol•L−1•min−1
B.反应进行到10 min时,体系吸收的热量为9.68 kJ
C.b、d两点中v(正)与v(逆)均相等
D.25 min时,正反应速率增大
-
已知NO2与N2O4相互转化:2NO2(g) N2O4(g);△H=-24.2kJ/mol在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如右图。下列推理分析合理的是( )
N2O4(g);△H=-24.2kJ/mol在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如右图。下列推理分析合理的是( )
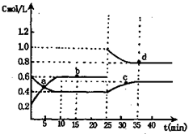
A.a,b,c,d四点中c正与v逆均相等
B.反应进行到10min时,体系吸收的热量为9.68kJ
C.前10min内,用v(NO2)表示的该反应速率为0.02mol/L·min
D.25min时,导致平衡移动的原因是升温
-
已知NO2与N2O4相互转化:2NO2(g) N2O4(g);△H=-24.4kJ/mol在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的量浓度随时间变化的关系如下图。下列推理分析合理的是( )
N2O4(g);△H=-24.4kJ/mol在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的量浓度随时间变化的关系如下图。下列推理分析合理的是( )
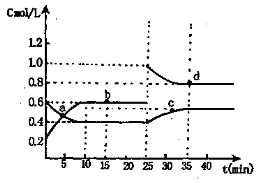
A.前10min内,用v(NO2)表示的该反应速率为0.02mol/(L·min)
B.反应进行到10min时,体系吸收的热量为9.76kJ
C.a,b,c,d四点中v正与v逆均相等
D.25min时,导致平衡移动的原因是升温
-
已知2NO2(红棕色) N2O4(无色)可以同时相互转化,
N2O4(无色)可以同时相互转化,
①在密封有NO2的玻璃瓶中,升高温度,颜色加深,问NO2转化为N2O4是一个 热反应。
②在一个恒温恒压容器中,通入稀有气体。颜色 ,平衡 移动。
③在一个密闭恒容体系中,增大NO2的量,会引起NO2转化率 ,颜色 ,再通入稀有气体增大压强,平衡 移动,颜色 。
N2O4(g)(正反应为放热反应)。现将一定








