-
(14分)茶是我国人民喜爱的饮品。某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有钙、铁、铝三种金属元素。
[查阅部分资料]:草酸铵[(NH4)2C2O4]属于弱电解质;草酸钙(CaC2O4)难溶于水;Ca2+、A13+、Fe3+完全沉淀的pH:Ca(OH)2:pH≥13;A1(OH)3:pH≥5.5;Fe(OH)3:pH≥4.1。
试根据上述过程及信息填空:
(1)步骤②加盐酸的作用是 _________________________________________ ;
(2)写出检验Ca2+的离子方程式 ___________________________;
(3)写出沉淀C所含主要物质的化学式 _____________________________;
(4)写出步骤⑧用A试剂生成红色溶液的离子方程式_____________________________;
(5)步骤⑨的作用是 ________;
(6)猜测步骤⑩的目的是 _________________________________ ;
(7)已知:2Fe (s)+ 3/2O2 (g)= Fe2O3(s),△H = — Q1 kJ·mol-1
2Al(s) + 3/2O2 (g)= Al 2O3(s),△H = — Q2 kJ·mol-1
则Q1 ___________Q2 (填“>”, “<”或“=”)

-
(14分)茶是我国人民喜爱的饮品。某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有Ca、A1、Fe三种元素。
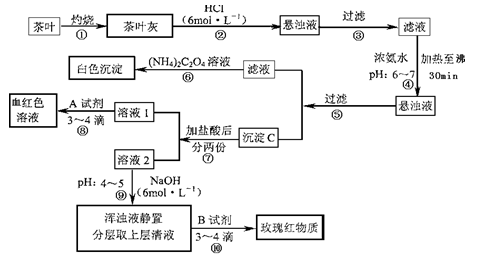
【资料查询】:草酸铵[(NH4)2C2O4]属于弱电解质。草酸钙(CaC2O4)难溶于水。Ca2+、
A13+、Fe3+完全沉淀的pH:Ca(OH)2:pH≥13;A1(OH)3:pH≥5.5;Fe(OH)3:pH≥4.1。
试根据上述过程及信息填空:
(1)步骤②加盐酸的作用是________。
(2)步骤③操作中用到的玻璃仪器有________。
(3)写出步骤⑥中检验Ca2+存在的离子方程式________。
(4)写出沉淀C所含主要物质的化学式。
(5)写出步骤⑧中选用A试剂的化学式________。
(6)步骤⑨的作用是________,
猜测步骤⑩的目的是________。
-
茶是我国人民喜爱的饮品。我市某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有Ca、Al、Fe三种元素。
【查阅部分资料】草酸铵[(NH4)2C2O4]属于弱电解质。草酸钙(CaC2O4)难溶于水。Ca2+、Al3+、Fe3+完全沉淀的pH为Ca(OH)2:pH≥13;Al(OH)3:pH≥5.5;Fe(OH)3:pH≥4.1。

请根据上述过程及信息填空:
(1)步骤②加盐酸的作用是 。
(2)写出检验Ca2+的离子方程式 。
(3)写出沉淀C所含主要物质的化学式 。
(4)写出步骤⑧用A试剂生成红色溶液的离子方程式 。
(5)步骤⑨的作用是 。
(6)称取400g茶叶样品灼烧得灰粉后,加入过量盐酸后过滤,将所得滤液加入过量的(NH4)2C2O4溶液,再过滤、洗涤、干燥、称量得到5.12g沉淀,原茶叶中钙元素的质量分数为 。
-
茶是我国人民喜爱的饮品,其中含有多种有益于人体健康的成分,据测定茶叶中含有450种以上的有机成分与15种以上的元素.某化学研究小组欲探究茶叶中钙元素的含量,设计了探究实验方案如下:(已知茶叶中的铝、铁元素对钙离子的测定有影响)
步骤1:称取500克干燥的茶叶,置于通风橱中,充分灼烧使茶叶灰化,再用研钵磨细后移入烧杯中,然后将200mL 1mol•L-1盐酸加入灰中搅拌、过滤、洗涤.
步骤2:向步骤1所得滤液中逐滴加入稀氢氧化钠溶液,调节溶液的pH为6~7左右,使铝、铁的氢氧化物完全沉淀,再加热煮沸30min,加入7.95g无水碳酸钠,充分搅拌,待沉淀完全后,过滤,洗涤,过滤后得到滤液和沉淀.
步骤3:将步骤2所得的滤液稀释至500mL,取其中的20.00mL溶液以甲基橙作指示剂,用0.1000mol.L-1的HCl标准溶液滴定,终点时消耗盐酸的体积为20.00mL,计算结果.请回答下列问题:
(1)步骤 1中,使茶叶灰化需要三角架、泥三角、酒精喷灯、______、______等仪器.
(2)步骤2中,判断沉淀已经洗涤干净的方法是______.
(3)步骤3中,滴定操作时,眼睛注视______.被滴定的20mL滤液中 CO32-的物质的量为______mol,原茶叶中钙离子的质量分数为______.
-
某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有钙、铁、铝三种金属元素。【已知完全沉淀的pH:Ca(OH)2:pH ≥ 13;Al(OH)3:pH ≥ 5.5;Fe(OH)3:pH ≥ 4.1】
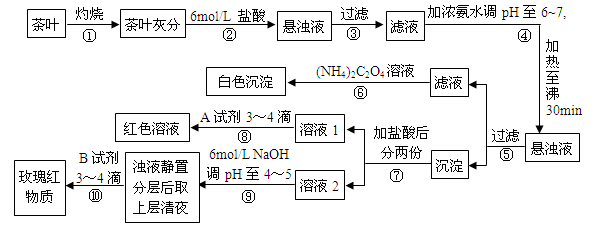
下列说法不正确的是
A.步骤②加入6mol/L盐酸的主要目的是为了将茶叶灰分中的钙、铁、铝难溶性化合物转化为可溶性氯化物
B.步骤⑤所得滤液中溶质的主要成分为:CaCl2、NH3·H2O
C.步骤⑥可以检出钙元素存在,离子反应方程式为Ca2++C2O42- = CaC2O4↓
D.步骤⑧中A试剂为KSCN溶液,离子反应方程式为Fe3++3SCN-  Fe(SCN)3
Fe(SCN)3
-
某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有钙、铁、铝三种金属元素。【已知完全沉淀的pH:Ca(OH)2:pH ≥ 13;Al(OH)3:pH ≥ 5.5;Fe(OH)3:pH ≥ 4.1】
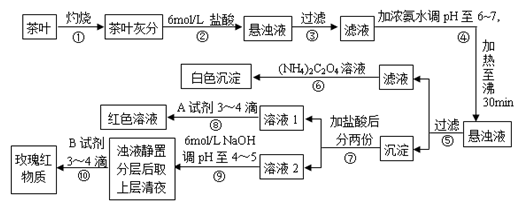
下列说法不正确的是( )
A.步骤②加入6mol/L盐酸的主要目的是为了将茶叶灰分中的钙、铁、铝难溶性化合物转化为可溶性氯化物
B.步骤⑤所得滤液中溶质的主要成分为:CaCl2、NH3·H2O
C.步骤⑥可以检出钙元素存在,离子反应方程式为Ca2++C2O42- = CaC2O4↓
D.步骤⑧中A试剂为KSCN溶液,离子反应方程式为Fe3++3SCN-  Fe(SCN)3
Fe(SCN)3
-
某化学兴趣小组设计以下实验步骤与操作来定性检验茶叶中含有的少量钙、铁、铝三种元素。
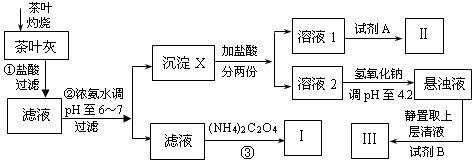
已知Ca2+、Al3+、Fe3+完全形成相应氢氧化物沉淀的pH如下表:
| Ca(OH)2 | Al(OH)3 | Fe(OH)3 |
| pH | ≥13 | ≥5.2 | ≥4.1 |
(1)步骤①中加入盐酸的作用是 ________________。
(2)步骤②中调节pH至6~7的目的是________________。
(3)沉淀X所含主要物质的化学式为 ________________。
(4)写出步骤③中发生反应的离子方程式:________。
(5)试剂A为________;试剂B为铝试剂,加入该试剂后的实验现象是________。
-
化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:①该牙膏摩擦剂由碳酸钙、氢氧化铝组成;
②牙膏中其它成分遇到盐酸时无气体产生。
实验内容:Ⅰ.摩擦剂中氢氧化铝的定性检验。
取适量牙膏样品,加水充分搅拌、过滤,往滤渣中加入过量NaOH溶液。
(1)该过程涉及主要反应的离子方程式是 。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的沉淀质量,以确定碳酸钙的质量分数。
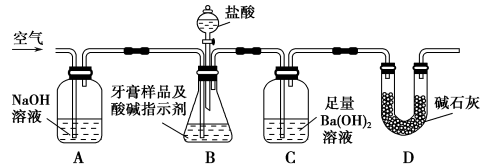
依据实验过程回答下列问题:
(2)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:_________________________。
(3)C中反应生成沉淀的化学方程式是_____________________。
(4)下列各项措施中,能提高测定准确度的是________(填标号)。
a.滴加盐酸不宜过快
b.在A~B之间增添盛有浓硫酸的洗气装置
c.在加入盐酸之前,应排净装置内的CO2气体
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取10.00 g样品三份,进行三次测定,测得C中产生沉淀平均质量为3.94 g。则样品中碳酸钙的质量分数为________。
(6)有人认为只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是______________________。
-
生铁中含碳和硫等元素。化学兴趣小组对某生铁样品成分及其含量进行探究。
I.生铁中碳和硫元素的定性检验
(1)将以下装置进行连接以完成实验(夹持仪器已略去,填接口字母代号)
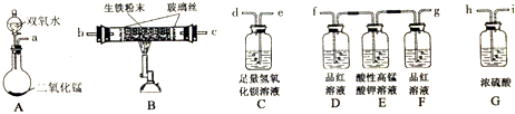
a→( ) →( ) →( ) →( ) →( ) →( ) →( )
(2)将样品研磨成粉末的目的是 。
(3)确认样品中含有碳元素的现象是 。
II.生铁中碳、硫质量分数的测定
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量。称取样品m1g进行实验,
充分反应后,测得C中生成的沉淀为m2g,该样品中碳的质量分数不小于(用含m1、m2的式子表示)
(5)乙同学认为,待一定量样品充分反应后,向E装置中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案是否合理? (填“是”或“否”);说明理由 。
(6)丙同学提议:为测定样品中硫的含量,可将c装置中试剂改为足量的30%双氧水,并按A→C→B→C装置连接进行实验,充分反应后,请你简述后续的实验方案 。
-
茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案用以测定某品牌茶叶中钙元素的质量分数并检验铁元素的存在(已知 为白色沉淀物质)。首先取200g茶叶样品焙烧得灰粉后进行如下操作:
为白色沉淀物质)。首先取200g茶叶样品焙烧得灰粉后进行如下操作:
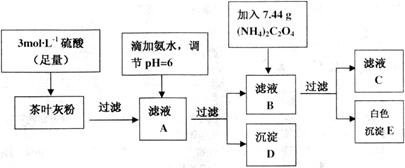
请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为::
| 离子 | 
| 
|
| 完全沉淀时的pH | 13 | 4.1 |
实验前要先将茶叶样品高温灼烧成灰粉,其主要目的是__________。
(2)写出从滤液A→沉淀D的离子反应方程式__________。
(3)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,试
判断沉淀D已经洗涤干净的方法是__________。
(4)用KMnO 标准溶液滴定C溶液时所发生的反应为:
标准溶液滴定C溶液时所发生的反应为:
 。
。
现将滤液C稀释至500 mL,再取其中的25.00 mL溶液,用硫酸酸化后,用0.1000
mol·L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00 mL。
①此步操作过程中需要用到下列哪些仪器(填写序号)________;
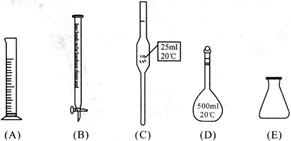
②达到滴定终点时,溶液的颜色变化是________;
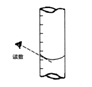
③滴定到终点,静置后,如右图读取KMnO4标准溶液的刻度数据,则测定的钙元素含量将________ (填“偏高”、“偏低”、“无影响”)。
(5)原茶叶中钙元素的质量分数为________。
(6)可以通过检验滤液A来验证该品牌茶叶中是否含有铁元素,所加试剂及实验现象是________。










