已知下列弱酸的电离常数:
H2CO3: Ka1=4.30×10-7 ;Ka2=5.61×10-11
H2SO3: Ka1=1.54×10-2 ;Ka2=1.02×10-7
HClO:Ka=2.95×10-8
下列离子在溶液中结合H+的能力不正确的是
A.HCO>HSO3- B. CO
>SO
C.HCO
>ClO- D.ClO->SO
高二化学选择题中等难度题
已知下列弱酸的电离常数:
H2CO3: Ka1=4.30×10-7 ;Ka2=5.61×10-11
H2SO3: Ka1=1.54×10-2 ;Ka2=1.02×10-7
HClO:Ka=2.95×10-8
下列离子在溶液中结合H+的能力不正确的是
A.HCO>HSO3- B. CO
>SO
C.HCO
>ClO- D.ClO->SO
高二化学选择题中等难度题
已知下列弱酸的电离常数:
H2CO3: Ka1=4.30×10-7 ;Ka2=5.61×10-11
H2SO3: Ka1=1.54×10-2 ;Ka2=1.02×10-7
HClO:Ka=2.95×10-8
下列离子在溶液中结合H+的能力不正确的是
A.HCO>HSO3- B. CO
>SO
C.HCO
>ClO- D.ClO->SO
高二化学选择题中等难度题查看答案及解析
已知部分弱酸的电离平衡常数如下表:
| 弱酸 | H2CO3 | HClO | HF |
| 电离平衡常数 (25℃) | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka=2.98×10-8 | Ka=3.6×10-4 |
下列叙述正确的是
A. Na2CO3溶液不能与次氯酸发生反应
B. 物质的量浓度相同的①NaF②Na2CO3③NaClO三种溶液的pH:③>②>①
C. 氢氟酸与NaClO溶液混合能够发生反应:HF+NaClO=HClO+NaF
D. 少量CO2通入NaClO溶液中的离子反应:CO2+H2O+2ClO-=CO32-+2HClO
高二化学单选题中等难度题查看答案及解析
已知部分弱酸的电离平衡常数如表:
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数(25℃) | Ka=1.75×10-5 | Ka=2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
下列离子方程式正确的是( )
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-═CO+2HClO
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO
C.少量SO2通入Na2CO3溶液中:SO2+H2O+2CO═SO
+2HCO
D.相同浓度NaHCO3溶液与醋酸溶液等体积混合:H++HCO═CO2↑+H2O
高二化学单选题中等难度题查看答案及解析
已知部分弱酸的电离平衡常数如表所示
| 弱酸 | CH3COOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数Ka(25℃) | 1.75×10-5 | 2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
下列离子方程式正确的是( )
A.CO2+H2O +2C1O- =CO32-+2HClO B.2CH3COOH+CO32-=2CH3COO-+CO2↑ +H2O
C.SO2+H2O +Ca2+ +2ClO-=CaSO3↓ +2HClO D.SO2+CO32-=CO2+SO32-
高二化学单选题中等难度题查看答案及解析
已知部分弱酸的电离平衡常数如下表:
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数(25℃) | Ka=1.75×10-5 | Ka=2.98×10-8 | Ka1=4.30×10-7 | Ka1=1.54×10-2 |
下列离子方程式正确的是
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-=CO+2HClO
B.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.少量的SO2通入Na2CO3溶液中:SO2+H2O+2 CO=SO
+2HCO3-
D.相同浓度NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-=CO2↑+H2O
高二化学单选题困难题查看答案及解析
已知部分弱酸的电离平衡常数如表所示:
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数(25 ℃) | Ka=1.75×10-5 | Ka=2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
下列离子方程式正确的是
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-=CO32-+2HClO
B.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.少量的SO2通入Na2CO3溶液中:SO2+H2O+2CO32-=SO32-+2HCO3-
D.相同浓度NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-=CO2↑+H2O
高二化学单选题中等难度题查看答案及解析
已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
| 醋酸 | 碳酸 | 亚硫酸 |
| Ka=1.75×10﹣5 | Ka1=4.30×10﹣7 Ka2=5.61×10﹣11 | Ka1=1.54×10﹣2 Ka2=1.02×10﹣7 |
(1)写出碳酸的第一步电离平衡常数表达式:Ka1=__.
(2)在相同条件下,试比较H2CO3、HCO3﹣和HSO3﹣的酸性强弱:__>__>__.
(3)如图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液pH随水量的变化图象中:
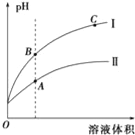
①曲线I表示的酸是__(填化学式).
②A、B、C三点中,水的电离程度最大的是__(填字母).
(4)下列事实不能说明醋酸是弱酸的是_______
①当温度低于16.6℃时醋酸可凝结成冰一样晶体
②0.1mol/L的醋酸钠溶液的pH约为9
③等体积等物质的量浓度的硫酸比醋酸消耗氢氧化钠多
④0.1mol/L的醋酸的pH约为4.8
⑤pH都等于4且等体积的醋酸和盐酸,与等浓度NaOH溶液充分反应时,醋酸消耗碱液多
⑥同物质的量浓度的醋酸和盐酸加水稀释至pH相同时,醋酸加入的水多
高二化学填空题中等难度题查看答案及解析
已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
| 醋酸 | 碳酸 | 亚硫酸 |
| Ka=1.75×10﹣5 | Ka1=4.30×10﹣7 Ka2=5.61×10﹣11 | Ka1=1.54×10﹣2 Ka2=1.02×10﹣7 |
(1)写出碳酸的第一步电离平衡常数表达式:Ka1=__.
(2)在相同条件下,试比较H2CO3、HCO3﹣和HSO3﹣的酸性强弱:__>__>__.
(3)如图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液pH随水量的变化图象中:
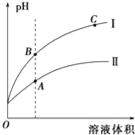
①曲线I表示的酸是__(填化学式).
②A、B、C三点中,水的电离程度最大的是__(填字母).
(4)下列事实不能说明醋酸是弱酸的是_______
①当温度低于16.6℃时醋酸可凝结成冰一样晶体
②0.1mol/L的醋酸钠溶液的pH约为9
③等体积等物质的量浓度的硫酸比醋酸消耗氢氧化钠多
④0.1mol/L的醋酸的pH约为4.8
⑤pH都等于4且等体积的醋酸和盐酸,与等浓度NaOH溶液充分反应时,醋酸消耗碱液多
⑥同物质的量浓度的醋酸和盐酸加水稀释至pH相同时,醋酸加入的水多
高二化学填空题中等难度题查看答案及解析
已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
| 醋酸 | 碳酸 | 亚硫酸 |
| Ka= 1.75×10-5 | Ka1= 4.30×10-7 Ka2 = 5.61×10-11 | Ka1= 1.54×10-2 Ka2 = 1.02×10-7 |
(1)写出碳酸的第二步电离平衡常数表达式Ka2= 。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱 > > 。
(3)下图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液pH随水量的变化:
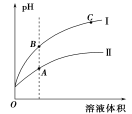
①图像中,曲线I表示的酸是 (填化学式)。
②A、B、C三点中,水的电离程度最大的是 (填字母)。
高二化学填空题困难题查看答案及解析
(8分)已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
| 醋酸 | 碳酸 | 亚硫酸 |
| Ka= 1.75×10-5 | Ka1= 4.30×10-7 Ka2 = 5.61×10-11 | Ka1= 1.54×10-2 Ka2 = 1.02×10-7 |
(1)写出碳酸的第一步电离平衡常数表达式:Ka1 = 。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱: > > 。
(3)下图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化
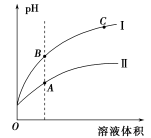
①图像中,曲线I表示的酸是 (填化学式)。
②A、B、C三点中,水的电离程度最大的是 (填字母)。
高二化学填空题困难题查看答案及解析