-
有四组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如下表所示:
第一组
A -268.8
B -249.5
C -185.8
D -151.7
第二组
F2 -187.0
Cl2 -33.6
Br2 58.7
I2 184.0
第三组
HF 19.4
HCl -84.0
HBr -67.0
HI -35.3
第四组
H2O 100.0
H2S -60.2
H2Se -42.0
H2Te -1.8
下列各项判断正确的是
A. 第四组物质中H2O的沸点最高,是因为H2O分子中化学键键能最强
B. 第三组与第四组相比较,化合物的稳定性顺序为:HBr>H2Se
C. 第三组物质溶于水后,溶液的酸性:HF>HCl>HBr>HI
D. 第一组物质是分子晶体,一定含有共价键
高二化学单选题中等难度题查看答案及解析
-
有五个系列同族元素的物质,101.3kPa时测定它们的沸点(℃)如下表所示:
①
He -268.8
(a) -249.5
Ar -185.8
Kr 151.7
②
F2 -187.0
Cl2 -33.6
(b) 58.7
I2 184.0
③
(c) 19.4
HCl -84.0
HBr -67.0
HI -35.3
④
H2O 100.0
H2S -60.0
(d) -42.0
H2Te -1.8
⑤
CH4 -161.0
SiH4 -112.0
GeH4 -90.0
(e) -52.0
对应表中内容,下列叙述中正确的是
A.a、b、c代表的化学物中均含化学键
B.系列②物质均有氧化性;系列③物质对应水溶液均是强酸
C.系列④中各化合物的稳定性顺序为:H2O>H2S>H2Se>H2Te
D.上表中物质HF和H2O,由于化学键的影响,其沸点出现反常现象
高二化学选择题中等难度题查看答案及解析
-
有五个系列的同族元素的物质,101.3 kPa时测定的沸点(℃)如下表所示:
①
He-268.8
(a)-249.5
Ar-185.8
Kr-151.7
②
F2-187.0
Cl2-33.6
(b)5.7
I2184.0
③
(c)19.4
HCl-84.0
HBr-67.0
HI-35.5
④
H2O100.0
H2S-60.0
(d)-42.0
H2Te-1.8
⑤
CH4-161.0
SiH4-112.0
GeH4-90.0
(e)-52.0
对应表中内容,下列叙述中不正确的是( )
A.a、b、e的化学式分别为Ne、Br2、SnH4
B.系列②物质均有氧化性,系列③物质对应水溶液均是强酸
C.系列④中各化合物的稳定性顺序为:H2O>H2S>(d)>H2Te
D.上表内的物质(c)和H2O,由于氢键的影响,其熔沸点在同族中特别高
高二化学选择题简单题查看答案及解析
-
有五组同族元素的物质,在101.3kPa时测定它们的沸点(℃)如下表所示:
①
He-268.8
(a)-249.5
Ar-185.8
Kr151.7
②
F2-187.0
Cl2-33.6
(b)58.7
I2184.0
③
(c)19.4
HCl-84.0
HBr-67.0
HI-35.3
④
H2O100.0
H2S-60.0
(d)-42.0
H2Te-1.8[
⑤
CH4-161.0
SiH4-112.0
GeH4-90.0
(e)-52.0
对应表中内容,下列各项中正确的是
A.a、b、c的化学式分别为Ne2、Br2、HF
B.第④组中各化合物的稳定性顺序为:H2O>H2S>H2Se>H2Te
C.第②组物质均有氧化性;第③组物质对应水溶液均是强酸
D.上表中同族物质对应的氢化物的沸点,均随相对分子质量的增大而升高
高二化学选择题困难题查看答案及解析
-
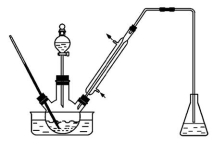
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置如图,相关物质的沸点见附表)。附表 相关物质的沸点(101 kPa)
物质
沸点/℃
物质
沸点/℃
溴
58.8
1,2-二氯乙烷
8
3.5
苯甲醛
179
间溴苯甲醛
229
其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60 ℃,缓慢滴加经浓H2SO4h!t干燥过的液溴,保温反应一段时间,冷却。
平台步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机层用10%NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4:减压蒸馏有机层,收集相应馏分。
(1)实验装置中冷凝管的主要作用是 ,锥形瓶中的溶液应为 。
(2)步骤1所加入的物质中,有一种物质是催化剂,其化学式为 。
(3)步骤2中用10%NaHCO3溶液洗涤有机层,是为了除去溶于有机层的 (填化学式)。
(4)步骤3中加入无水MgSO4固体的作用是 。
(5)步骤4中采用减压蒸馏技术,是为了防止 。
高二化学实验题困难题查看答案及解析
-
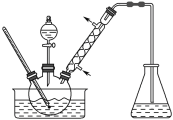
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的沸点见附表)。
附表 相关物质的沸点(101kPa)
物质
沸点/℃
物质
沸点/℃
溴
58.8
1,2-二氯乙烷
83.5
苯甲醛
179
间溴苯甲醛
229
其实验步骤为
步骤1:将三颈烧瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓H2SO4干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液,有机层用10%NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4: 。
试回答:
(1)实验装置中冷凝管的作用是冷凝回流,主要是减少___的挥发,锥形瓶中的溶液应为___。
(2)步骤1所加入的无水AlCl3,其作用是___。
(3)步骤2中用10%NaHCO3溶液洗涤是为了除去___(填化学式),该步骤是在___(填仪器名称)中完成的。
(4)步骤3中加入无水MgSO4固体的作用是___。
(5)步骤4的操作名称是___。
(6)步骤1中不能有水,一是AlCl3遇水会水解,另一个原因是有水时苯甲醛会和溴发生副反应,写出该副反应的化学方程式___。
高二化学实验题中等难度题查看答案及解析
-
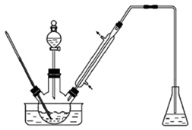
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见下图,相关物质的沸点见附表)。
附表:相关物质的沸点(101KPa)
物质
沸点/℃
物质
沸点/℃
溴
58.8
1,2-二氯乙烷
83.5
苯甲醛
179
间溴苯甲醛
229
其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经H2SO4干燥过的液溴,保温反应一段时间,冷却.
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液.有机相用10%NaHCO3溶液洗涤.
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤.
步骤4:减压蒸馏有机相,收集相应馏分。
(1)实验装置A的名称是___________,锥形瓶中的溶液应为_________。
(2)步骤1所加入的物质中,有一种物质是催化剂,其化学式为____________;
(3)步骤2中用10%NaHCO3溶液洗涤有机相,是为了除去溶于有机相的____________(填化学式).
(4)步骤3中加入无水MgSO4固体的作用是__________,分离的方法是____________;
(5)步骤4中采用减压蒸馏技术,是为了防止____________。
高二化学实验题简单题查看答案及解析
-
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积。该小组设计的简单实验装置如图所示:
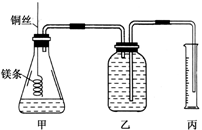
该实验的主要操作步骤如下:
①配制质量分数为36.5%的盐酸(假设其密度为1g/cm3);
②量取10.0mL该盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为___________;
④往广口瓶中装入足量水,按如图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请回答下列问题.
(1)题中涉及反应的化学方程式为___________。
(2)实验步骤⑤中应选用___________(填序号)的量筒.
A.1000mL B.2000mL C.5000mL
读数时除恢复到室温外,还要注意___________;
(3)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算式为Vm= ___________,若未除去镁条表面的氧化膜,则测量结果___________(填“偏大”、“偏小”或“无影响”)。
高二化学实验题简单题查看答案及解析
-
(15分)请回答以下问题:
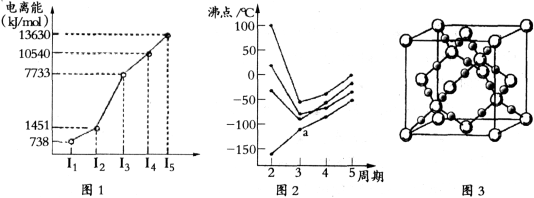
(1)第四周期的某主族元素,其第一至五电离能数据如下图1所示,则该元素对应原子的M层电子排布式为 。
(2)如下图2所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是 。简述你的判断依据
。
(3)CO2在高温高压下所形成的晶体其晶胞如下图3所示.该晶体的类型属于 (选填“分子”“原子”“离子”或“金属”)晶体。
(4)BCl3原子的杂化方式为 。第一电离能介于B、N之间的第二周期元素有
种。写出与BCl3结构相同的一种等电子体(写离子) 。
(5)Cu元素形成的单质,其晶体的堆积模型为______ ,D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是________ (填选项序号)。
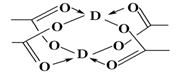
①极性键 ②非极性键 ③配位键 ④金属键
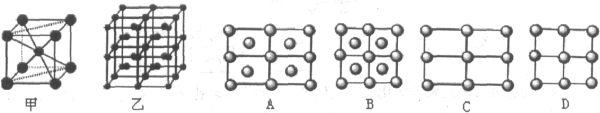
(6)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的A-D图中正确的是 .铁原子的配位数是 ,假设铁原子的半径是r cm,该晶体的密度是p g/cm3,则铁的相对原子质量为 (设阿伏加德罗常数的值为NA)。
高二化学填空题困难题查看答案及解析
-
下列给出的几种氯化物的熔点和沸点:
NaCl
MgCl2
AlCl3
SiCl4
熔点/℃
801
714
190(5×101 kPa)
-70
沸点/℃
1413
1412
180
57.57
据表中所列数据判断下列叙述与表中相吻合的是( )
A.AlCl3在加热条件下能升华 B.SiCl4晶体属于原子晶体
C.AlCl3晶体是典型的离子晶体 D.NaCl的晶格能比MgCl2小
高二化学单选题简单题查看答案及解析