常温下,用0.50mol/L氢氧化钠溶液滴定某一元弱酸(HA)的溶液中,滴定曲线如图所示,下列叙述不正确的是
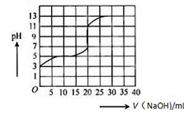
A.该弱酸在滴定前的浓度大于0.001mol/L
B.由滴定起点数据可计算该弱酸的Ka(电离平衡常数)为2×10-5
C.滴定过程为求滴定终点,最合适的指示剂是酚酞
D.滴定终点时,c(Na+) >c(A-) > c(OH-) >c(H+)
高三化学选择题中等难度题
常温下,用0.50mol/L氢氧化钠溶液滴定某一元弱酸(HA)的溶液中,滴定曲线如图所示,下列叙述不正确的是

A.该弱酸在滴定前的浓度大于0.001mol/L
B.由滴定起点数据可计算该弱酸的Ka(电离平衡常数)为2×10-5
C.滴定过程为求滴定终点,最合适的指示剂是酚酞
D.滴定终点时,c(Na+) >c(A-) > c(OH-) >c(H+)
高三化学选择题中等难度题
常温下,用0.50mol/L氢氧化钠溶液滴定某一元弱酸(HA)的溶液中,滴定曲线如图所示,下列叙述不正确的是

A.该弱酸在滴定前的浓度大于0.001mol/L
B.由滴定起点数据可计算该弱酸的Ka(电离平衡常数)为2×10-5
C.滴定过程为求滴定终点,最合适的指示剂是酚酞
D.滴定终点时,c(Na+) >c(A-) > c(OH-) >c(H+)
高三化学选择题中等难度题查看答案及解析
以0.10mol/L的氢氧化钠溶液滴定某一元弱酸的滴定曲线如图所示。横轴为加入氢氧化钠的体积数,纵轴为溶液的pH。下列正确的是
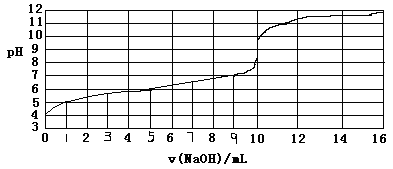
A.此一元弱酸的电离常数(Ka)约为1.0×10-6
B.此弱酸的浓度为1×10-4mol/L
C.此实验最好选用甲基红(变色范围在4.2~6.3)作指示剂
D.此滴定反应为吸热反应
高三化学选择题中等难度题查看答案及解析
常温下,用0.1000mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程溶液pH随NaOH溶液的体积的变化曲线如图所示(忽略中和热效应)。下列说法不正确的是
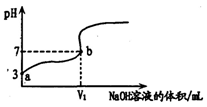
A. 常温下,HA的电离常数K(HA)约为10-5
B. v1<20
C. 溶液中水的电离程度:a点>b点
D. 滴定过程为了确定滴定终点,最合适的指示剂是酚酞
高三化学选择题中等难度题查看答案及解析
常温下,用0.1mol/L的NaOH溶液滴定相同浓度的一元弱酸HA20mL,滴定过程中溶液的pH随滴定分数(滴定分数=  ) 的变化曲线如图所示(忽略中和热效应),下列说法不正确的是
) 的变化曲线如图所示(忽略中和热效应),下列说法不正确的是

A. HA溶液加水稀释后,溶液中c(HA)/c(A-)的值减少
B. 当滴定分数为1时,溶液中水的电离程度最大
C. 当滴定分数大于1时,溶液中离子浓度关系一定是c(Na+)>c(A-)>c(OH-)> c(H+)
D. 当滴定分数为x时,HA的电离常数为KHA=(10-7x)/(1-x)
高三化学单选题困难题查看答案及解析
以0.10mol/L的氢氧化钠溶液滴定某一元弱酸(已知其在该条件下的电离度α≈1%)的滴定曲线如图所示。横坐标为加入氢氧化钠的体积,纵坐标为溶液的pH。下列说法正确的是( )
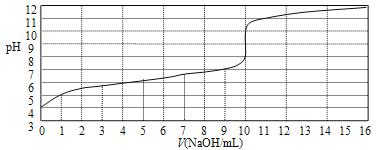
A.此一元弱酸的电离常数(Ka)约为1.0×10-6
B.此弱酸的浓度为1×10-4mol/L
C.此实验可选用甲基橙作指示剂
D.此实验可选用酚酞作指示剂
高三化学多选题中等难度题查看答案及解析
常温下,用0.1000mol/L的NaOH溶液滴定20ml同浓度的一元弱酸HA,滴定过程溶液pH随X的变化曲线如图所示(忽略中和热效应,滴定分数是指滴定剂与被滴定物质的物质的量之比),下列说法不正确的是

A.HA溶液加水稀释后,溶液中的值减小
B.HA的电离常数(x为滴定分数)
C.当滴定分数为100时,溶液中水的电离程度最大
D.滴定分数大于100时,溶液中离子浓度关系一定是c(Na+)>c(A-)>c(OH-)>c(H+)
高三化学选择题困难题查看答案及解析
常温下,0.1000mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.1000mol·L-1的两种一元酸HX、HY溶液,滴定曲线如图所示。下列说法正确的是

A. HX是强酸,HY是弱酸
B. V[NaOH(aq)]=10.00mL时,
C. V[NaOH(aq)]=20.00mL时,所得的两种溶液的pH均等于7
D. V[NaOH(aq)]=20.00mL时,所得的两种溶液的导电性,HX的比HY的强
高三化学选择题困难题查看答案及解析
常温下,用0.1000mol/L的NaOH溶液滴定20ml同浓度的一元弱酸HA,滴定过程溶液pH随X的变化曲线如图所示(忽略中和热效应),下列说法不正确的是
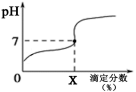
A.HA溶液加水稀释后,溶液中的值减小
B.HA的电离常数(x为滴定分数)
C.当滴定分数为100时,溶液中水的电离程度最大
D.滴定分数大于100时,溶液中离子浓度关系一定是c(Na+)>c(A-)>c(OH-)>c(H+)
高三化学选择题困难题查看答案及解析
常温下,用0.1000mol/L的NaOH溶液滴定20ml同浓度的一元弱酸HA,滴定过程溶液pH随X的变化曲线如图所示(忽略中和热效应),下列说法不正确的是

A.HA溶液加水稀释后,溶液中的值减小
B.HA的电离常数(x为滴定分数)
C.当滴定分数为100时,溶液中水的电离程度最大
D.滴定分数大于100时,溶液中离子浓度关系一定是c(Na+)>c(A-)>c(OH-)>c(H+)
高三化学选择题中等难度题查看答案及解析
常温下,用0.1000mol/L的NaOH溶液滴定20ml同浓度的一元弱酸HA,滴定过程溶液pH随X的变化曲线如图所示(忽略中和热效应),下列说法不正确的是
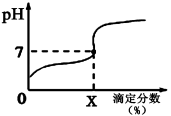
A.HA溶液加水稀释后,溶液中的值减小
B.HA的电离常数(x为滴定分数)
C.当滴定分数为100时,溶液中水的电离程度最大
D.滴定分数大于100时,溶液中离子浓度关系一定是c(Na+)>c(A-)>c(OH-)>c(H+)
高三化学选择题极难题查看答案及解析