-
(3分)防治碘缺乏病的碘添加剂是KIO3(如加碘盐),可用盐酸酸化的KI淀粉混合液检验食盐是否加碘,其反应的离子方程式为:________
高三化学填空题简单题查看答案及解析
-
①在家庭中用食醋和碘化钾淀粉试纸检验食盐是否是加碘(KIO3)盐
②用酒精从碘水中萃取碘
③用加热的方法从碘和沙子的混合物中分离出碘
④实验室制Cl2、C2H4都用同一套装置
⑤用淀粉溶液直接检验I-
⑥根据加入AgNO3溶液产生白色沉淀的现象认定溶液中含Cl-
⑦盛放液溴的试剂瓶内放少量蒸馏水防止液溴的挥发
⑧用溴水鉴别C2H4和C2H6
A. ①②③⑧ B. ③④⑥⑦ C. ①③⑦⑧ D. ②④⑥⑦
高三化学选择题中等难度题查看答案及解析
-
市售食盐常有无碘盐和加碘盐(含KIO3和少量的KI)。
I. 某同学设计检验食盐是否为加碘盐的定性实验方法:
①取待检食盐溶于水,加入稀硫酸酸化,再加入过量的KI溶液,振荡。
②为验证①中有I2生成,向上述混合液中加入少量CCl4充分振荡后,静置。
(1)若为加碘盐,则①中发生反应的离子方程式为_________。
(2)②中的实验操作名称是_________。
(3)实验过程中能证明食盐含KIO3的现象是_________。
Ⅱ. 碘摄入过多或者过少都会增加患甲状腺疾病的风险。目前国家标准(GB/T13025.7)所用的食盐中碘含量测定方法:
①用饱和溴水将碘盐中少量的I-氧化成IO3-。
②再加入甲酸发生反应:Br2+HCOOH=CO2↑+2HBr。
③在酸性条件下,加入过量KI,使之与IO3-完全反应。
④以淀粉作指示剂,用Na2S2O3标准溶液进行滴定,测定碘元素的含量。
I2+2Na2S2O3=2NaI+Na2S4O6
(1)①中反应的离子方程式为_________。
(2)测定食盐碘含量过程中,Na2S2O3,与IO3-的物质的量之比为_________。
(3)有人提出为简化操作将①、②省略,但这样会造成测定结果偏低。请分析偏低的原因:__________________。
高三化学实验题中等难度题查看答案及解析
-
(12分) 为防止碘缺乏病,通常在食盐中加入KIO3。
(1)用淀粉碘化钾溶液和稀硫酸可定性检验出食盐中的IO3-,表示该反应的离子方程
式是________________________________________,
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液
将I2还原,又可以回收四氯化碳。Na2SO3稀溶液与I2反应的离子方程式是 ________。
(3)已知:I2+2S2O32-=2I-+S4O62-。
某课外活动小组为测定混有MgCl2的食用加碘盐中所含MgCl2、KIO3的含量,按下图所示实验步骤进行实验。
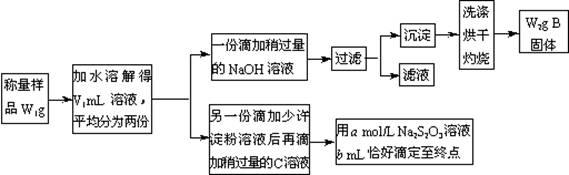
请回答下列问题:
①写出B和C的化学式:B________,C________。
②滴定时,判断滴定达到终点的现象是________。
③KIO3的质量分数是________(列出计算式)。
④使所测MgCl2的质量分数可能偏高的操作是(填写字母)________
A 过滤后未洗涤所得沉淀,直接烘干灼烧
B 在敞口容器中用托盘天平称量样品时,操作时间过长
C 沉淀灼烧不彻底
高三化学实验题中等难度题查看答案及解析
-
I.(1)已知食盐常加入KIO3来补充碘元素,检验食盐中是否加碘,可利用如下反应:__KIO3+___KI+___H2SO4═___K2SO4+___I2+___H2O(配平反应方程式)
①利用上述反应检验食盐中是否加碘,所需试剂是________(填下列选项的序号)
A、碘水 B、KI溶液 C、淀粉溶液 D、稀硫酸 E、AgNO3溶液
②如果反应中转移0.2mol电子,则生成I2的物质的量为___________
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染.化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气)若反应中消耗Cl21.5mol则被氧化的NH3在标准状况下的体积为__________L.
II.用98%的浓硫酸(其密度为1.84g/cm3)配制100mL 1.0mol.L-1稀硫酸,
实验步骤如下:①计算所用浓硫酸的体积②量取一定体积的浓硫酸③溶解④检漏、转移、洗涤⑤定容、摇匀。若实验仪器有:A.100mL量筒 B.托盘天平 C.玻璃棒D.50mL容量瓶 E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
回答下列问题:
(1)需量取浓硫酸的体积为___________mL.
(2)实验时选用的仪器有___________(填序号)
(3)配制过程中,下列情况会使配制结果偏高的是___________(填序号)
①定容时俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
④所用的浓硫酸长时间放置在密封不好的容器中⑤用量筒量取浓硫酸时仰视读数
高三化学简答题中等难度题查看答案及解析
-
I-具有还原性,含碘食盐中的碘元素主要以KIO3的形式存在,I-、I2、IO3-在一定条件下可发生如图转化关系,下列说法不正确的是
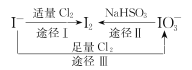
A.用淀粉-KI试纸和食醋可检验食盐是否加碘
B.由图可知氧化性的强弱顺序为Cl2>IO3->I2
C.生产等量的碘,途径I和途径II转移电子数目之比为5 :2
D.途径III反应的离子方程式:3Cl2+I-+3H2O=6Cl-+IO3-+6H+
高三化学单选题中等难度题查看答案及解析
-
I-具有还原性,含碘食盐中的碘元素主要以KIO3的形式存在,I-、I2、IO3-在一定条件下可发生如图转化关系,下列说法不正确的是
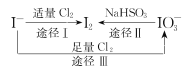
A.用淀粉-KI试纸和食醋可检验食盐是否加碘
B.由图可知氧化性的强弱顺序为Cl2>IO3->I2
C.生产等量的碘,途径I和途径II转移电子数目之比为5 :2
D.途径III反应的离子方程式:3Cl2+I-+3H2O=6Cl-+IO3-+6H+
高三化学单选题中等难度题查看答案及解析
-
I-具有还原性,含碘食盐中的碘元素主要以KIO3的形式存在,I-、I2、IO3-在一定条件下可发生如图转化关系。下列说法不正确的是
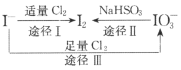
A.用淀粉-KI试纸和食醋可检验食盐是否加碘
B.由图可知氧化性的强弱顺序为C12>IO3->I2
C.生产等量的碘,途径I和途径Ⅱ转移电子数目之比为2:5
D.途径Ⅲ反应的离子方程式:3C12+I-+3H2O=6C1-+IO3-+6H+
高三化学单选题简单题查看答案及解析
-
为消除碘缺乏病,卫生部规定食盐必须加碘,其中的碘以碘酸钾(KIO3)的形式存在。已知溶液中的IO3-可和I-发生反应:IO3-+5I-+6H+===3I2+3H2O。根据此反应,可用试纸和一些生活中常用的物质进行实验,证明在食盐中存在IO3-,可供选用的物质有:①自来水;②蓝色石蕊试纸;③KI淀粉试纸;④淀粉;⑤食糖;⑥食醋;⑦白酒。进行上述实验时必须使用的物质是( )
A.①③ B.③⑥
C.②④⑥ D.①②④⑤⑦
高三化学选择题中等难度题查看答案及解析
-
下列实验方案,不能达到实验目的的是( )
选项
实验目的
实验方案
A
检验食盐中是否添加KIO3
取食盐试样,溶于KI溶液,加入淀粉溶液,观察溶液是否变蓝
B
验证氯酸钾中含有氯元素
取少量氯酸钾加入MnO2充分加热,残留物溶于水,取上层清液,滴入稀硝酸酸化的AgNO3溶液,观察是否有白色沉淀
C
验证硝酸是挥发性酸
用两根玻璃棒分别蘸取浓硝酸和浓氨水,然后靠近,观察是否有白烟产生
D
验证Br2氧化性强于Fe3+
取少许FeCl2晶体溶于稀盐酸,加入KSCN观察溶液是否变红,滴入溴水后再观察是否变红
高三化学选择题中等难度题查看答案及解析