-
(12分)Al及其化合物用途广泛,工业上可以将明矾石经处理后得到明矾[KAl(SO4)2·12H2O],再将明矾焙烧后制得Al2O3等物质,进一步处理后还可以得到Al。
已知焙烧明矾的化学方程式为:
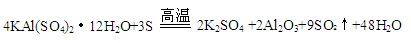
请回答:
(1)Al2O3的摩尔质量是 。
(2)工业上可用电解Al2O3制备Al,其化学方程式是 。
(3)在焙烧明矾的反应中,氧化剂和还原剂的物质的量之比是 。
(4)焙烧明矾时产生的SO2可综合利用来制硫酸。
已知25℃、101 kPa时:
2SO2(g) +O2(g) 2SO3(g) △H1 = 一197 kJ/mol
2SO3(g) △H1 = 一197 kJ/mol
2H2O (g)=2H2O(1) △H2 = 一44 kJ/mol
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3 = 一545 kJ/mol
SO3(g)与H2O(l)反应的热化学方程式是 。
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。
①该电池的负极反应式 。
②电池总反应的化学方程式 。
-
(12分)铝及其化合物用途广泛。工业上焙烧明矾【KAl(SO4)2·12H2O】可得到A12O3,反应的化学方程式为4KAl(SO4)2·12H2O+3S 2K2SO4+2A12O3+9SO2↑+48H2O。
2K2SO4+2A12O3+9SO2↑+48H2O。
请回答下列问题:
(1)在焙烧明矾的反应中,被氧化和被还原的元素质量之比是________________。
(2)焙烧明矾时产生的SO2可用来制硫酸。已知25℃、10lkPa时:
①2SO2(g) +O2(g)  2SO3(g) ΔH=—197KJ/mol
2SO3(g) ΔH=—197KJ/mol
②2H2O(g)  2H2O(l)ΔH=—44KJ/mol
2H2O(l)ΔH=—44KJ/mol
③2SO2(g) +O2(g) + 2H2O(g) 2H2SO4(l)ΔH=—545KJ/mol
2H2SO4(l)ΔH=—545KJ/mol
则反应SO3(g)+ H2O(l)= H2SO4(l)ΔH=______KJ/mol。
(3)工业上利用电解熔融的A12O3制备Al,其化学方程式是_____________________;电解时阳极和阴极材料均为石墨,电解时所消耗的电极是__________(填“阳极”或“阴极”)。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液,可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。
①该电池的负极反应式为____________;②电池总反应的化学方程式为________________。
-
明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4、和H2SO4的工艺过程如下所示:
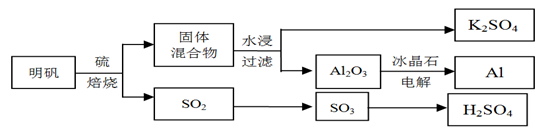
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O + 3S = 2K2SO4 + 2Al2O3 + 9SO2 + 48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是________。
(2)从水浸后的滤液中得到K2SO4晶体的方法是________。
(3)Al2O3在一定条件下可制得AlN,其晶体结构如图所示,该晶体中Al的配位数是________。
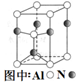
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是________。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+ O2(g) 2SO3(g) △H1 = -197 kJ /mol;
2SO3(g) △H1 = -197 kJ /mol;
H2O(g) H2O(l) △H2 = -44 kJ/mol;
H2O(l) △H2 = -44 kJ/mol;
2SO2(g)+ O2(g)+ 2H2O(g)=2H2SO4(aq) △H3 = -545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是________。
焙烧948 t明矾(M = 474 g/mol),若SO2的利用率为96%,可产生质量分数为98%的硫酸________t。
-
(15分)【化学——选修化学与技术】明矾石经处理后得到明矾[ KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
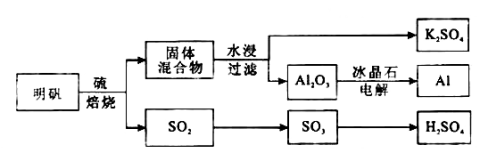
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4 +2Al2O3+9SO2+48H2O
请回答下列问题:
 (1)在焙烧明矾的反应中,还原剂是 (2分);
(1)在焙烧明矾的反应中,还原剂是 (2分);
(2)从水浸后的滤液中得到K2SO4晶体的方法是 (2分);
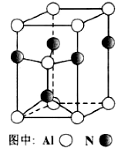
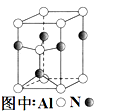
(3)A12O3在一定条件下可制得AIN,其晶体结构如图所示,该晶体中Al的配位数是 (2分);
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 (3分);
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101 kPa时:
2SO2(g) +O2(g) 2SO3(g) △H1= 一197 kJ/mol;
2SO3(g) △H1= 一197 kJ/mol;
2H2O (g)=2H2O(1) △H2=一44 kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3=一545 kJ/mol。
则SO3 (g)与H2O(l)反应的热化学方程式是 (3分);
(6)焙烧948吨明矾(M=474g/mol ),若SO2 的利用率为96%,可生产质量分数为98%的硫酸 吨(3分)。
-
【化学——选修2 化学与技术】(15分)明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4、和H2SO4的工艺过程如下所示:
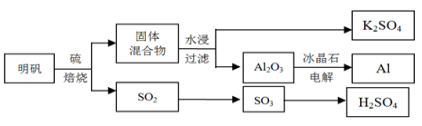
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O + 3S === 2K2SO4 + 2Al2O3 + 9SO2 + 48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是 。
(2)从水浸后的滤液中得到K2SO4晶体的方法是 。
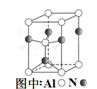
(3)Al2O3在一定条件下可制得AlN,其晶体结构如图所示,该晶体中Al的配位数是 。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+ O2(g) 2SO3(g) △H1 = -197 kJ /mol;
2SO3(g) △H1 = -197 kJ /mol;
H2O(g) H2O(l) △H2 = -44 kJ/mol;
H2O(l) △H2 = -44 kJ/mol;
2SO2(g)+ O2(g)+ 2H2O(g) 2H2SO4(aq) △H3 = -545 kJ/mol。
2H2SO4(aq) △H3 = -545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是 。
焙烧948 t明矾(M = 474 g/mol),若SO2的利用率为96%,可产生质量分数为98%的硫酸______ t。
-
明矾石经处理后得到明矾( KAl(SO4)2·12H2O)。从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
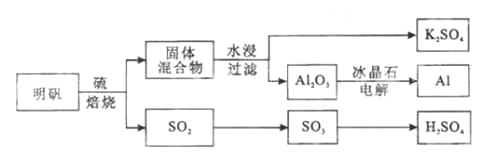
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是__________________。
(2)从水浸后的滤液中得到K2SO4晶体的方法是_____________________。
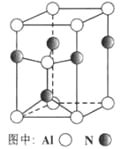
(3)A12O3在一定条件下可制得AIN,其晶体结构如右图所示,该晶体中Al的配位数是____。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是_____________________________。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101 kPa时:
2SO2(g) +O2(g) 2SO3(g) △H1= 一197 kJ/mol;
2SO3(g) △H1= 一197 kJ/mol;
2H2O (g)=2H2O(1) △H2=一44 kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3=一545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是__________________________。
焙烧948t明矾(M=474 g/mol ),若SO2的利用率为96%,可生产质量分数为98%的硫酸________t。
-
明矾石经处理后得到明矾( KAl(SO4)2·12H2O)。从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
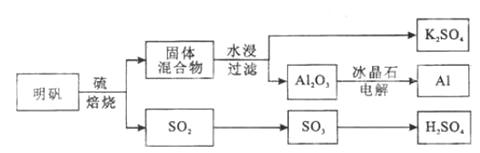
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是__________________。
(2)从水浸后的滤液中得到K2SO4晶体的方法是_____________________。
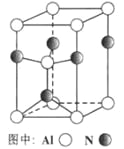
(3)A12O3在一定条件下可制得AIN,其晶体结构如右图所示,该晶体中Al的配位数是____。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是_____________________________。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101 kPa时:
2SO2(g) +O2(g) 2SO3(g) △H1= 一197 kJ/mol;
2SO3(g) △H1= 一197 kJ/mol;
2H2O (g)=2H2O(1) △H2=一44 kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3=一545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是__________________________。
焙烧948t明矾(M=474 g/mol ),若SO2的利用率为96%,可生产质量分数为98%的硫酸________t。
-
明矾石经处理后得到明矾[KAl(SO4)2•12H2O].从明矾制备Al、K2SO4、和H2SO4的工艺过程如图1所示:焙烧明矾的化学方程式为:4KAl(SO4)2•12H2O+3S═2K2SO4+2Al2O3+9SO2+48H2O
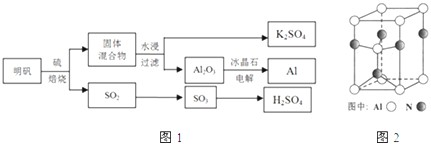
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是________.
(2)从水浸后的滤液中得到K2SO4晶体的方法是________.
(3)Al2O3在一定条件下可制得AlN,其晶体结构如图2所示,该晶体中Al的配位数是________.
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是________.
(5)焙烧产生的SO2可用于制硫酸.已知25℃、101kPa时:
2SO2(g)+O2(g)⇌2SO3(g)△H1=-197kJ/mol;
H2O(g)⇌H2O(l)△H2=-44kJ/mol;
2SO2(g)+O2(g)+2H2O(g)═2H2SO4△H3=-545kJ/mol.
则SO3(g)与H2O(l)反应的热化学方程式是________.
焙烧948t明矾(M=474g/mol),若SO2的利用率为96%,可产生质量分数为98%的硫酸________t.
-
明矾石经处理后得到明矾(KAl(SO4)2·12H2O)。由明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
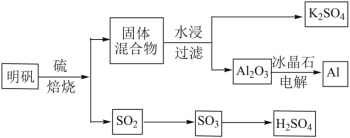
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,氧化剂和还原剂的物质的量之比为_______。
(2)从水浸后的滤液中得到K2SO4晶体的操作方法是_______。
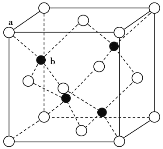
(3)A12O3在一定条件下可制得AIN,AlN的晶体结构与金刚石相似,晶胞结构如图所示。每个晶胞中含有_______个铝原子,若Al与N原子最近距离为apm,则该晶体的密度为_______g/cm3。(阿伏加德罗常数用NA表示)
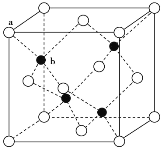
(4)SO2分子的空间构型为_______
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时
2SO2(g)+O2(g) 2SO3(g)△H1=一197kJ/mol;
2SO3(g)△H1=一197kJ/mol;
2H2O(g)=2H2O(1)△H2=一44kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是_______。
-
明矾石经处理后得到明矾(KAl(SO4)2·12H2O)。由明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
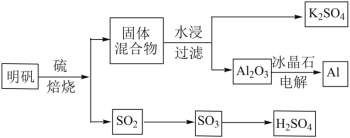
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,氧化剂和还原剂的物质的量之比为_______。
(2)从水浸后的滤液中得到K2SO4晶体的操作方法是_______。
(3)A12O3在一定条件下可制得AIN,AlN的晶体结构与金刚石相似,晶胞结构如图所示。每个晶胞中含有_______个铝原子,若Al与N原子最近距离为apm,则该晶体的密度为_______g/cm3。(阿伏加德罗常数用NA表示)
(4)SO2分子的空间构型为_______
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时
2SO2(g)+O2(g) 2SO3(g)△H1=一197kJ/mol;
2SO3(g)△H1=一197kJ/mol;
2H2O(g)=2H2O(1)△H2=一44kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是_______。
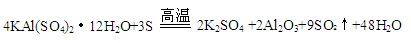
2SO3(g) △H1 = 一197 kJ/mol



 (1)在焙烧明矾的反应中,还原剂是
(1)在焙烧明矾的反应中,还原剂是










