-
某研究性学习小组做了以下实验:向溴水中加入足量乙醛溶液,观察到溴水褪色的现象。
(1)[提出问题]
产生上述现象的原因是什么?
(2)[提出猜想]
①溴水与乙醛发生取代反应。
②___________________________________________________。
③___________________________________________________。
(3)[设计方案]
方案一:检验褪色后溶液的酸碱性。
方案二:测定反应前溴水中Br2的物质的量和反应后Br-离子的物质的量。
(4)[实验探究]
取含0.005mol Br2的溶液10mL,加入足量乙醛溶液使其褪色,再加入过量AgNO3溶液,过滤、洗涤、干燥后称重固体质量为1.88g。
(5)[解释与结论]
假设测得反应前溴水中Br2的物质的量为a mol,
若测得反应后n(Br-)=0 mol,则说明溴水与乙醛发生了____________反应。
若测得反应后n(Br-)=a mol,则说明溴水与乙醛发生了____________反应。
若测得反应后n(Br-)=2a mol,则说明溴水与乙醛发生了____________反应。
若已知CH3COOAg易溶解于水,试通过计算判断溴水与乙醛发生反应的类型为___________。理由是________________________________________。
其反应的离子方程式为__________________________________________________。
(6)[反思与评价]
方案一是否可行?__________。理由是_______________________________。
高二化学实验题中等难度题查看答案及解析
-
某研究性学习小组做了以下实验:向溴水中加入足量乙醛溶液,观察到溴水褪色的现象。
[提出问题]
产生上述现象的原因是什么?
[提出猜想]
①溴水与乙醛发生取代反应。
②___________________________________________________。
③___________________________________________________。
[设计方案]
方案一:检验褪色后溶液的酸碱性。
方案二:测定反应前溴水中Br2的物质的量和反应后Br-离子的物质的量。
[实验探究]
取含0.005mol Br2的溶液10mL,加入足量乙醛溶液使其褪色,再加入过量AgNO3溶液,过滤、洗涤、干燥后称重固体质量为1.88g。
[解释与结论]
假设测得反应前溴水中Br2的物质的量为a mol,
若测得反应后n(Br-)=0mol,则说明溴水与乙醛发生了____________反应。
若测得反应后n(Br-)=amol,则说明溴水与乙醛发生了____________反应。
若测得反应后n(Br-)=2amol,则说明溴水与乙醛发生了____________反应。
若已知CH3COOAg易溶解于水,试通过计算判断溴水与乙醛发生反应的类型为___________。
理由是__________________________________________________________。
其反应方程式为_______________________________________________________。
[反思与评价]
方案一是否可行?__________。理由是_______________________________________。
高二化学填空题极难题查看答案及解析
-
某学习小组做以下实验:在溴水中加入足量乙醛溶液,充分反应,溴水褪色;为探究褪色的原因,他们提出了如下猜想:
①溴水中的Br2可能与乙醛发生取代反应,产生HBr;
②乙醛分子中含有不饱和键,溴水可能与乙醛发生加成反应;
③乙醛具有还原性,溴水可能将乙醛氧化为乙酸,Br2转化为HBr.
设计如下方案进行探究:
方案(一):检验褪色后溶液的酸碱性,确定其发生哪类反应;
方案(二):测定反应前溴水中Br2的物质的量和反应后 Br-的物质的量确定其发生哪类反应;
(1)假设测得反应前溴水中Br2的物质的量为a mol,
若测得反应后n(Br-)=0mol,说明溴水与乙醛发生了______反应;
若测得反应后n(Br-)=a mol,说明溴水与乙醛发生了______反应;
若测得反应后n(Br-)=2a mol,说明溴水与乙醛发生了______反应.
(2)向含Br2 0.005mol的溴水中加入足量乙醛使其褪色,然后加过量的AgNO3溶液,过滤、洗涤、干燥、称量,得到固体1.88g.已知CH3COOAg易溶于水,通过计算,判断溴水与乙醛发生的反应为______(填序号):①氧化反应 ②取代反应 ③加成反应
(3)方案(一)是否可行?______ (填“是”或“否”),原因是:______.高二化学解答题中等难度题查看答案及解析
-
(8分)某学习小组做以下实验:在溴水中加入足量乙醛溶液,充分反应,溴水褪色;为探究褪色的原因,他们提出了如下猜想:
①溴水中的Br2可能与乙醛发生取代反应,产生HBr;
②乙醛分子中含有不饱和键,溴水可能与乙醛发生加成反应;
③乙醛具有还原性,溴水可能将乙醛氧化为乙酸,Br2转化为HBr
设计如下方案进行探究:
方案(一):检验褪色后溶液的酸碱性,确定其发生哪类反应;
方案(二):测定反应前溴水中Br2的物质的量和反应后 Br-的物质的量确定其发生哪类反应; 反应类型选项有:①氧化反应 ②取代反应 ③加成反应
(1) 假设测得反应前溴水中Br2的物质的量为a mol,
i若测得反应后n(Br-)= 0 mol, 说明溴水与乙醛发生了________反应;(从上面提供的反应类型选项中选择,然后将序号写在答题纸上,下同)
ii若测得反应后n(Br-) = a mol,说明溴水与乙醛发生了________反应;
iii若测得反应后n(Br-)= 2a mol,说明溴水与乙醛发生了________反应。
(2)向含Br2 0.005mol的溴水中加入足量乙醛使其褪色,然后加过量的AgNO3溶液,过滤、洗涤、干燥、称量,得到固体1.88克。已知CH3COOAg易溶于水,通过计算,判断溴水与乙醛发生的反应为________(填序号): ①氧化反应 ②取代反应 ③加成反应
(3)方案(一)是否可行?______________ , 原因是:________
高二化学实验题简单题查看答案及解析
-
某学习小组做以下实验:在溴水中加入足量乙醛溶液,充分反应,溴水褪色。为探究褪色的原因,他们提出了如下三种猜想:
①溴水中的Br2可能与乙醛发生取代反应
②乙醛分子中含有不饱和键,溴水可能与乙醛发生加成反应
③乙醛具有还原性,溴水可能将乙醛氧化为乙酸,Br2转化为HBr
为探究哪一种猜想正确,一研究小组提出了如下两种方案:
方案(一):检验褪色后溶液的酸碱性,确定其发生哪类反应
方案(二):测定反应前溴水中Br2的物质的量和反应后 Br-的物质的量确定其发生哪类反应
(1)方案(一)是否可行?______ (填“可行”或“不可行”) ;理由是:________
(2)假设测得反应前溴水中Br2的物质的量为a mol,
若测得反应后n(Br-)=________mol, 则说明溴水与乙醛发生了取代反应
若测得反应后n(Br-)=________mol,则说明溴水与乙醛发生了加成反应
若测得反应后n(Br-)=________mol,则说明溴水将乙醛氧化为乙酸
(3)向含Br2 0.005mol的溴水中加入足量乙醛使其褪色,然后加过量的AgNO3溶液,过滤、洗涤、干燥、称量,得到固体1.88克。已知CH3COOAg易溶于水,通过计算,判断溴水与乙醛发生的反应为________(填猜想序号),溴水与乙醛反应的化学方程式为________
(4)已知柠檬醛的结构简式为
 ,若要检验出其中的碳碳双键,其方法是 ________。
,若要检验出其中的碳碳双键,其方法是 ________。高二化学实验题困难题查看答案及解析
-
向草酸(H2C2O4)溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色总是先慢后快。对其原因,某研究性学习小组结合化学反应原理提出猜想与假设,并设计了一系列实验进行探究:
实验(1):在两支试管中分别加入10mL等浓度的草酸溶液,在②号试管中加入少量硫酸锰固体。然后在两支试管中分别加入5滴0.1 mol·L-1的硫酸酸化高锰酸钾溶液。现象如下(表1)
①号试管
②号试管
加入药品
草酸溶液
硫酸酸化高锰酸钾溶液
草酸溶液
硫酸酸化高锰酸钾溶液
硫酸锰固体
实验现象(褪色时间)
溶液褪色很慢(30s)
溶液褪色很快(2s)
实验(2):在两支试管中分别加入5 mL等浓度的草酸溶液,在②号试管中再滴加10滴稀硫酸,然后各加入5滴0.1 mol·L-1的高锰酸钾溶液。现象如下(表2)
编号
①号试管
②号试管
褪色时间
现象
100 s
90 s
均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。
实验(3):取3支试管分别加入5 mL等浓度草酸溶液,然后在①、②、③号试管中依次加入10滴、1 mL、2 mL稀硫酸溶液,各加入5滴0.1 mol·L-1的高锰酸钾溶液,然后置于温度为65℃的水浴中加热。观察现象(表3)。
编号
①号试管
②号试管
③号试管
褪色时间
实验现象
80 s
100 s
120 s
均有气泡产生;①号试管的溶液褪色比②、③号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。
(1) 该研究性学习小组的实验目的是________。
(2)该研究性学习小组进行实验时所用的方法是科学实验中常用的一种方法,该方法叫________法;
(3)实验(1)得出的结论是________。
(4)由实验(2)和实验(3)得出的结论是(写三点)
_________________________,_____________________,_______________;
(5)据有关现象写出草酸溶液与酸性高锰酸钾溶液反应的离子方程式:
________H2C2O4+________MnO4—+ ________ ________=________Mn2++ ________ ________+ ________H2O
高二化学填空题简单题查看答案及解析
-
向溴水中加入足量的乙醛溶液,可以看到溴水褪色,对产生该现象的原因有如下三种猜想:①溴水与乙醛发生取代反应;②由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应;③由于乙醛具有还原性,溴水将乙醛氧化为乙酸。为探究哪种猜想正确,一研究性学习小组提出了如下两种实验方案:
方案一:检验褪色后溶液的酸碱性;
方案二:测定反应前溴水中 Br2 的物质的量和反应后溶液中 Br—离子的物质的量。
(1)方案一是否可行__________填(“是”或“否”),理由是____________________。
(2)假设测得反应前溴水中 Br2 的物质的量为 amol,
若测得反应后 n(Br-)=__________mol,则说明溴水与乙醛发生取代反应;
若测得反应后 n(Br-)=__________mol,则说明溴水与乙醛发生加成反应;
若测得反应后 n(Br-)=__________mol,则说明溴水将乙醛氧化为乙酸。
(3)按物质的量之比为 1︰5 配制 1000mLKBrO3-KBr 溶液,该溶液在酸性条件下完全反应可生成 0.5molBr2。取该溶液 10mL 加入足量乙醛溶液,使其褪色,然后将所得溶液稀释为 100mL,准确量取其中 10mL,加入过量的 AgNO3 溶液,过滤、洗涤、干燥后称量得到固体 0.188g。若已知 CH3COOAg 易溶于水,试通过计算判断溴水与乙醛发生反应的类型为__________(选填猜想序号)。
(4)写出上述测定过程中的三个反应的离子方程式:
①KBrO3 和KBr 在酸性条件下的反应:______________________________;
②溴水与乙醛的反应:______________________________;
③测定 Br-离子含量的反应:______________________________;
高二化学实验题简单题查看答案及解析
-
某实验小组学习过氧化钠与水的反应时,向滴有酚酞的水中加入过氧化钠,发现溶液先变红后褪色,对此产生兴趣并进行研究。
(1)写出Na2O2与水反应的化学方程式:______。
(2)甲同学查阅资料:红色褪去的原因是H2O2在碱性条件下氧化了酚酞。
①甲同学通过实验证实了Na2O2与水反应所得溶液中有较多的H2O2:取少量反应所得溶液,加入试剂______(填化学式),有气体产生。
②甲同学利用3% H2O2溶液、酚酞试液、1mol·L-1 NaOH溶液,证实了碱性条件是必需的。
操作
现象
实验1
向2mL 3%H2O2溶液中加入3滴酚酞试液,振荡,静置5min,再加入5滴1mol·L-1 NaOH溶液
观察到______。
(3)为了更深入地了解该原理,甲同学继续查阅资料,发现H2O2溶液中相关微粒的物质的量分数X(i)与溶液pH的关系如图所示。
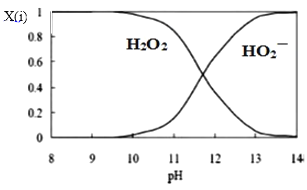
据此,甲同学设计实验2继续研究:
操作
现象
实验2
i.配制20mL 3%H2O2与NaOH的混合溶液,调节pH分别为10~14。
ii.滴入3滴酚酞试液,搅拌后静置,记录酚酞完全褪色的时间
得到如图所示实验结果:
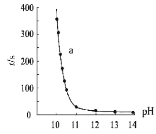
甲同学由此提出假设I:溶液褪色的主要原因是酚酞被HO
氧化,请结合化学反应速率和化学平衡的相关知识解释此假设:_____。
(4)乙同学查阅资料,发现酚酞(以H2L表示)在不同pH条件下存在多种结构之间的变化:
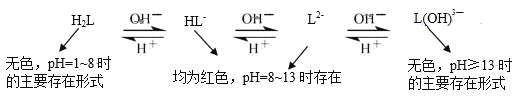
由此提出,甲同学实验2中pH˃13时红色褪去的原因还存在假设II:_____。
(5)针对假设I、II,小组同学设计了如下实验:
试剂加入顺序
现象
实验3
i.烧杯中加入10mL 2mol·L-1 NaOH溶液、8mL H2O
ii.加入3滴酚酞试液
溶液变红,然后褪色
iii.搅拌、静置后加入2mL 30% H2O2溶液
_____
iv.向褪色后的溶液中加入盐酸调节pH至12
溶液变红,然后褪色
实验4
i.烧杯中加入10mL 2mol·L-1 NaOH溶液、8mL H2O
ii.加入2mL 30% H2O2溶液
iii.搅拌、静置后加入3滴酚酞试液
溶液变红,然后褪色
iv.向褪色后的溶液中加入盐酸调节pH至12
不变红
①与L2-和HL-相比较,L(OH)
比前两者更_____被氧化(填“难”或“易”)。
②实验3中调节pH至12,溶液变红然后褪色的原因是:_____。
③根据实验得出结论:甲同学实验2中pH˃13时红色褪去的主要原因是_____(填“假设I”或“假设II”),请依据实验现象阐述理由:_____。
高二化学实验题简单题查看答案及解析
-
某化学实验兴趣小组在“探究氯水与溴化亚铁溶液反应”的实验中发现:“在足量的溴化亚铁溶液中,加入1~2滴氯水,振荡后溶液呈黄色。”
根据已有化学知识及资料,请你对上述现象形成原因进行分析与探究:
(1)提出问题猜想:
溶液呈黄色是因发生离子反应① 2Fe2+ + Cl2 = 2Fe3+ + 2Cl- 所致。
溶液呈黄色是因发生离子反应②_______________________(填离子方程式)所致。
(2)设计实验并验证
为验证①与②中是哪个原因导致了溶液变黄色,设计并进行了以下实验。请根据以下所给试剂,进行合理选用,完成实验方案1和方案2:
试剂
酚酞试液.CCl4.无水酒精.KSCN溶液
方案
操作步骤
实验现象
结论
1
取所述黄色溶液于试管中,滴加_______并振荡
溶液变红色
____________
2
取所述黄色溶液于试管中,滴加_______并振荡
________________
(同上)
(3)实验结论:以上实验不仅验证了溶液变黄的真实原因,同时证明了Fe2+的还原性比Br-______________(填“强”.“弱”. “几乎一致”)。
高二化学综合题中等难度题查看答案及解析
-
某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目:
方案Ⅰ:有人提出将大小相等的铁片和铜片,分别同时放入稀硫酸(或稀盐酸)中,观察产生气泡的快慢,据此确定它们的活动性。该原理的离子方程式为___________________。
方案Ⅱ:有人利用Fe、Cu作电极设计成原电池,以确定它们的活动性。试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出电极反应式。
正极反应式:____________________。
负极反应式:____________________。
方案Ⅲ:结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案(与方案Ⅰ、Ⅱ不能雷同):________________,用离子方程式表示其反应原理:_____________________。
高二化学实验题困难题查看答案及解析