-
某同学称取了4.0 gNaOH固体,欲配制100 mL溶液。回答下列问题:
(1)该实验中,用到的能确定体积的两种玻璃仪器是________、________。
(2)操作过程中多次用到玻璃棒,其在实验中的作用有_____。
(3)不规范的实验操作会导致实验结果的误差。分析下列操作对实验结果的影响(填“偏大”、“偏小”或“不变”):
①在溶解过程中有少量液体溅出烧杯外________;
②定容时仰视仪器上的刻度线________;
③定容后,将容量瓶振荡摇匀后,静置发现液面低于刻度线,于是又加入少量水至刻度线________。
(4)最后所得的溶液应存放在试剂瓶中,并贴上标签,请你填写该标签(如图)。
-
下列有关实验原理或实验操作正确的是
A.将氯化铁固体溶于稀盐酸配制FeCl3溶液
B.称取4.0gNaOH,放入100mL容量瓶中,加水稀释,配制1.0mol·L-1的NaOH溶液
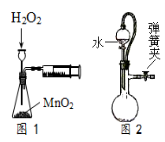
C.利用图1装置定量测定H2O2的分解速率
D.如图2所示,关闭弹簧夹检查装置的气密性
-
下列实验数据记录或实验方法正确的是( )
A.用天平称取4.0gNaOH固体,用100mL量筒配制1.00mol/L的NaOH溶液100mL
B.用25mL的滴定管(内装有标准NaOH溶液)滴定未知浓度的盐酸用去NaOH溶液15mL
C.用pH试纸测得新制氯水的pH为4
D.用250mL容量瓶配制250mL0.2mol/L的NaOH溶液
-
下列有关实验原理或实验操作正确的是( )
A.称取4.0gNaOH,放入100mL容量瓶中,配制1.0mol/L的NaOH溶液
B.将氯化铁固体溶于稀盐酸配制FeCl3溶液
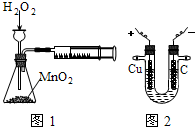
C.利用图1装置定量测定H2O2的分解速率
D.利用图2装置模拟工业上电解饱和食盐水
-
下列实验数据记录和实验方法正确的是( )
A.用天平称取4.0gNaOH固体,用100mL量筒配制1.00mol/L的NaOH溶液
B.用25mL的滴定管(内装有标准NaOH溶液)滴定未知浓度的盐酸用去NaOH溶液22.32mL
C.用pH试纸测得新制氯水的pH为4
D.常温下,用气球收集500mLNO2气体,求得NO2气体的物质的量为(0.5/22.4)mol
-
某班同学用如下实验探究 Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成 100mL 0.1mol/L 的溶液.配制过 程中所需要的玻璃仪器有量筒、玻璃棒、烧杯、________________、____________________ ,配制氯化亚 铁溶液时所用溶剂需除去溶解其中的氧,除去水中氧的简单操作为__________,用饱和氯 化铁溶液制备 Fe(OH)3 胶体的离子方程式为________________________________________________。
(2)甲组同学取 2mL FeCl2 溶液,先加入 1 滴 KSCN 溶液,无现象,再加入几滴氯水, 溶液变 红,说明 Cl2 可将 Fe2+氧化。FeCl2 溶液与氯水反应的离子方程式为_____。
(3)乙组同学认为甲组的实验不够严谨,该组同学在 2mLFeCl2 溶液中先加入 0.5mL 煤 油,再于液面下依次加入 l 滴 KSCN 溶液和几滴氯水,溶液变红,煤油的作用是_____。
(4)丙组同学取 10 mL 0.1mol/LKI 溶液,加入 6mL 0.1mol/LFeCl3 溶液混合。分别取
2mL 此溶 液于 3 支试管中进行如下实验:
① 第一支试管中加入 1mLCCl4 充分振荡、静置,CCl4 层呈紫色 ;在水层中加入硝酸酸化 的硝酸银溶液,有黄色沉淀生成;
② 第二只试管中加入 1 滴铁氰化钾溶液,生成蓝色沉淀;
③ 第三支试管中加入 1 滴 KSCN 溶液,溶液变红。 实验②的离子方程式为_____________; 实验①和③说明:在I-过量的情况下,溶液中仍含有_____(填离子符号),由此可以证 明该氧化还原反应为_____。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发 生反应的离子方程式为_____;一段时间后.溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是_____;生成沉淀的原因是_____(用平衡移动原理解释)。
-
实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题
(1)根据计算,需称取氯化钠 g。
(2)配制时,必须用到的玻璃仪器有 。
(3)配制溶液有下列几步操作:a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,f.将溶液移至容量瓶,g.贴标签,h.定容。正确的操作顺序是 。
(4)下列操作结果使溶液物质的量浓度偏低的是 。
A.没有将洗涤液转入容量瓶中 B.容量瓶洗涤后,未经干燥处理
C.定容时,俯视容量瓶的刻度线 D.加水定容时,水的量超过了刻度线
-
实验室要用NaOH固体配制100mL 2 mol·L-1的NaOH溶液,试回答下列各题:
(1)下列仪器中,一定不会用到的是___________
A锥形瓶 B量筒 C胶头滴管 D100mL容量瓶 E托盘天平
(2)若要实施配制,除上述仪器外,尚缺的玻璃仪器或用品是_______________。
(3)人们常将配制过程简述为以下各步骤:
A冷却 B称量 C洗涤 D定容 E溶解 F摇匀 G转移溶液
其正确的操作顺序应是___________________ __(填各步骤序号)。
(4)下列操作会导致所配制的溶液浓度偏高的是_____
| A.定容时仰视容量瓶刻度线 |
| B.容量瓶中有少量水 |
| C.未冷却定容 |
| D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处 |
(5)需用托盘天平称量NaOH________克
-
下列实验操作规范且能达到相应实验目的的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 配制100g4%的NaOH溶液 | 称取4.0gNaOH放在烧杯中,再加入96.0mL水,搅拌均匀 |
| B | 证明铜与浓硫酸反应生成硫酸铜 | 向反应后并冷却的试管中加入适量的水,溶液变蓝 |
| C | 证明Ksp(BaSO4)<Ksp(BaCO3) | 向BaCO3悬浊液中加入饱和Na2SO4溶液 |
| D | 检验Al和Fe2O3反应后固体中是否含Fe2O3 | 取样,溶于足量稀硫酸,滴加KSCN溶液不变红,说明不含Fe2O3 |
A.A B.B C.C D.D
-
(18分)某同学欲配制450mL 0.1mol/L的碳酸钠溶液,试根据所学回答下列问题。
(1)若采用5mol/L的碳酸钠溶液配制溶液,需要用到碳酸钠溶液的体积为________。
(2)若用碳酸钠固体配制,一定会用到的仪器有________________________
A.450ml容量瓶 B.500 ml容量瓶 C.量筒 D.胶头滴管
E.烧杯 F.玻璃棒 G.托盘天平
(3)欲准确配制所需溶液,下列称量质量正确的是 ( )
A.称Na2CO3 4.8克 B.Na2CO3 5.3克
C.称Na2CO3·10H2O 12.87克 D.称Na2CO3·10H2O 14.30克
(4)若在配溶液的过程中用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是________(填序号)。
A.吸出多余液体,使凹液面与刻度线相切
B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
C.经计算加入一定量的碳酸钠固体
D.重新配制
(5)下列操作可能导致结果偏高的是________。
A.转移后没有洗涤烧杯
B.定容时俯视
C.定容时仰视
D.称取的Na2CO3 溶液中混有少量Na2CO3·10H2O
E.配溶液前用碳酸钠溶液润洗容量瓶


