| 组别 | 对应曲线 | c(HCl)/mol•L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |
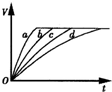
A.第4组实验的反应速率最慢
B.第1组实验中盐酸的浓度大于2.5 mol•L-1
C.第2组实验中盐酸的浓度小于2.5 mol•L-1
D.第3组实验的反应温度低于30℃
高三化学选择题中等难度题
| 组别 | 对应曲线 | c(HCl)/mol•L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |

高三化学选择题中等难度题
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得不同时间(t)内产生气体体积(V)的数据如图,根据图示分析实验条件,下列说法中一定不正确的是( )
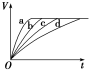
| 组合 | 对应曲线 | c(HCl)/mol·L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |
A.第1组实验中盐酸的浓度大于2.5 mol·L-1
B.第2组实验中盐酸的浓度等于2.5 mol·L-1
C.第3组实验的反应温度低于30 ℃
D.第4组实验的反应速率最慢
高三化学选择题中等难度题查看答案及解析
| 组别 | 对应曲线 | c(HCl)/mol•L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |

高三化学选择题中等难度题查看答案及解析
等质量的碳酸钙与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如下图所示,根据图示分析实验条件,下列说法中一定不正确的是( )
| 组别 | 对应曲线 | c(HCl) / mol·L-1 | 反应温度 / ℃ | 铁的状态 |
|
| 1 | a | 30 | 粉末状 | ||
| 2 | b | 30 | 粉末状 | ||
| 3 | c | 2.5 | 块状 | ||
| 4 | d | 2.5 | 30 | 块状 |
A.第4组实验的反应速率最慢
B.第1组实验中盐酸的浓度可能最大
C.第2组实验中盐酸浓度可能等于2.5mol/L
D.第3组实验的反应温度低于30 ℃
高三化学单选题中等难度题查看答案及解析
等质量的碳酸钙与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如下图所示,根据图示分析实验条件,下列说法中一定不正确的是( )
| 组别 | 对应曲线 | c(HCl) / mol·L-1 | 反应温度 / ℃ | 铁的状态 |
|
| 1 | a | 30 | 粉末状 | ||
| 2 | b | 30 | 粉末状 | ||
| 3 | c | 2.5 | 块状 | ||
| 4 | d | 2.5 | 30 | 块状 |
A. 第4组实验的反应速率最慢
B. 第1组实验中盐酸的浓度可能最大
C. 第2组实验中盐酸浓度可能等于2.5mol/L
D. 第3组实验的反应温度低于30 ℃
高三化学选择题中等难度题查看答案及解析
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得图,则曲线a、b、c、d所对应的实验组别可能是( )
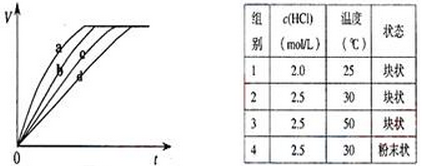
A.4-3-2-1 B.1-2-3-4
C.3-4-2-1 D.1-2-4-3
高三化学选择题中等难度题查看答案及解析
(8分)标准状况下,进行甲、乙、丙三组实验,各取30.0 mL相同浓度的盐酸,然后分别慢慢地加入不同质量的同一种镁铝合金粉末,得下列有关数据(假设反应前后溶液的体积不发生变化):
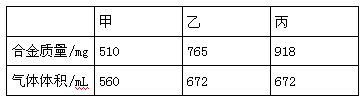
根据实验数据,计算:
(1)盐酸中HCl的物质的量浓度为_____________。
(2)合金中镁的质量分数(计算结果保留至0.1%,有必要的计算步骤和语言叙述,只写答案不得分,下同)。
(3)甲组实验后,还需向容器中加入lmol·L-1的NaOH溶液多少毫升恰好使铝元素以[Al(OH)4]-存在,并使Mg2+刚好沉淀完全?
高三化学填空题中等难度题查看答案及解析
某小组通过分析镁与酸反应时pH的变化,探究镁与醋酸溶液反应的实质。
(实验)在常温水浴条件下,进行实验Ⅰ~Ⅲ,记录生成气体体积和溶液pH的变化:
Ⅰ.取0.1 g光亮的镁屑(过量)放入10 mL 0.10 mol·L–1 HCl溶液中;
Ⅱ.取0.1 g光亮的镁屑放入10 mL 0.10 mol·L–1 CH3COOH溶液(pH = 2.9)中;
Ⅲ.取0.1 g光亮的镁屑放入10 mL pH = 2.9 HCl溶液中。
(数据)
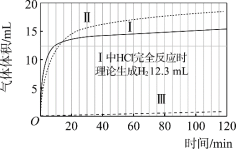

图1 图2
(1)起始阶段,Ⅰ中主要反应的离子方程式是____。
(2)Ⅱ起始溶液中约为____。(选填“1”、“10”或“102”)
(3)起始阶段,导致Ⅱ、Ⅲ气体产生速率差异的主要因素不是c(H+),实验证据是____。
(4)探究Ⅱ的反应速率大于Ⅲ的原因。
提出假设:CH3COOH能直接与Mg反应。
进行实验Ⅳ:____。
得出结论:该假设成立。
(5)探究醋酸溶液中与Mg反应的主要微粒,进行实验Ⅴ。
与Ⅱ相同的条件和试剂用量,将溶液换成含0.10 mol·L–1的 CH3COOH与0.10 mol·L–1 CH3COONa的混合溶液(pH = 4.8),气体产生速率与Ⅱ对比如下。
| a.实验Ⅴ起始速率 | b.实验Ⅱ起始速率 | c.实验ⅡpH=4.8时速率 |
| 2.1 mL·min–1 | 2.3 mL·min–1 | 0.8 mL·min–1 |
对比a~c中的微粒浓度,解释其a与b、a与c气体产生速率差异的原因:____。
(6)综合以上实验得出结论:
①镁与醋酸溶液反应时,CH3COOH、H+、H2O均能与镁反应产生氢气;
②____。
(7)实验反思:120 min附近,Ⅰ~ⅢpH均基本不变,pH(Ⅰ) ≈ pH(Ⅱ) < pH(Ⅲ),解释其原因:____。
高三化学实验题困难题查看答案及解析
将一定质量的钠、钾分别投入盛有相同浓度和体积的盐酸盐酸过量
的两个烧杯中,产生的气体的质量随时间变化曲线如图所示,则下列说法正确的是
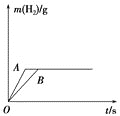
A.投入的Na、K的质量一定相等
B.投入的Na的质量大于K的质量
C.曲线A表示Na与盐酸反应,曲线B表示K与盐酸反应
D.该实验能证明K的金属性比钠的强
高三化学单选题中等难度题查看答案及解析
在标准状况下进行下列实验,各取30.0 mL同浓度的盐酸,加入同一种镁铝合金的粉末产生气体,有关数据如表所示:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(mg) | 255 | 385 | 459 |
| 标准状况下气体的体积(mL) | 280 | 336 | 336 |
下列说法正确的是
A.甲、乙组的实验中,盐酸均是过量的
B.盐酸的物质的量浓度为0.8 mol·L-1
C.合金中镁、铝的物质的量之比为1∶1
D.丙组中铝的物质的量为0.0045mol
高三化学选择题困难题查看答案及解析
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 770 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
高三化学选择题中等难度题查看答案及解析