-
银锌电池(钮扣式电池)的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-=ZnO+H2O;
Ag2O+H2O+2e- = 2Ag+2OH- ;总反应为:Ag2O+Zn=2Ag+ZnO,下列判断正确的是( )
A、锌为正极,Ag2O为负极 B、锌为负极,Ag2O为正极
C、原电池工作时,正极区PH减小 D、原电池工作时,负极区PH增大
高二化学选择题简单题查看答案及解析
-
银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH- ;总反应为:Ag2O+Zn=2Ag+ZnO,下列判断正确的是( )
A.锌为正极,Ag2O为负极; B.锌为阳极,Ag2O为阴极;
C.原电池工作时,负极区pH减小; D.原电池工作时,负极区pH增大;
高二化学选择题简单题查看答案及解析
-
银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH- ;总反应为:Ag2O+Zn=2Ag+ZnO,下列判断正确的是( )
A.锌为正极,Ag2O为负极 B.锌为阳极,Ag2O为阴极
C.原电池工作时,负极区PH减小 D.原电池工作时,负极区PH增大
高二化学选择题简单题查看答案及解析
-
(6分)常见的纽扣式电池为银锌电池。它用不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒内靠正极壳一端填充由Ag2O和少量石墨组成的正极活性材料,负极盖一端填充锌汞合金作负极活性材料,电解质溶液为浓KOH,溶液两边用羧甲基纤维素作隔膜。锌银电池的负极是Zn,正极是Ag2O,电解质是KOH,其总的反应式为:
Zn+Ag2O=2Ag+ZnO。
(1)写出正、负极的电极反应式:负极:________。
正极:________。
(2)电池工作过程中,电池负极溶液的PH________(填“增大”、“减小”或“不变”)
高二化学填空题中等难度题查看答案及解析
-
钮扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液。放电时两个电极反应分别为Zn+2OH--2e-=Zn(OH)2、Ag2O+H2O+2e-=2Ag+2OH-,下列说法中,正确的是( )
A.锌是负极,氧化银是正极
B.锌发生还原反应,氧化银发生氧化反应
C.溶液中OH-向正极移动,K+、H+向负极移动
D.在电池放电过程中,电解质溶液的酸碱性基本保持不变
高二化学单选题简单题查看答案及解析
-
电子计算机所用钮扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是: Zn + 2OH- -2e-==ZnO + H2O Ag2O +H2O + 2e-==2Ag +2 OH- ,下列判断正确的是
A. 锌为正极,Ag2O为负极 B. 锌为负极,Ag2O为正极
C. 原电池工作时,正极区溶液pH减小 D. 原电池工作时,负极区溶液pH增大
高二化学选择题中等难度题查看答案及解析
-
电子计算机所用钮扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是: Zn + 2OH- -2e-==ZnO + H2O Ag2O +H2O + 2e-==2Ag +2 OH- ,下列判断正确的是
A.锌为正极,Ag2O为负极 B.锌为负极,Ag2O为正极
C.原电池工作时,正极区溶液pH减小 D.原电池工作时,负极区溶液pH增大
高二化学选择题简单题查看答案及解析
-
(12分)
(1)以甲烷、空气、氢氧化钾溶液为原料,石墨为电极可以构成燃料电池。该电池的负极反应式为。
(2)用如图所示装置进行电解①若A、B均为石墨电极,C为足量CuS04溶液,则电解的总反应方程式为________。

电解一段时间后,取出电极,向电解液中加入适量的________(填化学式)可使C溶液恢复到电解前的成分和浓度。
②若A、B均为铂电极,C为Na2SO4溶液(含酚酞),电解一段时间后,________(填“A”或“B”)极附近显红色;将电极取出,搅拌使溶液混合均匀,测得溶液的pH ________7(填“<”、“=”或“>”)。
③若A、B为同一材料的电极,C为CuCl2溶液,电解过程中CuCl2溶液的浓度始终 保持不变,则A、B为________(填化学式)电极;当电路中有0.04 mol电子通过时,阴极增重(________) g。
高二化学填空题简单题查看答案及解析
-
某原电池的总反应为2H2+O2=2H2O,两电极材料都是石墨,氢氧化钾为电解质溶液,下列说法不正确的是
A. 氧气在正极发生还原反应 B. 负极反应式为H2-2e-+2OH-=2H2O
C. 该电池工作一段时间后电解质溶液中c(OH-)变大 D. 若正极消耗的气体质量为4克,则转移的电子的物质的量为0.5mol
高二化学选择题中等难度题查看答案及解析
-
右图1为甲烷和O2构成的燃料电池示意图,电解质溶液为KOH溶液,图2为电解AlCl3溶液的装置,电极材料均为石墨。用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。下列说法正确的是
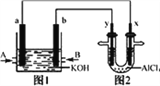
A. 图2中Y电极为阴极
B. 图2中总反应的化学方程式为:2AlCl3+6H2O
2Al(OH)3↓+3Cl2↑+3H2↑
C. 图1中电解质溶液的pH增大
D. 图1中的a 电极反应式为:CH4-8e-+8OH-=CO2+6H2O
高二化学单选题中等难度题查看答案及解析