-
溴是海水中重要的非金属元素,地球上90%的溴元素以Br-的形式存在于海水中,所以人们称溴为“海洋元素”。下列有关说法中正确的是
A.从海水中提取溴时,不涉及氧化还原反应
B.苯与溴水反应生成溴苯
C.可以用CCl4萃取溴水中的溴
D.向FeBr2溶液中通入Cl2时,一定会发生如下反应:
2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
高三化学选择题中等难度题查看答案及解析
-
【化学--化学与技术】
溴是海水中重要的非金属元素,地球上99%的溴元素以Br-的形式存在于海水中,因此溴被称为“海洋元素”.目前,从海水中提取溴是世界各国生产溴的主要方法,其工艺流程如下:
请回答下列问题:
(1)写出步骤①中反应的离子方程式________.
(2)步骤③在________ (填设备名称)中完成,反应的化学方程式为________.
(3)在步骤⑤蒸馏的过程中,温度控制在80℃~90℃,温度过高或过低于不利于生产,其原因是________.
(4)溴单质在四氯化碳中的溶解度比在水中大得多,四氯化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氯化碳,原因是________.
高三化学填空题中等难度题查看答案及解析
-
下列叙述不正确的是( )
A.地球上99%的溴元素以溴单质形式存在于海洋中
B.在每升海水中含量低于1mg的元素称为海水中的微量元素
C.海水是锂元素的一个重要来源
D.世界上生产的镁大部分来自海水高三化学选择题中等难度题查看答案及解析
-
下列叙述不正确的是( )。
A.地球上99%的溴元素以溴单质形式存在于海洋中
B.在每升海水中含量低于1 mg的元素称为海水中的微量元素
C.海水是锂元素的一个重要来源
D.世界上生产的镁大部分来自海水
高三化学选择题简单题查看答案及解析
-
CO2的转换在生产、生活中具有重要的应用。
(1)CO2的低碳转型对抵御气候变化具有重要意义,海洋是地球上碳元素最大的“吸收池”。
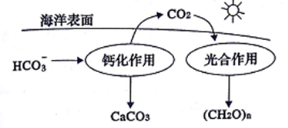
①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为_________、___________________。
②在海洋碳循环中,可通过上图所示的途径固碳。写出钙化作用的离子方程式:____________。
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2
2Na2CO3+C。放电时,在正极得电子的物质为___________;充电时,阳极的反应式为___________。
(3) 目前工业上有一种方法是用CO2和H2在230℃并有催化剂条件下转化生成甲醇蒸汽和水蒸气。下图表示恒压容器中0.5molCO2和1.5 mol H2转化率达80%时的能量变化示意图。能判断该反应达到化学平衡状态的依据_______(填字母)。
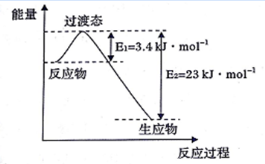
a.容器中压强不变 b.H2的体积分数不变
c.c(H2 =3c(CH3OH) d.容器中密度不变
e. 2个C = O断裂的同时有6个H - H断裂
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)
CO2(g) +H2(g),得到如下三组数据:
实验组
温度/℃
起始量/mol
平衡量/mol
达到平衡所
需时间/min
CO
H2O
H2
CO
1
650
4
2
1.6
2.4
6
2
900
2
1
0.4
1.6
3
3
900
a
b
c
d
t
①实验2条件下平衡常数K=____________。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值_________ (填具体值或取值范围)。
③ 实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时v(正____v(逆)(填“ <”、“ >”或“=")。
(5)已知在常温常压下:
①2CH3OH(I) +3O2(g)=2CO2(g) +4H2O(g) △H= -1275.6 kJ • mol-1
②2CO(g) +O2(g)=2CO2(g) △H = -566.0 kJ·mol-1
③H2O(g)=H2O(I) △H =-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式_____________。
高三化学简答题中等难度题查看答案及解析
-
CO2的转换在生产、生活中具有重要的应用。
Ⅰ.CO2的低碳转型对抵御气候变化具有重要意义。
(1)海洋是地球上碳元素的最大“吸收池”。
①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为____________。
②在海洋碳循环中,可通过下图所示的途径固碳。写出钙化作用的离子方程式:_____________。
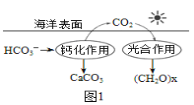
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2
2Na2CO3+C。放电时,在正极得电子的物质为______;充电时,阳极的反应式为_____。
Ⅱ.环境中的有害物质常通过转化为CO2来降低污染。
(3)TiO2是一种性能优良的半导体光催化剂,能有效地将有机污染物转化为CO2等小分子物质。下图为在TiO2的催化下,O3降解CH3CHO的示意图,则该反应的化学方程式为____。
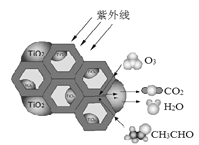
(4)用新型钛基纳米PbO2作电极可将苯、酚类等降解为CO2 和H2O。该电极可通过下面过程制备:将钛基板用丙酮浸泡后再用水冲洗,在钛板上镀上一层铝膜。用它做阳极在草酸溶液中电解,一段时间后,铝被氧化为氧化铝并同时形成孔洞。再用Pb(NO3)2溶液处理得纳米PbO2,除去多余的氧化铝,获得钛基纳米PbO2电极。
①用丙酮浸泡的目的是______。
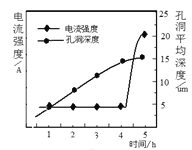
②电解时,电流强度和基板孔洞深度随时间变化如图所示,氧化的终点电流突然增加的原因是______。
高三化学综合题中等难度题查看答案及解析
-
为了实现“将全球温度上升幅度控制在2℃以内”的目标,科学家正在研究温室气体CO2的转化和利用。
(1)海洋是地球上碳元素的最大“吸收池”
①溶于海水中的CO2主要以四种无机碳形式存在,分别为CO2、H2CO3、CO32-和_________(填离子符号)。
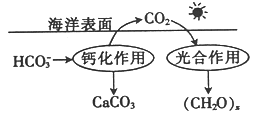
②在海洋中,可通过如图所示的途径来固碳。则发生光合作用时,CO2与H2O反应生成(CH2O)x和O2的化学方程式为__________________。
(2)有科学家提出可利用FeO来吸收CO2,已知:
C(s)+2H2O(g)
CO2(g)+2H2(g) △H=+113.4 kJ·mol-1
3FeO(s)+H2O(g)
Fe3O4(s)+H2(g) △H=+18.7 kJ·mol-1
则6FeO(s)+CO2(g)
2Fe3O4(s)+C(s) △H=_____kJ·mol-1。
(3)以CO2为原料可制备甲醇:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),向一恒容密闭容器中充入1moCO2(g)和3molH2(g),测得CO2(g)和CH3OH(g)的浓度随时间的变化如图所示。
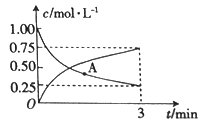
①若A点的正反应速率用v正(CO2)来表示,A点的逆反应速率用v逆(CO2)来表示,则v正(CO2)_______(填“>”“ <”或“=”)v逆(CO2)。
②0~3min内,氢气的平均反应速率v(H2)_______________。
(4)在一定条件下,二氧化碳转化为甲烷:CO2(g)+4H2(g)
CH4(g)+2 H2O(g),△H。向一密闭容积正充入一定量的CO2和H2,在300℃时发生上述反应,达到平衡时测得c(CO2)= 0.2 mol·L-1,c(H2) =0.8 mol·L-1,c(H2O)=1.6mol·L-1。则该温度下上述反应的平衡常数K= ________。若200℃时该反应的平衡常数K=64.8,则该反应的△H_____(填“>’’或“<”)O。
高三化学简答题中等难度题查看答案及解析
-
下列说法正确的是
A.硅元素主要以单质、氧化物、硅酸盐的形式存在于自然界中
B.镁、铝具有一定的抗腐蚀性,是因为镁、铝不易被氧化
C.84消毒液的主要成分是NaClO
D.某些金属元素的焰色反应、海水提溴、煤的液化、石油的裂化都是化学变化的过程
高三化学选择题中等难度题查看答案及解析
-
燃煤后烟气脱硫方法之一是利用天然海水的碱性吸收烟气中SO2并转化为无害的SO42-,其流程的示意图如下 (从吸收塔排出的海水中S元素主要以HSO3-形式存在)
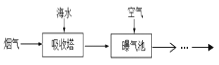
下列有关说法正确的是( )
A. 海水中碳元素主要以HCO3-的形式存在,HCO3-的水解方程式为HCO3-+H2O
CO32-+H3O+
B. 排入曝气池进行处理时,鼓入大量空气,主要目的是为了将HSO3-氧化为SO42-
C. 为了加快SO2的吸收速率,进入吸收塔的海水温度越高越好
D. 经过曝气池氧化后的“海水”可以直接排放到大海
高三化学选择题中等难度题查看答案及解析
-
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是
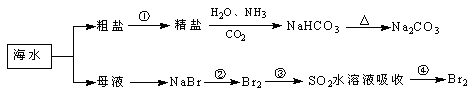
A.工业上通过电解熔融状态MgCl2制取金属镁
B.在第②、④步骤中,溴元素均被氧化
C.用澄清的石灰水可鉴别NaHCO3和Na2CO3
D.制取NaHCO3的反应是利用其溶解度小于NaCl
高三化学选择题中等难度题查看答案及解析