298 K 时,向20 mL 0.01mol/LCH3COOH 溶液中逐滴加入0.01mol/L KOH 溶液,其pH变化曲线如图所示。下列叙述错误的是

A. a>2
B. 醋酸的电离平衡常数:Ka= 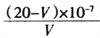
C. b点溶液中:c(CH3COOH)+2c(H+) = c(CH3COO-) +2c(OH-)
D. a、b、c、d 四点溶液的导电性强弱顺序:d>c>b>a
高三化学单选题中等难度题
298 K 时,向20 mL 0.01mol/LCH3COOH 溶液中逐滴加入0.01mol/L KOH 溶液,其pH变化曲线如图所示。下列叙述错误的是

A. a>2
B. 醋酸的电离平衡常数:Ka= 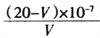
C. b点溶液中:c(CH3COOH)+2c(H+) = c(CH3COO-) +2c(OH-)
D. a、b、c、d 四点溶液的导电性强弱顺序:d>c>b>a
高三化学单选题中等难度题
298 K 时,向20 mL 0.01mol/LCH3COOH 溶液中逐滴加入0.01mol/L KOH 溶液,其pH变化曲线如图所示。下列叙述错误的是

A. a>2
B. 醋酸的电离平衡常数:Ka= 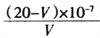
C. b点溶液中:c(CH3COOH)+2c(H+) = c(CH3COO-) +2c(OH-)
D. a、b、c、d 四点溶液的导电性强弱顺序:d>c>b>a
高三化学单选题中等难度题查看答案及解析
(6分)已知某温度下CH3COOH的电离常数K=1.6×10-5。该温度下向20mL0.01mol/LCH3COOH溶液中逐滴加入0.01mol/L KOH溶液,其pH变化曲线如下图所示(忽略温度变化)。请回答下列有关问题:
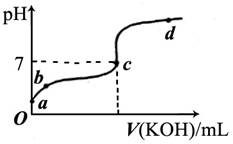
(1)a点溶液中c(H+)为________。
(2)b点溶液中离子浓度的大小顺序可能有________种情况。
(3)a、b、c三点中水的电离程度最大的是________。
高三化学填空题简单题查看答案及解析
298K时,向20mL 0.01mol·L-1 HF溶液中逐滴加入0.01mol·L-1 KOH溶液,其pH变化曲线如图所示。下列叙述正确的是( )

A. 水电离出的H+浓度:a<b<c<d
B. 氢氟酸的电离平衡常数:Ka=
C. V=20
D. b点溶液中:c(F-)>c(HF)
高三化学单选题困难题查看答案及解析
常温下,向20 mL0.01mol/LCH3COOH溶液中逐滴加入0.01mol/L的NaOH溶液,溶液中水电离的c(H+)随加入NaOH溶液的体积变化如下图所示,下列说法正确的是( )
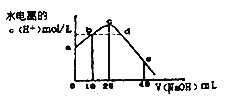
A. b、d两点溶液的pH相同
B. 从a到c,对醋酸的电离既有促进作用也有抑制作用
C. e 点所示溶液中,c(Na+)=2c(CH3COO-)+2c(CH3COOH)=0.01mol/L
D. 从a→c的过程中,既存在pH=7的点也存在水电离的c(H+)=10-7mol/L的点
高三化学单选题困难题查看答案及解析
常温下,向20mL 0.0lmol/LCH3COOH溶液中逐滴加入0.01mol/L的NaOH溶液,溶液中水所电离出的c(H+)随加入NaOH溶液的体积变化示意图如图4, 下列说法正确的是
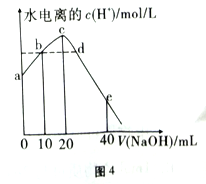
A. 从a到c,对醋酸的电离既有促进作用也有抑制作用
B. b、d两点溶液的pH相同
C. e点所示溶液中,c(Na+)=2c(CH3COO-)+2c(CH3COOH)=0.01mol/L
D. c点所示溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
高三化学选择题困难题查看答案及解析
已知某温度下CH3COOH的电离常数K=1.6×10-5。该温度下向20 mL 0.01 mol/L CH3COOH溶液中逐滴加入0.01 mol/L KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:

(1)a点溶液中c(H+)为 。
(2)b点溶液中离子浓度大小顺序为 或 或 。c点溶液中的离子浓度大小顺序为 。
(3)a、b、c三点中水的电离程度最大的是 ,滴定过程中宜选用 作指示剂。
高三化学选择题中等难度题查看答案及解析
已知25℃时CH3COOH的电离常数K=1.6×10-5。该温度下向20ml 0.01mol·L-1 CH3COOH溶液中逐滴加入0.01mol·L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是

A. a点溶液中c(H+)为4.0×10-5mol/L
B. c点溶液中的离子浓度大小顺序为c(K+)>c(CH3COO->c(H+)=c(OH-)
C. V=200
D. a、b、c三点中水的电离程度最大的是c点
高三化学选择题中等难度题查看答案及解析
常温下,向10mL0.01mol/L的草酸溶液中逐滴加入0.01mol/L的KOH溶液,所得溶液中H2C2O4、HC2O4-、C2O42-、三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法正确的是( )
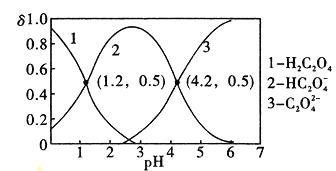
A.NaHC2O4溶液中HC2O4-的水解程度大于电离程度
B.当V(KOH)=5mL时,c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
C.当V(KOH)=20mL时,溶液中存在:c(OH-)-c(H+)=c(HC2O4-)+2c(H2C2O4)
D.当V(KOH)=15mL时,溶液中存在:c(K+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+)
高三化学单选题中等难度题查看答案及解析
在298K 1.0l×l05Pa下,将32g SO2通入750mL 1mol/L KOH溶液中充分反应.测得反应放出xkJ的热量。已知在该条件下,lmol SO2通入1 L 2mol/L KOH溶液中充分反应放出ykJ的热量。则SO2与KOH溶液反应生成KHSO3的热化学方程式正确的是( )
A.SO2(g)+KOH(aq)=KHSO3(aq) △H=-(4x-y)kJ/mol
B.SO2(g)+KOH(aq)=KHSO3(aq) △H=-(2x-y)kJ/mol
C.SO2(g)+KOH(aq)=KHSO3(aq) △H=-(2y-x)kJ/mol
D.2SO2(g)+2KOH(1)=2KHSO3(1) △H=-(8x-2y)kJ/mol
高三化学选择题中等难度题查看答案及解析
在298 K、1.01×105 Pa下,将32 g SO2通入750 mL 1 mol/L KOH溶液中充分反应。测得反应放出x kJ的热量。已知在该条件下,1 mol SO2通入1 L 2 mol/L KOH溶液中充分反应放出y kJ的热量。则SO2与KOH溶液反应生成KHSO3的热化学方程式正确的是( )
A.SO2(g)+KOH(aq)=KHSO3(aq)ΔH=-(4x-y) kJ/mol
B.SO2(g)+KOH(aq)=KHSO3(aq)ΔH=-(2x-y) kJ/mol
C.SO2(g)+KOH(aq)=KHSO3(aq)ΔH=-(2y-x) kJ/mol
D.2SO2(g)+2KOH(l)=2KHSO3(l)ΔH=-(8x-2y) kJ/mol
高三化学选择题中等难度题查看答案及解析