-
(11分)某研究性小组对Fe3+ 与S2-的反应有不同的看法,
(1)猜想可能发生三种反应情况:双水解反应;氧化还原反应; ;(填反应类型)。
针对上述猜想该小组做了如下探究实验:
序号
实验操作
现象
①
向大试管中加入20mL 0.1mol∙L-1的Na2S溶液
(已知Na2S溶液显碱性,pH约为12),再滴加5mL 0.1mol∙L-1的FeCl3溶液,边滴边振荡
产生大量黑色沉淀,反应后溶液仍显碱性
②
向另一支大试管中加入20mL 0.1mol∙L-1FeCl3溶液(已知FeCl3溶液显酸性,pH约为2),再滴加5mL 0.1 mol∙L-1的Na2S溶液,边滴边振荡
局部有黑色沉淀但瞬间消失,溶液颜色变浅,并产生大量黄色浑浊,反应后溶液仍显酸性
【查阅资料】
Fe2S3是黑色或深黄绿色固体,中性或碱性很稳定,FeS是黑褐色的固体。
(2)根据实验现象和理论分析:实验①发生的离子反应方程式为: 。
实验②发生反应的离子方程式: 。
(3)设计实验验证实验②所发生的化学反应,检验对象是实验②所得混合物。
限选试剂:稀盐酸、NaOH溶液、CS2、KSCN溶液、酸性KMnO4溶液、H2O2。
实验操作
预期现象和结论
(4)综合分析实验①、②,影响Fe3+ 与S2- 的反应类型的可能因素有 ; 。(至少填两点)
高三化学实验题困难题查看答案及解析
-
(一)某化学研究性学习小组讨论Fe3+和SO32﹣之间发生怎样的反应,提出了两种可能;一是发生氧化还原反应:2Fe3++SO32﹣+H2O=2Fe2++SO42﹣+2H+;二是发生双水解反应:2Fe3++3SO32﹣+6H2O=2Fe2++2Fe(OH)3(胶体)+3H2SO4,为了证明是哪一种反应发生,同学们设计并实施了下列实验,请填写下列空白:
实验Ⅰ:学生选择的实验用品:N
a2SO3浓溶液,BaCl2稀溶液,稀盐酸,试管若干,胶头滴管若干,从选择的药品分析,设计这个实验的目的是 .
实验Ⅱ:取5mL FeCl3浓溶液于试管中,再滴加入 Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色,这种红褐色液体是 向红褐色液体中加入稀盐酸至过量,将所得溶液分为两等份,其中一份加入KSCN溶液变成血红色,反应的离子方程式为 .另一份加入BaCl2稀溶液有少量白色沉淀生成,产生该白色沉淀的离子方程式是 .
实验Ⅲ:换成两种稀溶液重复实验Ⅱ,产生现象完全相同,由上述实验得出的结论是
若在FeCl3溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无
色气体,该反应的化学方程式是 .
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看出,二者的水溶液与FeCl3溶液反应现象差别很大,分析其可能的原因是:① ;② .
(二)镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。NiSO4·xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得。操作步骤如下:

①向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,除去Cu2+的离子方程式为__________。
②滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是______________。
高三化学实验题中等难度题查看答案及解析
-
某化学研究性学习小组讨论Fe3+溶液和SO32-溶液之间发生怎样的反应,提出了两种可能,写出预计反应的离子方程式:
一是发生氧化还原反应 ,二是发生彻底互促水解反应 。
为了证明发生怎样的反应,同学们设计并进行如下实验,请填写下列空白:
实验Ⅰ:取5 mL FeCl3浓溶液于试管中,逐滴加入某Na2SO3浓溶液至过量,观察到无气泡产生,无沉淀生成,但溶液颜色最终变为红褐色。这种红褐色液体是 。
向红褐色液体中逐滴加入稀盐酸至过量,可观察到溶液最终变为黄色。将所得溶液加入BaCl2稀溶液,有少量白色沉淀生成,产生该白色沉淀的离子方程式是 。
实验Ⅱ:将FeCl3和Na2SO3溶液分别稀释后,重复实验Ⅰ,产生的现象完全相同。
同学们由上述实验得出的结论是 。
指导老师看过上述实验步骤后认为该设计有缺陷,应在开始实验前对某主要药品进行检验,该主要药品为 ;检验的目的是 。
高三化学实验题困难题查看答案及解析
-
某化学研究性学习小组讨论Fe3+溶液和SO32-溶液之间发生怎样的反应,提出了两种可能,写出预计反应的离子方程式:
一是发生氧化还原反应________①________;二是发生互促水解反应________②________。
为了证明发生怎样的反应,同学们设计并进行如下实验,请填写下列空白:
实验Ⅰ:取5mLFeCl3浓溶液于试管中,逐滴加入某Na2SO3浓溶液至过量,观察到无气泡产生,无沉淀生成,但溶液颜色最终变为红褐色。这种红褐色液体是________③________。
向红褐色液体中逐滴加入稀盐酸至过量,可观察到溶液最终变为黄色。将所得溶液分成两等份:
其中一份加入KSCN溶液,溶液变成血红色,此步实验的目的是________④________;另一份加入BaCl2稀溶液,有少量白色沉淀生成,产生该白色沉淀的离子方程式是________⑤________。
实验Ⅱ:将FeCl3和Na2SO3溶液分别稀释后,重复实验Ⅰ,产生的现象完全相同。
同学们由上述实验得出的结论是________⑥________。
指导老师看过上述实验步骤后认为该设计有缺陷,应在开始实验前对某主要药品进行检验,该主要药品为________⑦;检验的目的是________⑧________。
高三化学实验题困难题查看答案及解析
-
(12分)某化学研究性学习小组探讨Fe3+和SO32-之间发生怎样的反应,请你一起参与并协助他们完成实验。
⑴提出猜想:
甲同学认为发生氧化还原反应,其反应的离子方程式为________;
乙同学认为发生双水解反应,其反应方程式为2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3;
⑵实验验证:
丙同学设计了下列实验来探究反应的可能性。
①为了检验所用Na2SO3是否变质,应选用的试剂是________。
②取5mLFeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量,观察到溶液颜色由黄色变为红棕色(无气泡产生,也无沉淀生成)。
③将②溶液分成两等份,其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成;另一份滴入几滴KSCN溶液,溶液变成血红色。
⑶得出结论:
①根据丙同学的实验得出的结论是: ;
②实验③中溶液变成血红色的离子方程式为________。
⑷拓展探究:
①丁同学在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是。
②从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,其可能的原因除SO32-水解能力较CO32-________(填“大”或“小”)外,还有
高三化学实验题中等难度题查看答案及解析
-
(12分)某化学研究性学习小组探讨Fe3+和SO32—之间发生怎样的反应,请你一起参与并协助他们完成实验。
(1)提出猜想:
甲同学认为发生氧化还原反应,其反应方程式为________;
乙同学认为发生双水解反应,其反应方程式为2Fe3++3SO32—+6H2O=2Fe(OH)3(胶体)+3H2SO3; ……
(2)实验验证:
丙同学设计了下列实验来探究反应的可能性。
①为了检验所用Na2SO3是否变质,应选用的试剂是。
②取5mLFeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量,观察到溶液颜色由黄色变为红棕色(无气泡产生,也无沉淀生成)。
③将②溶液分成两等份,其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成;另一份滴入几滴KSCN溶液,溶液变成血红色。
(3)得出结论:
①根据丙同学的实验得出的结论是:________;
②实验③中溶液变成血红色的离子方程式为________。
(4)拓展探究:
①丁同学在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是________。
②从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,其可能的原因除SO32-水解能力较CO32-小外,还有________。
高三化学实验题简单题查看答案及解析
-
某化学研究性学习小组探讨Fe3+和SO32-之间发生怎样的反应,请你一起参与并协助他们完成实验。
(1)提出猜想:
甲同学认为发生氧化还原反应,其反应方程式为___________________。
乙同学认为发生了相互促进的水解反应,其反应方程式为:
2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3
(2)实验验证:
丙同学设计了下列实验来探究反应的可能性。
①为了检验所用Na2SO3是否变质,应选用的试剂是_____________。
②取5 mL FeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量,观察到溶液颜色由黄色变为红褐色(无气泡产生,也无沉淀生成)。
③将②溶液分成两等份,其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成;另一份滴入几滴KSCN溶液,溶液变成血红色。
(3)得出结论:
①根据丙同学的实验得出的结论是:___________________________________。
②实验③中溶液变成血红色的有关离子方程式为___________________。
(4)拓展探究:
①丁同学在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是___________________________________。
②从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,两者的水溶液与氯化铁溶液反应的现象差别很大,其可能的原因除SO32-水解能力较CO32-小外,还有___________________________________。
高三化学实验题中等难度题查看答案及解析
-
某化学研究性学习小组探讨Fe3+和SO之间发生怎样的反应,请你一起参与并协助他们完成实验。
(1)提出猜想:
甲同学认为发生氧化还原反应,其反应方程式为___________________________________。
乙同学认为发生了相互促进的水解反应,其反应方程式为:
……
(2)实验验证:
丙同学设计了下列实验来探究反应的可能性。
①为了检验所用Na2SO3是否变质,应选用的试剂是________________________________。
②取5 mL FeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量,观察到溶液颜色由黄色变为红褐色(无气泡产生,也无沉淀生成)。
③将②溶液分成两等份,其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成;另一份滴入几滴KSCN溶液,溶液变成血红色。
(3)得出结论:
①根据丙同学的实验得出的结论是:___________________________________。
②实验③中溶液变成血红色的有关离子方程式为___________________________________。
(4)拓展探究:
①丁同学在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是___________________________________。
②从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,两者的水溶液与氯化铁溶液反应的现象差别很大,其可能的原因除
水解能力较
小外,还有___________________________________。
高三化学实验题极难题查看答案及解析
-
某化学研究性学习小组探讨Fe3+和
之间发生怎样的反应,请你一起参与并协助他们完成实验。(1)提出猜想:
甲同学认为发生氧化还原反应,其反应方程式为____________________________________。
乙同学认为发生双水解反应,其反应方程式为2Fe3++3
+6H2O===2Fe(OH)3(胶体)+3H2SO3。
……
(2)实验验证:
丙同学设计了下列实验来探究反应的可能性。
①为了检验所用Na2SO3是否变质,应选用的试剂是________________。
②取5 mL FeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量,观察到溶液颜色由黄色变为红棕色(无气泡产生,也无沉淀生成)。
③将②溶液分成两等份,其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成;另一份滴入几滴KSCN溶液,溶液变成血红色。
(3)得出结论:
①根据丙同学的实验得出的结论是:____________________________________。
②实验③中溶液变成血红色的有关离子方程式为_____________________。
(4)拓展探究:
①丁同学在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是__________________________________。
②从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,两者的水溶液与氯化铁溶液反应的现象差别很大,其可能的原因除
水解能力较
小外,还有________________。
高三化学填空题极难题查看答案及解析
-
某小组同学探究Cu和H2O2的反应。
(猜想预测)
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
(实验探究)
实验ⅰ:向装有0.5 g Cu的烧杯中加入20 mL 30% H2O2溶液,一段时间内无明显现象,10 小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:________。
(继续探究)
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2+ + 4NH3 ⇌[ Cu(NH3)4] 2+ ,[ Cu(NH3)4] 2+为深蓝色;Cu(OH)2可溶于氨水形成深蓝色溶液。
装置
序号
试剂a
现象
ⅱ
20 mL 30% H2O与4 mL 5 mol/L H2SO4 混合液
Cu表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡
ⅲ
20 mL 30% H2O2与4 mL5 mol/L氨水混合液
溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物
(2)实验ⅱ中:溶液变蓝的原因是________(用化学用语解释);经检验产生的气体为氧气,产生氧气的原因是________。
(3)对比实验ⅰ和ⅲ,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。
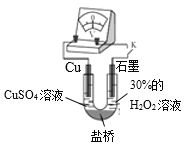
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:_________。利用该方法也可证明酸性增强可提高H2O2的氧化性,导致Cu溶解速率加快。
(4)对比实验ⅱ和ⅲ,实验ⅲ中产生氧气速率明显更快,可能的原因是_______。
(5)实验ⅲ有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因:________。
(6)基于以上实验,影响Cu与H2O2反应速率的因素有________。
高三化学实验题困难题查看答案及解析