-
Ⅰ.现有常温时浓度相同的五种电解质溶液:①CH3COOH ②Na2CO3 ③HNO3④CH3COONa ⑤NaOH
(1)五种溶质中是弱电解质的是_____(填编号),若常温时该弱电解质电离常数为K,1mol/L的该溶液中c(H+)约为_____mol/L(用K表示)
(2)④溶液中离子与分子共_____种(包括水分子).
(3)这五种溶液的pH由小到大的顺序是____________________(填编号).
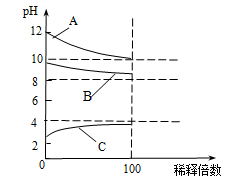
(4)将 CH3COONa溶液稀释100倍时,其pH变化如图中______曲线(填字母).Ⅱ.在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:2SO2(g)+O2(g) 2SO3(g)△H=-190kJ•mol-1
2SO3(g)△H=-190kJ•mol-1

(1)该反应500℃时的平衡常数_____450℃时的平衡常数(填“>”、“<”或“=”).
(2)450℃时,在一2L密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变 化如图,反应处于平衡状态的时间是___________
(3)据图判断,反应进行至20min时,曲线发生变化的原因是___________(用文字表达),10min到15min的曲线变化的原因可能是________(填字母).
A.加了催化剂B.缩小容器体积 C.降低温度 D.增加SO3物质的量
(4)欲提高SO2的转化率,下列措施可行的是________.(填字母)
a.向装置中再充入N2 b.向装置中再充入O2c.改变反应的催化剂 d.升高温度
-
(13分) 现有常温时浓度相同的五种电解质溶液:
①CH3COOH ②Na2CO ③HNO3 ④CH
③HNO3 ④CH COONa ⑤NaOH
COONa ⑤NaOH
(1)五种溶质中是弱电解质的是______(填编号),若常温时该弱电解质电离常数为K,1mol/L的该溶液中c(H+)约为__________mol/L(用K表示)
(2)④溶液中离子与分子共______种(包括水分子)。
(3)这五种溶液的pH由小到大的顺序是______________________________(填编号)。
(4)将 CH COONa溶液稀释100倍时,其pH变化如图中_______曲线(填字母).
COONa溶液稀释100倍时,其pH变化如图中_______曲线(填字母).
(5)上述五种溶液中分别加入AlCl3溶液,有气泡产生的是________(填编号),写出能产生气泡现象的离子方程式:.
-
现有电解质溶液:①Na2CO3 ②NaHCO3 ③CH3COONa ④NaOH
(1)当四种溶液的pH相同时,其物质的量浓度由大到小的顺序是________(填编号,以下相同)
(2)在上述四种电解质溶液中,分别加入AlCl3溶液,无气体产生的是________.
-
(4分)现有电解质溶液:①Na2CO3 ②NaHCO3 ③CH3COONa ④ NaOH
(1)当四种溶液的pH相同时,其物质的量浓度由大到小的顺序是________(填编号,以下相同)
(2)在上述四种电解质溶液中,分别加入AlCl3溶液,无气体产生的是________
-
常温下.有浓度均为0.1 mol·L-l的下列4种溶液:①NaCN溶液②NaOH溶液③CH3COONa溶液④Na2CO3溶液
| HCN | H2CO3 | CH3COOH |
| Ka=4.9×10-10 | Ka1=4×10-7 Ka2=5.6×10-11 | Ka=1.7×10-5 |
(1)这4种溶液pH由大到小的顺序是_______(填序号)。
(2)NaCN溶液显碱性的原因(用方程式说明)______
(3)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③_____④(填“>”、“<"、“=”)。
(4)25℃时,将amol·L-1 的醋酸和 0.1 mol·L-lNaOH溶液等体积混合后,溶液的pH=7,则a_____0.1(填“﹥”、“﹤”或“=”)。
(5)Na2CO3溶液中离子浓度大小为:___________
(6)向NaCN溶液中通入CH3COOH,则发生的离子反应方程式为:_______。
(7)同温下,溶液的pH值④____①(填“>”、“<"、“=”)。
-
(6分)现有浓度为0.1 mol·L-1的五种电解质溶液①Na2CO3;②NaHCO3;③NaAlO2;④CH3COONa; ⑤NaOH,已知:CO2+3H2O+2AlO2- = 2Al(OH)3↓+CO32 -
(1)这五种溶液的pH由小到大的顺序是: (填编号);
(2)在上述五种溶液中分别加入AlCl3溶液,能产生大量无色无味气体的是: (填编号);
(3)将上述①、②、③、④四种溶液两两混合时,有一对溶液相互间能发生反应,写出该反应的离子方程式: 。
-
(6分)现有浓度为0.lmol/L的五种电解质溶液:①Na2CO3 ②NaHCO3 ③NaAlO2④CH3COONa⑤NaOH
已知:
(1)上述五种溶液的pH由大到小的顺序为________。(填序号)
(2)将五种溶液稀释相同的倍数时,其pH变化最大的是________。(填序号)
(3)在上述五种溶液中分别加入AlCl3溶液后,能产生无色气体的是_______:(填序号)
-
现有浓度均为0.1 mol•L-1的五种电解质溶液①Na2CO3;②NaHCO3;③NaAlO2;④CH3COONa;⑤NaOH。
已知:HCO3- + H2O + AlO2-=Al(OH)3↓ + CO32-
(1)25℃时⑤的pH=_____________。
(2)请写出NaHCO3在水溶液中的电离方程式___________________________________。
(3)这五种溶液的pH由大到小的顺序是_____________________________(填编号)。
(4)在上述五种溶液中分别加入AlCl3溶液,能产生大量无色无味气体的是______(填编号)。
(5)将五种溶液稀释相同的倍数时,其pH变化最大的是___________________(填编号)。
-
现有浓度为0.1 mol·L-1的五种电解质溶液:①Na2CO3 ②NaHCO3 ③NaAlO2 ④CH3COONa ⑤NaOH
已知:CO2+3H2O+2AlO2-=2Al(OH)3↓+CO32-
⑴这五种溶液的pH由小到大的顺序是____________________(填编号);
⑵将五种溶液稀释相同的倍数时,其pH变化最大的是___________(填编号);
⑶混合碳酸(H2CO3)溶液和NaAlO2溶液,试写出所有可能发生的化学反应方程式:_____;
⑷常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| 甲 | 0.20 | 0.20 | pH=a |
| 乙 | 0.10 | 0.10 | pH=8.00 |
①不考虑乙组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸_________;乙组实验所得混合溶液中由水电离出的c(OH-)=_________mol/L。
②求出该混合溶液中下列算式的结果。
I.c(Na+)-c(A-)=__________________;II.c(OH-)-c(HA)=_________。
-
现有电解质溶液:①Na2CO3②NaHCO3③NaAlO2④CH3COONa⑤NaOH,且已知:CO2+3H2O+2AlO2-═2Al(OH)3↓+CO32-.
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是______(填编号).
(2)将上述物质的量浓度均为0.1mol/L的五种溶液稀释相同倍数时,其pH变化最大的是______(填编号).
(3)在上述五种电解质溶液中分别加入AlCl3溶液,无气体产生的是______(填编号)
(4)将上述①、②、③、④这四种电解质溶液混合,发生反应的离子方程式为______.

2SO3(g)△H=-190kJ•mol-1


