-
已知热化学方程式:
H2O(g) == H2(g) + O2(g) △H=" +241.8" kJ·mol-1
H2(g)+ O2(g) == H2O(1) △H= -285.8 kJ·mol-1
当1g液态水变为水蒸气时,其热量变化是( )
A. 吸热88kJ B. 吸热2.44 kJ C. 放热44kJ D. 吸热44 kJ
高二化学单选题中等难度题查看答案及解析
-
已知热化学方程式:
H2O(g) = H2(g) +
O2(g) △H = +241.8 kJ·mol-1
H2(g)+
O2(g) = H2O(1) △H = -285.8 kJ·mol-1
当18g液态水变为水蒸气时,其热量变化是
A.吸热44 k J B.吸热88kJ C.放热44kJ D.吸热2.44 kJ
高二化学选择题中等难度题查看答案及解析
-
已知热化学方程式:
H2O(g) == H2(g) +1/2 O2(g) △H = +241.8 kJ·mol-1
H2(g)+ 1/2O2(g) == H2O(1) △H = -285.8 kJ·mol-1
当1g液态水变为水蒸气时,其热量变化是
A. 吸热88kJ B. 吸热2.44 kJ C. 放热2.44 kJ D. 吸热44 kJ
高二化学选择题中等难度题查看答案及解析
-
已知热化学方程式:
H2O(g)=H2(g)+
O2(g)△H=+241.8kJ·mol-1
H2(g)+
O2(g)=H2O(1)△H=-285.8kJ·mol-1
当1g液态水变为水蒸气时,其热量变化是( )
A.吸热88kJ B.吸热44kJ C.放热44kJ D.吸热2.44kJ
高二化学单选题简单题查看答案及解析
-
在101 kPa和298 K时,有关反应的热化学方程式有:
H2(g)+
O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
H2(g)+
O2(g)===H2O(l) ΔH2=-285.8 kJ·mol-1
下列说法错误的是( )
A.H2燃烧生成1 mol H2O(g)时,放出241.8 kJ的热量
B.O2前面的
表示参加反应的O2的分子数目
C.燃烧热是以在101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量定义的,则 H2的燃烧热为285.8 kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
(1)已知下列热化学方程式:
H2(g)+1/2O2(g)==H2O(l) ΔH=−285.8 kJ·mol−1
H2(g)+1/2O2(g)==H2O(g) ΔH=−241.8 kJ·mol−1
C(s)+ 1/2O2(g)==CO(g) ΔH=−110.5 kJ·mol−1
C(s)+O2(g)==CO2(g) ΔH=−393.5 kJ·mol−1
回答下列问题:
①燃烧10gH2生成液态水,放出的热量为________。
②CO的燃烧热为________。
(2)0.3mol乙硼烷气体(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ的热量,则其热化学方程式为________________________。
(3)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出稀H2SO4溶液与稀NaOH溶液反应的热化学方程式__________________。
(4)已知:2SO2(g)+O2(g)
2SO3(g) ΔH=-196.6 kJ·mol–1
2NO(g)+O2(g)
2NO2(g) ΔH=-113.0 kJ·mol–1
请写出NO2与SO2反应生成SO3和NO的热化学方程式____________________。
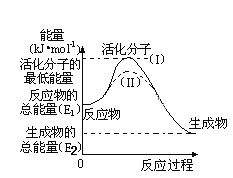
(5)研究活化能对于能源技术的革新有非常重大的实际意义。请认真观察下图,回答问题:
①图中反应的ΔH=_____________kJ/mol(用含有E1、E2代数式表示)。
②已知热化学方程式:H2(g)+1/2O2(g) = H2O(g) ΔH=-241.8kJ/mol,该反应的活化能为167.2kJ/mol,则H2O(g)=H2(g)+1/2O2(g)的活化能为________kJ/mol。
高二化学综合题中等难度题查看答案及解析
-
已知下列热化学方程式:
① H2(g) +
O2(g) = H2O(
);△H = -285kJ/mol
② H2O(g) = H2(g) +
O2(g); △H = + 241.8kJ/mol
③ C(s) +
O2(g) = CO(g); △H = -110.4kJ/mol
④ C(s) + O2(g) = CO2(g);△H = -393.5kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是______________。(用序号填写)
(2)燃烧10g H2生成液态水,放出的热量为_____________。
(3)CO的燃烧热的热化学方程式为___________________________________。
(4)已知常温下拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为:___________________
高二化学填空题中等难度题查看答案及解析
-
已知下列热化学方程式:
①H2(g)+
O2(g)=H2O(
); △H=﹣285kJ/mol
②H2(g)+
O2(g)=H2O(g); △H=﹣241.8kJ/mol
③C(s)+
O2(g)=CO(g); △H=﹣110.4kJ/mol
④C(s)+ O2(g)=CO2(g); △H=﹣393.5kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是_________________________________;
(2)C的燃烧热为_________________ kJ/mol;
(3)燃烧10g H2生成液态水,放出的热量为_____________________kJ;
高二化学填空题中等难度题查看答案及解析
-
下列有关热化学方程式或反应热的说法正确的是
A.已知:H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1,则H2燃烧热为-241.8 kJ·mol-1
B.已知:S(g)+O2(g)=SO2(g) ΔH1=-Q1;S(s)+O2(g)=SO2(g) ΔH2=-Q2(Q1、Q2均正值),则Q1<Q2
C.已知:1/2H2SO4(浓)+NaOH(aq)= 1/2 Na2SO4(aq)+H2O(l) ΔH1;CH3COOH(aq)+NH3·H2O(aq)=CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2|
D.已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g) ΔH=+489.0 kJ·mol-1;CO(g)+1/2O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1;C(石墨,s)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1641 kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
已知下列热化学方程式:
①H2(g)+
O2(g)===H2O(l) ΔH=-285.8 kJ/mol
②H2(g)+
O2(g)===H2O(g) ΔH=-241.8 kJ/mol
③C(s)+
O2(g)===CO(g) ΔH=-110.5 kJ/mol
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是_____________(填序号)。
(2)H2的燃烧热为_____________,C的燃烧热为_____________。
(3)燃烧10 g H2生成液态水,放出的热量为________。
(4)CO的燃烧热为______________,其热化学方程式为_______________________。
(5)在某温度时,测得0.01 mol•L-1的NaOH溶液的pH为11。该温度下,水的离子积常数Kw =________。
高二化学综合题简单题查看答案及解析