-
(8分)[化学—化学与技术]
粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。在实验室条件下以硫酸铜溶液为电解液,用电解的方法对粗铜提纯,并对阳极泥和电解液中金属进行回收和含量测定。回答以下问题;
(1)步骤一:电解精制:电解过程中,硫酸铜的浓度会________(选填:变大、不变、变小)。
步骤二:电解完成后,对电解液进行处理。
(2)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式:________。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl— = AuCl4— | >>1 |
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比l:3的混合物).请你简要解释金能够溶于王水的原因________。
(3)电解液含量的测定:下图是该小组探究电解液的一个实验流程:

则100mL滤液中Cu2+ 的浓度为________mol·L—1 ,Fe2+的浓度为________mol·L—1
-
(14分)已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(杂质与酸不反应)。某化学兴趣小组在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。
步骤一:电解精制:
电解时,粗铜应与电源的▲ _极相连,阴极上的电极反应式为▲ 。
电解过程中,硫酸铜的浓度会▲ (选填:变大、不变、变小)。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(1)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式:▲ 。残渣含有极少量的黄金。为了回收金,他们查阅了有关资料(见下表):
| 序号 | 反应 | 化学平衡常数 |
| 1 | Au + 6HNO3(浓) Au(NO3)3 + 3NO2↑+ 3H2O Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl- = AuCl4- | >>1 |
从资料中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1∶3的混合物),请你从化学平衡移动的角度简要解释金能够溶于王水的原因▲ 。
(2)滤液含量的测定:以下是该小组探究滤液的一个实验流程:

则100mL滤液中Cu2+ 的浓度为▲ mol·L-1 ,Fe2+的浓度为▲ mol·L-1
-
(11分) 已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。某化学兴趣小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。
步骤一:电解精制:
请回答以下问题:
电解时,粗铜应与电源的________极相连。阴极上的电极反应式为________。
电解过程中,硫酸铜的浓度会________(选填:变大、不变、变小)。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(1)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式:________。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl— = AuCl4— | >>1 |
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1∶3的混合物),请你简要解释金能够溶于王水的原因:________。
(2)滤液含量的测定:
以下是该小组探究滤液的一个实验流程:

则100mL滤液中Cu2+ 的浓度为________mol·L—1 ,Fe2+的浓度为mol·L—1
-
(8分)已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。某化学兴趣小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。步骤一:电解精制:
请回答以下问题:电解时,阴极上的电极反应式为________;
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(1)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式:________。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl— = AuCl4— | >>1 |
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1∶3的混合物),请你简要解释金能够溶于王水的原因:________
(2)滤液含量的测定: 以下是该小组探究滤液的一个实验流程:

则100ml滤液中Fe2+的浓度为________mol·L-1
-
(10分)已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不不反应)。某化学兴趣小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。
步骤一:电解精制:
请回答以下问题:
电解时,粗铜应与电源的________极相连。阴极上的电极反应式为________
电解过程中,硫酸铜的浓度会________(选填:变大、不变、变小)
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:
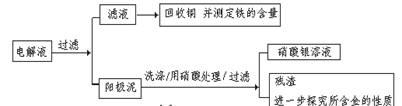
(1)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式:________
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au + 6HNO3(浓) Au(NO3)3 + 3NO2↑+ 3H2O Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl— AuCl4— AuCl4— | >>1 |
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1∶3的混合物),请你简要解释金能够溶于王水的原因:________
(2)滤液含量的测定:以下是该小组探究滤液的一个实验流程:

则100mL滤液中Cu2+ 的浓度为________mol·L-1 ,Fe2+的浓度为________mol·L-1
-
粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应).在实验室条件下以硫酸铜溶液为电解液,用电解的方法对粗铜提纯,并对阳极泥和电解液中金属进行回收和含量测定.
回答以下问题:
步骤一:电解精制:电解过程中,硫酸铜的浓度会______(选填:变大、不变、变小).
步骤二:电解完成后,对电解液进行处理:
(1)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式:______.
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au+6HNO3(浓)=Au(NO3)3+3NO2↑+3H2O | <<1 |
| 2 | Au3++4Cl-=AuCl4- | >>1 |
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1:3的混合物),请你简要解释金能够溶于王水的原因:______.
(2)滤液含量的测定:以下是该小组探究滤液的一个实验流程:

则100mL滤液中Cu2+ 的浓度为______mol•L-1,Fe2+的浓度为______mol•L-1.
-
粗铜中含有少量的锌、铁、银、金等金属。某化学兴趣小组以硫酸铜为电解液电解精炼铜之后,将电解液过滤得到滤液A和阳极泥。该小组同学设计如下实验方案测定滤液A中Fe2+ 、Cu2+ 的浓度。
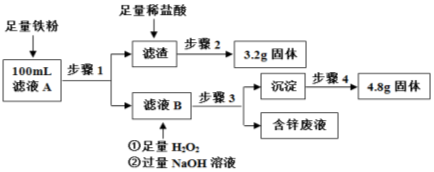
已知:Zn(OH)2可与NaOH反应生成溶于水的Na2ZnO2。
试回答下列问题:
(1)步骤2中涉及的操作是________、洗涤、晾干、称量;步骤4的操作依次是洗涤、灼烧、冷却、称量,在灼烧时,除需要三脚架外,还需要用到的实验仪器是____________(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.酒精灯
F.干燥器
(2)写出滤液B中加入H2O2 发生反应的离子方程式_________________________________
(3)滤液A中c(Cu2+)=_______mol•L-1 ,c(Fe2+)=_______mol•L-1 ;若步骤4的操作中“灼烧”不够充分,则滤液A中c(Fe2+)_____________(填偏大“偏大”、“偏小”或“无影响”)。
-
下列装置所示的实验中,能达到实验目的是( )
A.
除去Cl2中的HCl杂质
B.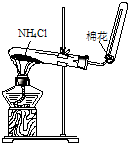
实验室制取NH3
C.
定量测定H2O2分解化学反应速率
D.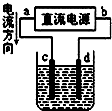
c为粗铜,d为纯铜,溶液为硫酸铜溶液,电解精炼铜
-
下列装置所示的实验中,能达到实验目的的是
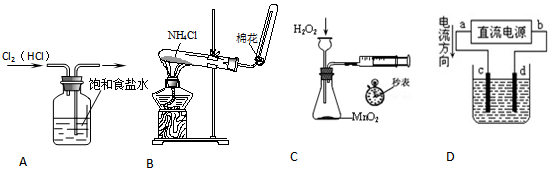
A.除去Cl2中的HCl杂质
B.实验室制取NH3
C.定量测定H2O2分解化学反应速率
D.c为粗铜,d为纯铜,溶液为硫酸铜溶液,电解精炼铜
-
用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2g 含有少量中性易溶杂质的样品,配成500mL 待测溶液。用0.1000mol·L-1的硫酸滴定,写出该中和反应的热化学方程式________________________________(中和热ΔH=-57.3 kJ/mol)。
(2)滴定过程中,眼睛应注视___________,若用酚酞作指示剂达到滴定终点的标志是_____________。
(3)根据下表数据,计算烧碱样品的纯度是___________(用百分数表示,保留小数点后两位)
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 |
| 滴定前的刻度(mL) | 滴定后的刻度(mL)) |
| 第一次 | 10. 00 | 0. 40 | 20. 50 |
| 第二次 | 10. 00 | 4. 10 | 24. 00 |
(4)下列实验操作会对滴定结果产生什么后果?(填“偏高”“偏低”或“无影响”)
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果____________。
②若将锥形瓶用待测液润洗,然后再加入10. 00mL待测液,则滴定结果____________。















