-
化学需氧量(COD)是水体质量的控制项目之一,COD是指用强氧化剂(我国采用K2Cr2O7处理一定量水样时所消耗的氧化剂的量,并换算成以氧气为氧化剂时,1L水样所消耗O2的质量(mg・L-1)。
现取某池塘中的水样20.00mL,加入10.00mL 0.04000mol/L K2Cr2O7溶液,并加入适量酸和催化剂,加热反应2h。在指示剂作用下,需用0.1000mol/L Fe(NH4)2(SO4)2溶液12.00mL滴定剩余的K2Cr2O7,此时,发生的反应是:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。求该池塘水样的COD为多少?
高三化学计算题简单题查看答案及解析
-
化学需氧量(COD)是衡量水质的重要指标之一。COD 是指在特定条件下用一种强氧化 剂(如 KMnO4)定量地氧化水体中的还原性物质所消耗的氧化剂的量(折算为氧化能力相当的O2 质量,单位:mg·L-1)。其测定过程如下: 取 100.0mL 水样,用硫酸酸化,加入 10.0 mL 0.002000mol·L-1 KMnO4溶液,充分作用后,再加入 10.0mL 0.005000mol·L-1
溶液。用 0.002000mol·L-1 KMnO4溶液滴定,滴定终点时消耗 6.50mL。
已知:2MnO
+5
+16H+=2Mn2++10CO2↑+8H2O
(1)1 mol KMnO4 的氧化能力与_____g O2 的氧化能力相当(作氧化剂时转移的电子数相同)。
(2)该水样的 COD 值是_____mg·L-1 (保留小数点后一位)。
高三化学计算题中等难度题查看答案及解析
-
化学需氧量(chemical oxygen demand,简称COD)表示在强酸性条件下重铬酸钾氧化 1 L 污水中有机物所需的氧化剂的量,并换算成以氧气为氧化剂时,1 L水样所消耗O2的质量(mg·L-1)计算。COD小,水质好。某湖面出现赤潮,某化学兴趣小组为测定其污染程度,用 1.176 g K2Cr2O7固体配制成 100 mL溶液,现取水样20.00 mL,加入10.00 mL K2Cr2O7溶液,并加入适量酸和催化剂,加热反应2 h。多余的K2Cr2O7用0.100 0 mol·L-1Fe(NH4)2(SO4)2溶液进行滴定,消耗Fe(NH4)2(SO4)2溶液的体积如下表所示。此时,发生的反应是CrO72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。(已知K2Cr2O7和有机物反应时被还原为 Cr3+,K2Cr2O7的相对分子质量为294)
序号
起始读数/mL
终点读数/mL
1
0.00
12.10
2
1.26
13.16
3
1.54
14.64
(1)K2Cr2O7溶液的物质的量浓度为______mol·L-1。
(2)求该湖水的COD为______mg·L-1。
高三化学计算题中等难度题查看答案及解析
-
化学需氧量(chemical oxygen demand,简称COD)表示在强酸性条件下重铬酸钾氧化一升污水中有机物所需的氧化剂的量,并换算成以氧气为氧化剂时,1 L水样所消耗O2的质量(mg·L-1)计算。COD小,水质好。某湖面出现赤潮,某化学兴趣小组为测定其污染程度,用1.176 g K2Cr2O7固体配制成100 mL溶液,现取水样20.00 mL,加入10.00 mL K2Cr2O7溶液,并加入适量酸和催化剂,加热反应2 h。多余的K2Cr2O7用0.100 0 mol·L-1Fe(NH4)2(SO4)2溶液12.00 mL恰好反应完,此时
,发生的反应是Cr2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O。
(已知K2Cr2O7和有机物反应时被还原为Cr3+,K2Cr2O7的相对分子质量为294)
(1)K2Cr2O7溶液的物质的量浓度为______________ mol·L-1。
(2)求该湖水的COD为____________mg·L-1。
高三化学计算题困难题查看答案及解析
-
(15分)浙江省“五水共治”是水质治理的重要举措,其中化学需氧量(COD)是水质测定中的重要指标,可以反映水中有机物等还原剂的污染程度。COD是指在一定条件下,用强氧化剂氧化水样中的还原剂及有机物时所消耗氧化剂的量,然后折算成氧化水样中的这些还原剂及有机物时需要氧气的量。某学习小组用重铬酸钾法测定某水样中的COD。主要的实验装置、仪器及具体操作步骤如下:
实验装置及仪器:

操作步骤:
①用仪器c将20.00mL水样置于250mL锥形瓶中,加入数粒碎瓷片。
②在水样中加入重铬酸钾标准溶液10.00mL,安装回流装置(如上图所示),从冷凝管上口加入30.00mL的H2SO4—Ag2SO4溶液,混匀后加热回流2h,充分反应。
③冷却后加指示剂2d,用硫酸亚铁铵溶液滴定多余重铬酸钾,至溶液由绿色变成红褐色。
已知:Cr2O72—+14H++6Fe2+=6Fe3++2Cr3++7H2O
请你回答下列问题:
(1)仪器c的名称: ;用仪器c吸取液体时,左手拿洗耳球,右手将仪器c插入溶液中吸取,当 时,立即用食指将管口堵住,将管尖离开液面,稍松食指使液面平稳下降,至凹液面最低处与标线相切,立即按紧管口。
(2)下列有关操作不正确的是 (用相应编号填写)
A.用硫酸亚铁铵溶液滴定时需上述仪器中的仪器b
B. 仪器c在使用时需要先用待取液进行润洗,管尖残留的液体一般不要吹出
C.加入数粒碎瓷片的作用是可以防止液体暴沸
D.上述操作步骤③中在滴定时判断滴定终点的指示剂可以是甲基橙
E.加热回流结束后,要用蒸馏水对冷凝管管壁进行冲洗
(3)在加热回流过程中,可以用水浴作为恒温加热源吗?同时请说明理由。
(4)下列因素对测定水样中的COD能产生影响的有 (用相应编号填写)
①硫酸的用量 ②反应装置中的锥形瓶在反应前用蒸馏水洗涤
③重铬酸钾的用量 ④回流时间的长短
(5)实验室配制重铬酸钾标准溶液的主要步骤及装置如下所示:
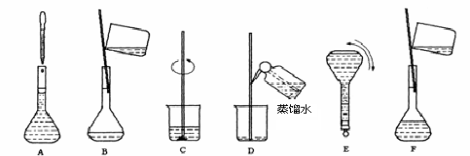
将上述实验步骤A到F按实验过程先后次序排列
(6)已知:重铬酸钾标准溶液的c(Cr2O72—)=0.0250mol·L—1,硫酸亚铁铵溶液的c(Fe2+)=0.0100 mol·L—1,滴定终点时所消耗的硫酸亚铁铵溶液的体积为12.00mL,则按上述实验方法,测得的该水样的化学需氧量CODCr(O2)= mg/L
高三化学实验题困难题查看答案及解析
-
化学知识在环境保护中起关键作用,下列叙述不正确的是
A.在燃煤中加入适量的生石灰能有效减少二氧化硫的排放
B.控制含磷洗涤剂的生产和使用有利于防止水体富营养化
C.采用汽车尾气处理技术可将汽车尾气中的NO和CO转化为无害气体
D.使用加酶洗衣粉,水温越高,洗涤效果更好
高三化学选择题中等难度题查看答案及解析
-
(14分)对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。
(1)硫酸工厂的酸性废水中砷(As)元素(主要以H3AsO3形式存在)含量极高,为控制砷的排放,某工厂采用化学沉降法处理含砷废水。请回答以下问题:
①已知砷是氮的同族元素,比氮原子多2个电子层,砷在元素周期表的位置为 ____,AsH3的稳定性比NH3的稳定性 (填“强”或“弱”)。
②工业上采用硫化法(通常用硫化钠)去除废水中的砷,生成物为难溶性的三硫化二砷,该反应的离子方程式为 。
(2)电镀厂的废水中含有的CN-有剧毒,需要处理加以排放。
①已知HCN为一元弱酸,则NaCN溶液的pH 7(填“>”、“=”或“<”)。
②处理含CN -废水的方法之一是在微生物的作用下,CN -被氧气氧化成HCO3—,同时生成NH3,该反应的离子方程式为 。
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A—表示乳酸根离子)。
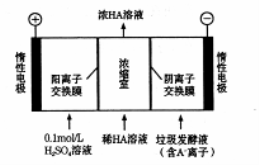
①阳极的电极反应式为 。
②简述浓缩室中得到浓乳酸的原理___________________________。
③电解过程中,采取一定的措施可控制阴极室的pH约为6~8,此时加入浓缩室的OH—可忽略不计。400mL10g/L的乳酸溶液通电一段时间后,浓度上升为145g/L(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为____L(乳酸的摩尔质量为90g/mol)。
高三化学填空题困难题查看答案及解析
-
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。
(1)硫酸厂的酸性废水中砷(As)元素(主要以 H3AsO3 形式存在)含量极高,为控制砷的排放, 某工厂采用化学沉淀法处理含砷废水。请回答以下问题:
①已知砷是氮的同族元素,比氮原子多 2 个电子层,砷在元素周期表的位置为_____。
②工业上采用硫化法(通常用硫化钠)去除废水中的砷,生成物为难溶性的三硫化二砷,该反 应的离子方程式为_____。
(2)电镀厂的废水中含有的 CN-有剧毒,需要处理加以排放。处理含 CN-废水的方法之一是在 微生物的作用下,CN-被氧气氧化成 HCO3- ,同时生成 NH3,该反应的离子方程式为_____。
(3)电渗析法处理厨房垃极发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子, A―表示乳酸根离子):
①阳极的电极反应式为_____
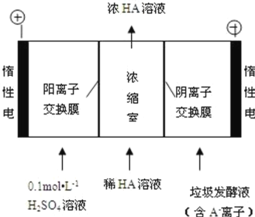
②电解过程中,采取一定的措施可控制阳极室的 pH 约为 6~8,此时进入浓缩室的 OH-可忽略不 计。400 mL 10 g·L-1 乳酸溶液通电一段时间后, 浓度上升为 145 g/L(溶液体积变化忽略不计),阴极上产生的 H2 在标准状况下的体积约为_____L (已知:乳酸的摩尔质量为 90 g/mol)。
高三化学综合题困难题查看答案及解析
-
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。
(1)硫酸厂的酸性废水中砷(As)元素(主要以 H3AsO3 形式存在)含量极高,为控制砷的排放, 某工厂采用化学沉淀法处理含砷废水。请回答以下问题:
①已知砷是氮的同族元素,比氮原子多 2 个电子层,砷在元素周期表的位置为_____。
②工业上采用硫化法(通常用硫化钠)去除废水中的砷,生成物为难溶性的三硫化二砷,该反 应的离子方程式为_____。
(2)电镀厂的废水中含有的 CN-有剧毒,需要处理加以排放。处理含 CN-废水的方法之一是在 微生物的作用下,CN-被氧气氧化成 HCO3- ,同时生成 NH3,该反应的离子方程式为_____。
(3)电渗析法处理厨房垃极发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子, A―表示乳酸根离子):
①阳极的电极反应式为_____
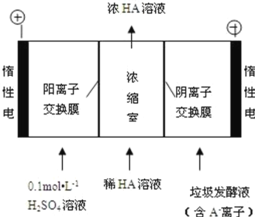
②电解过程中,采取一定的措施可控制阳极室的 pH 约为 6~8,此时进入浓缩室的 OH-可忽略不 计。400 mL 10 g·L-1 乳酸溶液通电一段时间后, 浓度上升为 145 g/L(溶液体积变化忽略不计),阴极上产生的 H2 在标准状况下的体积约为_____L (已知:乳酸的摩尔质量为 90 g/mol)。
高三化学综合题困难题查看答案及解析
-
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。
(1)硫酸厂的酸性废水中砷(As)元素(主要以H3AsO3形式存在)含量极高,为控制砷的排放,某工厂采用化学沉淀法处理含砷废水。请回答以下问题:
①已知砷是氮的同族元素,比氮原子多2个电子层,砷在元素周期表的位置为____________。
②工业上采用硫化法(通常用硫化钠)去除废水中的砷,生成物为难溶性的三硫化二砷,该反应的离子方程式为_____________________。
(2)电镀厂的废水中含有的CN-有剧毒,需要处理加以排放。处理含CN-废水的方法之一是在微生物的作用下,CN-被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为_____________。
(3)电渗析法处理厨房垃极发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子):
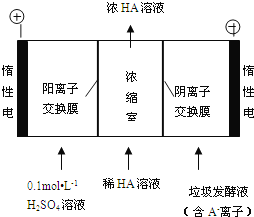
①阳极的电极反应式为________________________。
②简述浓缩室中得到浓乳酸的原理:________________________。
③电解过程中,采取一定的措施可控制阳极室的pH约为6~8,此时进入浓缩室的OH-可忽略不计。400 mL 10 g/L 乳酸溶液通电一段时间后,浓度上升为145 g/L(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为________L(提示:乳酸的摩尔质量为90 g/mol)。
高三化学综合题中等难度题查看答案及解析