-
(8分)实验室里常用浓盐酸跟高锰酸钾反应来制取少量氯气,反应的化学方程式为:2KMnO4 + 16HCl(浓)== 2KCl + 2MnCl2 + 5Cl2↑+ 8H2O
现用1L密度为1.19g/cm3、质量分数为36.5%的浓盐酸与一定质量的高锰酸钾反应,产生的氯气在标准状况下的体积为1.12L。
(1)计算反应中被氧化的HCl的物质的量。
(2)计算反应后溶液中H+的物质的量浓度。
高二化学计算题简单题查看答案及解析
-
实验室里常用浓盐酸跟高锰酸钾反应来制取少量氯气,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
现用1L密度为1.19g/cm3、质量分数为36.5%的浓盐酸与一定质量的高锰酸钾反应,产生的氯气在标准状况下的体积为1.12L.
(1)计算反应中被氧化的HCl的物质的量.
(2)计算反应后溶液中H+的物质的量浓度.高二化学解答题中等难度题查看答案及解析
-
实验室可以用高锰酸钾与浓盐酸反应制取氯气,反应的化学方程式如下:
2KMn04+16HCl(浓) = 2KCl+5Cl2↑+2MnCl2+8H20
对于该反应,下列说法正确的是
A.HCl是氧化剂 B.是非氧化还原反应
C.反应中锰元素被还原 D.反应中氢元素的化合价升高
高二化学选择题中等难度题查看答案及解析
-
实验室可以用高锰酸钾与浓盐酸反应制取氯气,反应的化学方程式如下:2KMn04+16HCl(浓) = 2KCl+5Cl2↑+2MnCl2+8H20
对于该反应,下列说法正确的是
A.HCl是氧化剂 B.是非氧化还原反应
C.反应中锰元素被还原 D.反应中氢元素的化合价升高
高二化学选择题中等难度题查看答案及解析
-
在实验室中,常用KMnO4代替MnO2与浓盐酸反应制取氯气,反应的化学方程式为2KMnO4+16HCl(浓)= 2MnCl2+5Cl2↑+2KCl+8H2O,下列叙述中正确的是( )
A. 反应中KMnO4被氧化
B. HCl发生还原反应
C. 每消耗2mol HCl时,反应中转移的电子为2 mol
D. 氧化剂与还原剂的物质的量之比为1﹕5
高二化学单选题中等难度题查看答案及解析
-
实验室通常用二氧化锰和浓盐酸反应制取氯气写出反应方程式______________,浓盐酸还可以和氯酸钾发生反应制取氯气写出反应方程式______________,氯气具有较强的__________性。
高二化学填空题简单题查看答案及解析
-
实验室可用氯酸钾与浓盐酸反应制取氯气,该反应的化学方程式为:
KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑
现将24.5g KClO3跟150mL 12mol/L(过量)盐酸充分反应,求:
(1)生成的Cl2在标准状况下体积为多少升?
(2)将反应后混合液稀释至500mL,此时溶液中Cl-的物质的量浓度为多少?(KClO3摩尔质量为122.5g/mol)]
高二化学计算题中等难度题查看答案及解析
-
实验室用一定量MnO2固体与足量浓盐酸在加热条件下充分反应制取2.24L标准状况下的氯气,其反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,,(相对原子质量O-16,Mn-55)
试计算:
(1)参加反应的MnO2的质量____________;
(2)反应后溶液的体积为100mL,溶液中MnCl2的物质的量浓度____________。
高二化学计算题简单题查看答案及解析
-
实验室通常用氧化剂+浓盐酸→金属氯化物+水+氯气的原理制取少量Cl2。现将一定质量的NaClO放入50mL 12.00mol·L-1的浓盐酸中,生成的Cl2在标准状况下的体积为1.12L。试计算(反应前后溶液的体积变化忽略不计):
(1)反应过程中,被氧化的HCl的物质的量为 mol
(2)反应后溶液中HCl的物质的量浓度为 mol·L-1。
高二化学填空题困难题查看答案及解析
-
(18分)氯气在科技、生产中应用广泛。
(1)工业上常用熟石灰和氯气反应制取漂白粉,化学方程式是___ 。
(2)实验室用MnO2与浓盐酸反应制取氯气的过程中,可用NaOH溶液吸收尾气,下列试剂也可用于吸收氯气的是____(填字母)。
a.KI溶液 b.FeCl2溶液 c.KCl溶液
写出你选择的一种吸收试剂与Cl2反应的离子方程式:____ 。
也可用浓氨水吸收氯气,同时生成一种无污染的气体,反应的化学方程式是____ 。
(3)以粗盐为原料制备亚氯酸钠(NaClO2)的工艺流程如下
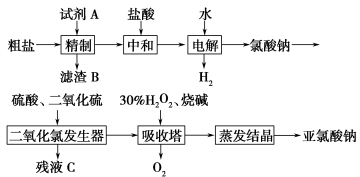
写出二氧化氯发生器中生成二氧化氯的离子方程式 。
(4)FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:

a.检验装置的气密性;
b.通入干燥的Cl2,赶尽装置中的空气;
c.用酒精灯在铁屑下方加热至反应完成;
d.在沉积的FeCl3固体下方加热
e.体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封。
请回答下列问题:
①装置D中FeCl2的作用是 ,写出检验FeCl3的离子方程式 。
②画出尾气吸收装置E并注明试剂。
③该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫,FeCl3与H2S反应的离子方程式为________________ 。
高二化学填空题困难题查看答案及解析