-
下表是元素周期表的一部分,根据表中给出的①—⑥六种元素,回答下列问题:
| 族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | | | | ① | | | ② | |
| 3 | ③ | ④ | | | | ⑤ | ⑥ | |
(1)画出元素④的原子结构示意图__________;
(2)元素①形成的最简单有机物的化学式是__________;
(3)表中所列元素中非金属性最强的元素是__________(填元素符号)
(4)元素⑤形成的最高价氧化物对应的水化物的化学式是__________;
(5)元素③和元素⑥形成的化合物的电子式是__________。
-
下表是元素周期表的一部分,根据表中给出的①—⑥六种元素,回答下列问题:
| 族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | | | | ① | | | ② | |
| 3 | ③ | ④ | | | | ⑤ | ⑥ | |
(1)画出元素④的原子结构示意图__________;
(2)元素①形成的最简单有机物的化学式是__________;
(3)表中所列元素中非金属性最强的元素是__________(填元素符号)
(4)元素⑤形成的最高价氧化物对应的水化物的化学式是__________;
(5)元素③和元素⑥形成的化合物的电子式是__________。
-
下表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题。
| 
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | C | N | O | F | |
| 3 | Na | Mg | Al | | | S | Cl | Ar |
(1)非金属性最强的元素是 ;
(2)化学性质最不活泼的单质是 ;
(3)C和O中,原子半径较大的是 ;
(4)某离子的结构示意图为 ,该离子的符号为__________;
,该离子的符号为__________;
(5)硫有两种重要氧化物,分别为SO2和 (填化学式);
(6)H2S和HCl中,热稳定性较强的是 ;
(7)NaOH、Mg(OH)2、Al(OH)3中,碱性最强的是 ;属于两性氢氧化物的是 ;
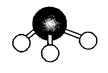
(8)氮的一种气态氢化物的分子球棍模型如图所示,写出它的化学式 ,其水溶液显 (填“酸性”或“碱性”),此氢化物中N元素和H元素的质量比m(N)∶m(H)= ;
(相对原子质量:N一14 H—1)
-
下表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | C | N | O | F | Ne |
| 3 | Na | | Al | | P | S | Cl | |
(1)单质的化学性质最不活沷的元素是__________;
(2)氧的原子结构示意图是__________;
(3)形成化合物种类最多的元素是__________;
(4)HF和H2O中,热稳定性较强的是__________;
(5)N和P中,原子半径较小的是__________;
(6)常温下,会在浓硫酸中发生钝化的金属是_________;
(7)元素最高价氧化物对应水化物中,碱性最强的是___(填化学式),酸性最强的是_____(填“H2SO4”或“ HClO4”);
-
(13分)下表为元素周期表中前四周期的部分元素(从左到右按原子序数递增排列,部分涉及到的元素未给出元素符号),根据要求回答下列各小题:
(1)在以上表格中所有元素里基态原子的电子排布中4s轨道上只有1个电子的元素有 (填元素名称)。
(2)根据元素原子的外围电子排布的特征,可将元素周期表前四周期元素分成4个区域,分别为s区、p区、d区、ds区,,则属于s区的元素有 种,属于d区的元素有 种。第二周期元素中除Ne外电负性由高到低的三种元素依次是 ,电离能由高到低的三种元素依次是 。
(3)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
| 元素 | Mn | Fe |
| 电离能 ( kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 |
| I3 | 3248 | 2957 |
回答下列问题:
Mn元素的电子排布式为____________________________________,
Fe2+的电子排布图为__________________________
比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个 电子难。对此,你的解释是:_____________________________
【解析】(1)考查元素周期表的结构和原子核外电子的排布规律。根据构造原理可知4s轨道上只有1个电子的元素是K、Cr和 Cu。
(2)除ds区外,区的名称来自于构造原理最后填入电子的能级的符号,即s区包括第IA和ⅡA,共2列。p区包括第ⅢA到第 ⅦA以及0族,共6列。D区包括第3列到第10列,共8列。ds区包括第11和12列,共2列。非金属性越强,电负性越大,第一电离能也越大,非金属性是Cl>S>P,所以电负性是Cl>S>P。由于P原子的3p轨道属于半充满,属于第一电离能是Cl>P>S。
(3)根据构造原理可以写出锰元素的电子排布,即1s22s22p63s23p63d54s2,Fe2+的电子排布图为1s22s22p63s23p63d6。由于Mn2+的3d轨道属于半充满,比较稳定,所以再失去1个电子所需要的能量就高。而Fe2+的3d轨道上有6个电子,Fe3+的3d轨道上有5个电子,属于不充满比较稳定,因此3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少。
-
如图为元素周期表的一部分,请针对给出的5种元素回答下列问题:

(1)元素①的原子结构示意图为:______.
(2)第二周期标出的元素中最高价氧化物对应的水化物酸性较强的是______(填元素符号);④⑤两种元素的离子氧化性较强的是______(填离子符号).
(3)请写出元素⑤的氢氧化物和稀盐酸反应的离子方程式______.
-
下面用序号给出了周期表中的部分元素,请从①~⑧中选择合适的元素回答下列问题:
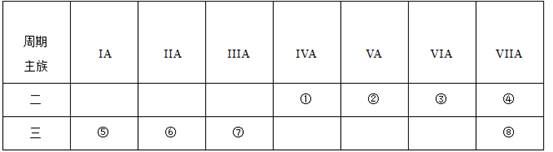
(1)上述元素中原子半径最大的是(填元素符号) ,气态氢化物最稳定的是(填化学式,下同) ,气态氢化物水溶液呈碱性的是 ,最高价氧化物对应水化物酸性最强的是 .
(2)元素①与③按原子个数1:2构成的分子的电子式为 .
(3)元素⑤和⑦的最高价氧化物对应水化物反应的离子方程式为 .
-
下表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答下列问题。

(1)元素④的符号是 ;
(2)⑤和⑥两种元素原子半径的大小关系:⑤ ⑥(填“>”或“<”);
(3)①和②两种元素金属性强弱关系:① ②(填“>”或“<”);
(4)①的最高价氧化物的水化物与元素③的单质反应的化学方程式为:________ _______。
-
下表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答下列问题.

(1)元素④的符号是 ;
(2)⑤和⑥两种元素原子半径的大小关系:⑤ ⑥(填“>”或“<”);
(3)①和②两种元素金属性强弱关系:① ②(填“>”或“<”);
(4)①的最高价氧化物的水化物与元素③的单质反应的化学方程式为: .
-
下表为元素周期表的一部分。请回答下列问题:
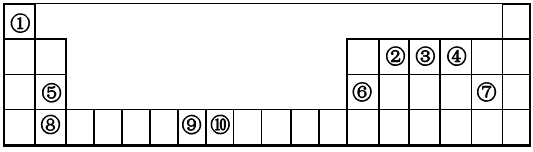
根据元素在周期表中的相对位置可知①~⑩分别是H、C、N、O、Mg、Al、Cl、Ca、Mn、Fe。
(1)上述元素中,属于s区的是____________(填元素符号)。
(2)写出元素④的基态原子的价电子排布图____________________。
(3)元素第一电离能为⑨________⑩ (填“大于”或“小于”)。
(4)元素③气态氢化物的VSEPR模型为________;该分子为________分子(填“极性”或“非极性”)。向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为_____________________________。
(5)⑥单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
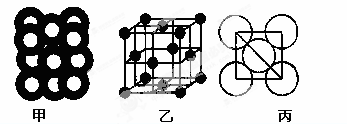
若已知⑥的原子半径为dcm,NA代表阿伏加德罗常数,元素⑥的相对原子质量为M,请回答:晶胞中⑥原子的配位数为________,该晶体的密度为________(用字母表示)
(6)实验证明:⑤和⑧的氧化物、KCl、TiN这4种晶体的结构与NaCl晶体结构相似(如下图所示),已知3种离子晶体的晶格能数据如下表:
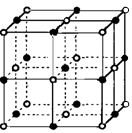
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:________(用化学式填写)。
其中⑧的氧化物晶体中一个阳离子周围和它最邻近且等距离的阳离子有________个。
 ,该离子的符号为__________;
,该离子的符号为__________;






