-
下列图像与所对应的叙述正确的是
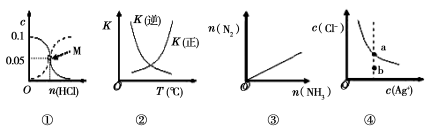
A.图①表示室温下,用0.1 mol•L-1的氨水吸收HCl气体时,溶液中的粒子浓度随HCl体积的变化。实现表示c(NH3·H2O),虚线表示c(NH4+),处于M点时溶液呈中性
B.图②表示2SO2(g)+O2(g)  2SO3(g)△H<0,正逆反应的平衡常数随温度的变化
2SO3(g)△H<0,正逆反应的平衡常数随温度的变化
C. 图③表示2NH3(g) N2(g) +3H2(g),在恒温恒压的密闭容器中达平衡时N2的物质的量随的 NH3物质的量的变化
N2(g) +3H2(g),在恒温恒压的密闭容器中达平衡时N2的物质的量随的 NH3物质的量的变化
D. 图④表示AgCl(s) Ag+(aq) +Cl-(aq)的离子浓度关系,当处于b点时,蒸发部分水后,可到达平衡线的a点
Ag+(aq) +Cl-(aq)的离子浓度关系,当处于b点时,蒸发部分水后,可到达平衡线的a点
-
下列坐标图均涉及平衡原理,其中相关表述正确的是( )

A.图①表示室温下,用0.1mol·L-1氨水吸收HCl气体时,溶液的粒子浓度随吸收HCl的变化,实线表示c(NH3·H2O),虚线表示c(NH4+),处于M点时溶液呈中性
B.图②表示2SO2(g)+O2(g)  2SO3(g) △H<0正逆反应的平衡常数K随温度的变化
2SO3(g) △H<0正逆反应的平衡常数K随温度的变化
C.图③表示反应2NH3(g)  3H2(g)+N2(g)在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
3H2(g)+N2(g)在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
D.图④表示AgCl(s)  Ag+(aq)+Cl-(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
Ag+(aq)+Cl-(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
-
下列坐标图均涉及平衡原理,其中相关表述正确的是( )

A.图①表示室温下,用0.1mol·L-1氨水吸收HCl气体时,溶液的粒子浓度随吸收HCl的变化,实线表示c(NH3·H2O),虚线表示c(NH4+),处于M点时溶液呈中性
B.图②表示2SO2(g)+O2(g)  2SO3(g) △H<0正逆反应的平衡常数K随温度的变化
2SO3(g) △H<0正逆反应的平衡常数K随温度的变化
C.图③表示反应2NH3(g)  3H2(g)+N2(g)在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
3H2(g)+N2(g)在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
D.图④表示AgCl(s)  Ag+(aq)+Cl-(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
Ag+(aq)+Cl-(aq)的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
-
用AG表示溶液酸度:AG = lg 。在室温下,用0.1 mol/L的HCl溶液滴定20.00mL0.1mol/L氨水。滴定结果可表示如下图: 下列分析正确的是
。在室温下,用0.1 mol/L的HCl溶液滴定20.00mL0.1mol/L氨水。滴定结果可表示如下图: 下列分析正确的是
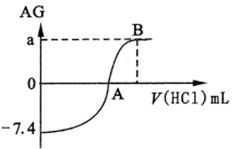
A. 0. lmol/L 氨水 pH = 10.2
B. A点加入盐酸的体积为20. 00mL
C. 若a=7,从A到B水的电离程度逐渐减小
D. B点溶液中可能存在c(Cl-)>c(NH4+ )>(H+)>c(OH-)
-
已知: 。室温下,向浓度为0.1mol·L-1的氨水中缓缓通入HCl,
。室温下,向浓度为0.1mol·L-1的氨水中缓缓通入HCl, 随pOH的变化曲线如下图所示。假设溶液体积没有变化,下列推断正确的是( )
随pOH的变化曲线如下图所示。假设溶液体积没有变化,下列推断正确的是( )
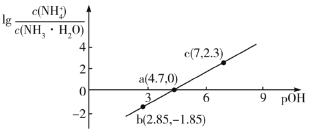
A.NH3·H2O的电离常数的数量级为10-4
B.b点溶液中:
C.c点溶液中:
D.pOH=8的溶液中:
-
室温下,将盐酸和氨水等体积混合(忽略体积变化),实验数据如下表:
| 实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH |
| c(氨水) | c(HCl) |
| ① | 0.1 | 0.1 | 5 |
| ② | 0.2 | x | 7 |
下列判断错误的是
A.实验②反应后的溶液中:c(NH4+)+c(NH3·H2O)>0.1 mol/L
B.实验①反应后的溶液中:c(H+)= c(Cl-)+c(OH-)-c(NH4+)
C.实验①反应后的溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.实验②反应后的溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+)
-
常温下,0.1 mol/L氨水溶液中 =1×10-8,下列叙述不正确的是( )
=1×10-8,下列叙述不正确的是( )
A.该溶液中氢离子的浓度:c(H+)=1×10-11 mol/L
B.0.1 mol/L氨水溶液与0.1 mol/L HCl溶液等体积混合后所得溶液中:c(N )+c(H+)=c(Cl-)+c(OH-)
)+c(H+)=c(Cl-)+c(OH-)
C.0.1 mol/L的氨水溶液与0.05 mol/L H2SO4溶液等体积混合后所得溶液中:c(N )+c(NH3)+c(NH3·H2O)=2c(S
)+c(NH3)+c(NH3·H2O)=2c(S )
)
D.浓度均为0.1 mol/L的NH3·H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(N )>c(NH3·H2O)>c(Cl-)>c(OH-)>c(H+)
)>c(NH3·H2O)>c(Cl-)>c(OH-)>c(H+)
-
常温下,0.1 mol/L氨水溶液中 =1×10-8,下列叙述不正确的是( )
=1×10-8,下列叙述不正确的是( )
A.该溶液中氢离子的浓度:c(H+)=1×10-11 mol/L
B.0.1 mol/L氨水溶液与0.1 mol/L HCl溶液等体积混合后所得溶液中:c(N )+c(H+)=c(Cl-)+c(OH-)
)+c(H+)=c(Cl-)+c(OH-)
C.0.1 mol/L的氨水溶液与0.05 mol/L H2SO4溶液等体积混合后所得溶液中:c(N )+c(NH3)+c(NH3·H2O)=2c(S
)+c(NH3)+c(NH3·H2O)=2c(S )
)
D.浓度均为0.1 mol/L的NH3·H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(N )>c(NH3·H2O)>c(Cl-)>c(OH-)>c(H+)
)>c(NH3·H2O)>c(Cl-)>c(OH-)>c(H+)
-
常温下,0.1mol/L氨水溶液中 =1×10-8,下列叙述不正确的是
=1×10-8,下列叙述不正确的是
A.该溶液中氢离子的浓度:c(H+)=1×10-11mol/L
B.0.1mol/L氨水溶液与0.1mol/L HCl溶液等体积混合后所得溶液中:c(NH+4)+c(H+)=c(Cl—)+c(OH+)
C.0.1mol/L的氨水溶液与0.05mol/L H2SO4溶液等体积混合后所得溶液中:c(NH+4)+c(NH3)+c(NH3·H2O)=2c(SO2—4)
D.浓度均为0.1mol/L的NH3·H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(NH4+)>c(NH3·H2O)>c(Cl-)>c(OH-)>c(H+)
-
今有室温下四种溶液,有关叙述不正确的是
| ① | ② | ③ | ④ |
| 浓度c/mol/L | 0.1 | 0.1 | 0.1 | 0.1 |
| 溶液 | 氨水 | CH3COONa溶液 | 醋酸 | 盐酸 |
A.在20mL①溶液中逐滴加入③溶液,溶液导电能力变化如下图(1)所示
B.②、③两溶液等体积混合,离子浓度:2c(Na+)=c(CH3COO-)+c(CH3COOH)
C.用③滴定①,用酚酞作指示剂,滴定曲线如下图(2)所示:

D.①、④两溶液等体积混合,离子浓度:c(Cl-)>c(NH4+)>c(H+)>c(OH-)

2SO3(g)△H<0,正逆反应的平衡常数随温度的变化
N2(g) +3H2(g),在恒温恒压的密闭容器中达平衡时N2的物质的量随的 NH3物质的量的变化
Ag+(aq) +Cl-(aq)的离子浓度关系,当处于b点时,蒸发部分水后,可到达平衡线的a点




