-
(10分)下表是元素周期表的一部分,表中字母分别代表某一化学元素,请回答有关问题。

(1)人们曾认为g、h、i不发生化学反应,因而把它们叫做稀有气体,但是后来发现这族气体可以参加化学反应,你认为g、h、i中最有可能首先被发现可以参加化学反应的元素是_______(写元素符号);g、h、i第一电离能由大到小的顺序为______。(用元素符号表示)
(2)e元素原子结构示意图为_______________。d元素原子核外电子排布式为_______________。
(3)a的阴离子半径____________b的阳离子半径(填大于、等于、小于)。
(4)在元素周期表中有一个对角线规则,其中包括b、c的化合物的性质十分相似。则b的氯化物分别与少量和过量的氢氧化钠溶液发生反应的离子方程式分别为(要表达出具体的元素符号,下同)______ _________________________;___________________________________。
(5)f的+4价氧化物可与浓盐酸反应,且已知其氧化性强于氯气,则该氧化物与浓盐酸反应的化学方程式可表示为______________________________________________。
(6)元素周期表中第6周期中的镧系元素共有________种,它们原子的电子层结构和性质十分相似。
(7)元素k的氢化物乙可由两种10个电子的微粒组成的化合物甲(化学式X3Y2)与水剧烈反应能生成。甲与水反应的化学反应方程式为:_______。
-
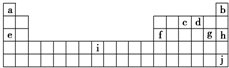
下表是元素周期表的一部分,表中所列字母分别代表十种化学元素,就表中字母所代表的元素回答下列问题.
(1)铅(原子序数为82)从单质到其化合物都有着广泛的应用,如制造焊锡、铅蓄电池、化工耐酸设备以及X射线的防护材料等.铅的氧化物主要有三种:PbO、PbO2和Pb3O4.请回答下列问题:
①铅位于元素周期表中第______周期第______族;
②PbO2是一种两性氧化物,试写出PbO2和NaOH浓溶液反应的离子方程式:______.
(2)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图______.
(3)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑.请预测首先被用来与F2反应制备稀有气体化合物的元素是______(填写字母).利用稀有气体化合物,人们实现了许多制备实验上的突破.如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式______ 3NaBrO4+Xe
-
【化学一物质结构与性质】(15分)
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素n的基态原子的价电子排布式 ,元素O在周期表的位置是 ,属于 区。
(2)k在空气中燃烧产物的分子构型为 ,中心原子的杂化方式为 ,该分子是 (填“极性”或“非极性”)分子。
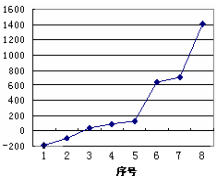
(3)第三周期8种元素按单质熔点高低的顺序如左下图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填下图中的序号)。
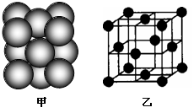
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如右下图乙所示。则晶胞中i原子的配位数为 。
-
(物质结构与性质)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
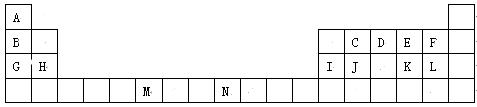
试回答下列问题:
(1)请写出元素N的基态原子电子排布式 。
(2)元素B、G形成的单质熔点更高的是_ ___(填化学式),原因是____ _
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是__________(填“极性”或“非极性”)分子。
(4)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有___________(填序号),CS2分子的空间构型是__________。
(5)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为 。
-
[化学一选修3物质结构与性质]
下表为长式周期表的一部分,其中的字母A--J分别代表对应的10种元素.
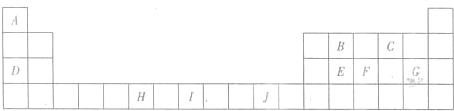
请回答下列问题:
(1)元素I的原子结构示意图为______.
(2)B、E两元素分别与元素C按原子个数比为1:2形成化合物时,中心原子的杂化方式分别为______和______,这两种化合物的熔沸点差别很大的原因是______.
(3)H3+离子在一定条件下能形成结构复杂的配离子[HG(A2C)5]2+形成该配离子时,H3+离子接受了配体提供的______.该配离子中含有的化学键类型是______,其中G的核外电子排布式为______.
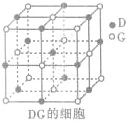
(4)元素D与元素G形成的化合物DG的晶胞结构如图所示,每个D离子周围与之最近的D离子的个数为______.若设该晶胞的棱长为a cm,阿伏加德罗常数的值为NA,则该化合物的密度为______.
-
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
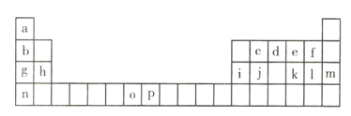
试回答下列问题:
(1)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_____ 。
(2)o、p两种元素的部分电离能数据如下表所示:
| 元素 | o | p |
| 电离能/ | 
| 717 | 763 |
| 
| 1509 | 1561 |
| 
| 3248 | 2957 |
比较两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是 ___________。
再失去一个电子难。对此,你的解释是 ___________。
(3)表中所列的某主族元素的电离能情况如图所示,则该元素是上述元素中的____(填元素符号)。

-
图是元素周期表中的一部分,表中所列字母分别代表一种化学元素,请回答下列问题:
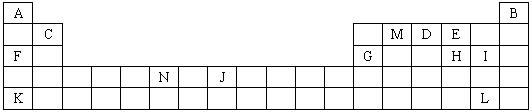
(1)上述所列元素的原子中,最外层电子层上只有两个电子的是______;(填“元素符号”)
(2)下列叙述正确的是______;(填字母序号)
a.K的最高价氧化物对应的水化物是一种强碱
b.硒化氢的稳定性强于H的氢化物的热稳定性
c.F与H形成化合物水溶液的pH大于F与I形成化合物水溶液的pH,说明相同浓度氢化物水溶液的酸性H弱于I
d.MA2E分子中M原子采取SP2杂化方式
e.N的电子排布式:ls22s22p63s23p63d44s2
f.电负性由大到小的顺序:E>D>M
g.第一电离能由大到小的顺序:E>D>M
(3)预测DA4+离子的空间构型为______,ME2的空间构型为______;
(4)向含有CoCl3•5NH3的溶液中加入硝酸银溶液,可析出AgCl沉淀.经测定,每1mol CoCl3•5NH3只生成2molAgCl.
请写出表示此配合物结构的化学式(钴的配位数为6):______,此配合物中Co的化合价为______.
-
下表是元素周期表的一部分.表中所列的字母分别代表某一化学元素.
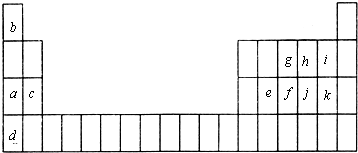
请你根据表中所给元素,回答下列问题:
(1)在短周期的所有元素中______的原子半径与______的原子半径之比最小(不包括稀有气体)(填元素符号).
(2)该表中金属性最强的元素与氧气反应生成化合物的化学式是______(填两种即可).
(3)海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,其单质做消毒杀菌剂的原因是______(用化学方程式表示).
(4)写出分别由a、b、h、j四种元素所形成的两种化合物的水溶液相互反应的离子方程式______.
(5)常温下某液态化合物只含上述元素中的两种,分子中原子个数比1:1,请你仅用一个化学方程式表示该液态化合物既有氧化性又有还原性______ 2H2O+O2↑
-
下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。

请你根据表中所给元素,回答下列问题:
(1)在短周期的所有元素中________的原子半径与________的原子半径之比最小(不包括稀有气体)(填元素符号)。
(2)金属性最强的元素与氧气反应生成化合物的化学式是________(填两种即可),j和k氢化物比较,稳定性强的是________(填写氢化物化学式)。
(3)海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,其单质做消毒杀菌剂的原因是________(用化学方程式表示)
(4)常温下某液态化合物只含上述元素中的两种,分子中原子个数比1:1,请你仅用一个化学方程式表示该液态化合物既有氧化性又有还原性________。
-
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)元素p为26号元素,请写出其原子的三价阳离子的电子排布式:______________。
(2)e与a反应的产物的分子中中心原子的杂化形式为__________,该分子是__________(填“极性”或“非极性”)分子。
(3)请写出f的氢化物在水中所存在氢键的表达式:(任写两种即可)_________________________。
(4)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p |
| 电离能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 |
| I3 | 3 248 | 2 957 |
| | | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是___________________________________;
(5)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
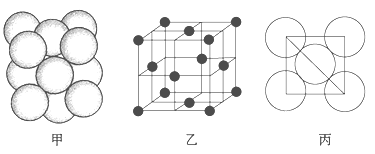
请问晶胞中i原子的配位数为________,一个晶胞中i原子的数目为________。













