在平衡体系2SO2(g)+O2(g)2SO3(g)(正反应为放热反应),能使SO3的产量增加的措施是( )
A、升高温度 B、加入催化剂 C、降低压强 D、通入氧气
高二化学选择题简单题
在平衡体系2SO2(g)+O2(g)2SO3(g)(正反应为放热反应),能使SO3的产量增加的措施是( )
A、升高温度 B、加入催化剂 C、降低压强 D、通入氧气
高二化学选择题简单题
在平衡体系2SO2(g)+O2(g)2SO3(g)(正反应为放热反应),能使SO3的产量增加的措施是( )
A、升高温度 B、加入催化剂 C、降低压强 D、通入氧气
高二化学选择题简单题查看答案及解析
对于在一固定容积容器中发生的反应:2SO2(g)+ O2(g)2SO3(g)(正反应为放热反应),下列措施中,既可加快反应速率,又可使平衡向右移动的是
A.降温 B.减压 C.加催化剂 D.增加O2
高二化学选择题简单题查看答案及解析
高二化学选择题中等难度题查看答案及解析
对于反应2SO2(g)+O2(g)2SO3(g) △H<0,下列措施中,既能使正反应速率增大又能使平衡正向移动的是
A.通入大量的SO2 B.增大容积的体积
C.移去部分SO3 D.升高体系的温度
高二化学单选题中等难度题查看答案及解析
工业上制硫酸的主要反应之一为2SO2(g)+O2(g)2SO3(g),反应过程中能量的变化如图所示。
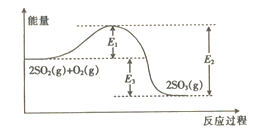
(1)由图可知该反应的正反应为_____________(填“吸热”或“放热”)反应。
(2)升高温度,平衡向_________(填“正反应”或“逆反应”)方向移动;正反应速率_____(填“增大”“减小”或“不变”,下同),逆反应速率_____________。
(3)向反应体系中加入催化剂后,图中E1____(填“增大”“减小”或“不变”,下同),E3___________。
(4)已知:2H2S(g)+O2(g)=2S(s)+2H2O(g) △H=-442.4 kJ·mol-1;
S(s)+O2(g)=SO2(g) △H=-297.0 kJ • mol-1。
则H2S(g)与O2(g)反应产生SO2(g)和H2O(g)的热化学方程式是_________________,当此反应转移3 mol电子时,放出的热量为_______kJ。
高二化学填空题中等难度题查看答案及解析
对于反应2SO2(g)+O2(g)2SO3(g),能增大正反应速率的措施是( )
A.移去部分SO3 B.增大容器的体积
C. 通入大量O2 D.升高体系温度
高二化学选择题简单题查看答案及解析
高二化学选择题中等难度题查看答案及解析
硫酸生产中炉气转化反应为2SO2(g)+O2(g)2SO3(g)。研究发现,SO3的体积分数 (SO3%)随温度(T)的变化如曲线I所示。下列判断不正确的是
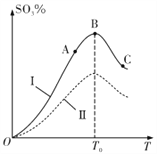
A. 该反应的正反应为放热反应
B. 曲线I上A、C两点反应速率的关系是:VA<VC
C. 反应达到B点时,2V正(O2) = V逆(SO3)
D. 已知V2O5的催化效果比Fe2O3好,若I表示用V2O5作催化剂的曲线,则Ⅱ可表示用Fe2O3作催化剂的曲线
高二化学选择题中等难度题查看答案及解析
针对平衡2O2(g)+O2(g) 2SO2(g),采用下列措施一段时间后,能增大逆反应速率的是( )
A.通入大量O2 B.增大容器容积 C.移去部分SO3 D.降低体系温度
高二化学选择题简单题查看答案及解析
硫酸生产中存在炉气转化反应:2SO2(g)+O2(g)2SO3(g)。研究发现,SO3的体积分数随温度(T)的变化如曲线I所示。下列判断正确的是
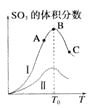
A.该反应的正反应为吸热反应
B.反应达到B点时,2υ正(O2)=υ逆(SO3)
C.曲线I上A、C两点反应速率的关系:υA>υC
D.已知V2O5的催化效果比Fe2O3好,若I表示用V2O5作催化剂时的曲线,则II是Fe2O3作催化剂时的曲线
高二化学单选题中等难度题查看答案及解析