-
燃烧热是指在25℃,101kPa,1 mol可燃物完全燃烧生成稳定的化合物时放出的热量。已知热化学方程式:①CO(g)+1/2 O2(g)== CO2(g) ΔH = -283.0 kJ·mol-1
②H2(g)+ 1/2O2(g)== H2O(g) ΔH = -241.8 kJ·mol-1
则下列说法正确的是
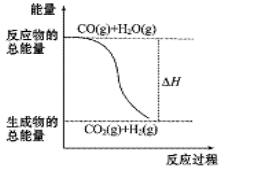
A.H2的燃烧热为241.8 kJ·mol-1
B.由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)  CO2(g)+H2(g) ΔH = -41.2 kJ·mol-1
CO2(g)+H2(g) ΔH = -41.2 kJ·mol-1
C.H2(g)转变成H2O(g)的化学反应一定要释放能量
D.根据②推知反应H2(g)+1/2O2(g)==== H2O(l) ΔH > -241.8 kJ·mol-1
-
已知25 ℃、101 kPa下,含1 mol碳原子的石墨完全燃烧生成CO2放出热量393.51 kJ;含1 mol碳原子的金刚石完全燃烧生成CO2放出395.41 kJ的热量。据此判断,下列说法正确的是( )
A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
-
直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(1)101 kPa时,1 mol CH3OH完全燃烧生成稳定的氧化物放出热量726.51 kJ/mol,则甲醇燃烧的热化学方程式为 ________ 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=+49.0 kJ·mol-1
②CH3OH(g)+ O2(g)= CO2(g)+2H2(g) △H2
O2(g)= CO2(g)+2H2(g) △H2
已知H2(g)+ O2(g)=H2O(g) △H =-241.8 kJ·mol-1
O2(g)=H2O(g) △H =-241.8 kJ·mol-1
则反应②的△H2= kJ·mol-1。
(3)甲醇燃料电池的结构示意图如右。甲醇进入 极(填“正”或“负”),正极发生的电极反应式为 ________ 。负极发生的电极反应式为 ________ 。
-
(1)肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。已知在101 kPa,320 g N2H4在氧气中完全燃烧生成氮气,放出热量624 kJ(25 ℃时),N2H4完全燃烧的热化学方程式是:
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。肼—空气燃料电池放电时,正极的电极反应式是 ;负极的电极反应式是 。
(3)如图是一个电化学过程示意图。
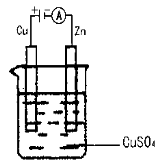
假设使用肼—空气燃料电池作为本过程的电源,铜片质量变化128 g,则肼—空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气的体积含量为20%)。
(4)传统制备肼的方法是以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是 。
-
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa、25℃时,16 gN2H4在氧气中完全燃烧生成氮气,放出热量312 kJ。N2H4完全燃烧反应的热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气 燃料电池放电时:正极的电极反应式是 。负极的电极反应方程式是 。
燃料电池放电时:正极的电极反应式是 。负极的电极反应方程式是 。
(3)下图是一个电化学过程示意图。
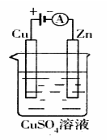
① 锌片上发生的电极反应方程式是 。
② 假设使用肼—空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气体积含量为20%)
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式是 。
(5)将0.3 mol AgNO3、0.4 mol Cu(NO3)2和0.1mol KCl溶于水配成100 mL溶液,用惰性电极电解一段时间后,当阴极生成0.1mol气体时,此时,另一极上的气体体积(标准状况)为 。
Cu(NO3)2和0.1mol KCl溶于水配成100 mL溶液,用惰性电极电解一段时间后,当阴极生成0.1mol气体时,此时,另一极上的气体体积(标准状况)为 。
-
已知:25℃、101kPa时,(1)12g石墨不完全燃烧生成CO,放出110.5kJ热量,CO继续燃烧又放出283.0kJ热量;(2)金刚石燃烧的热化学方程式为:
C(金刚石,s)+O2(g) CO2(g);△H=-395.0kJ·mol-1.下列说法中正确的是
A.由石墨制备金刚石是放热反应
B.等质量时,金刚石所具有的能量比石墨所具有的能量低
C.CO燃烧的热化学方程式为: 2CO(g)+O2(g) 2CO2(g);△H=-283.0kJ·mol-1
D.石墨燃烧的热化学方程式为:C(石墨,s)+O2(g) =CO2(g);△H=-393.5kJ·mol-1
-
(8分)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4的燃烧热化学方程式是 。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。
肼—空气燃料电池放电时:负极的电极反应式是 。
(3)电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O,充电时:阳极反应式: 用此装置电解水和重水(D2O)组成的混合液(两电极均是Pt),通电一段时间后,在两极共收集到33.6 L(标准状况)气体,总质量为18.5 g,则混合气体中H原子和D原子个数之比:
2PbSO4+2H2O,充电时:阳极反应式: 用此装置电解水和重水(D2O)组成的混合液(两电极均是Pt),通电一段时间后,在两极共收集到33.6 L(标准状况)气体,总质量为18.5 g,则混合气体中H原子和D原子个数之比:
-
(1)在101 kPa时,1 mol CH4完全燃烧生成CO2和液态水,放出890 kJ的热量。
①CH4的燃烧热为___,表示燃烧热的热化学方程式为_____________;
②1 000 L CH4(标准状况)燃烧后所产生的热量为_____。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g) ΔH= -574kJ·mol-1,CH4(g)+4NO(g)
4NO(g)+CO2(g)+2H2O(g) ΔH= -574kJ·mol-1,CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g) ΔH= -1 160 kJ·mol-1。写出CH4将NO2还原为N2的热化学方程式:_______________。
2N2(g)+CO2(g)+2H2O(g) ΔH= -1 160 kJ·mol-1。写出CH4将NO2还原为N2的热化学方程式:_______________。
-
已知:在25 oC 101KPa时
①1g氢气完全燃烧生成气态水放出120.9 KJ的热量
②2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol
③Na2O2(s)+CO2(g)=Na2CO3(s)+ ΔH=-226 kJ/mol
ΔH=-226 kJ/mol
在相同条件下根据以上信息回答下列问题:
(1)请书写氢气完全燃烧生成气态水的热化学方程式_______________________________。
(2)CO的燃烧热为ΔH=_____。
(3)请写出Na2O2(s)与CO(g)反应生成Na2CO3(s)的热化学方程式_______________________。
(4)请计算CO(g)与Na2O2(s)反应放出1018kJ热量时,转移电子的物质的量__________________。
-
(6分)Ⅰ、已知在101 kPa时,CH4完全燃烧生成1mol液态水,放出的热量为QkJ,则CH4完全燃烧反应的热化学方程式是:________。
Ⅱ、在铜片、锌片和400 mL稀硫酸组成的原电池中,若电路中通过0.2 mol电子,H2SO4恰好反应完毕。试计算:
(1)生成气体的体积(在标准状况下);
(2)原400 mL稀硫酸的物质的量浓度(不考虑溶液的体积变化)。

CO2(g)+H2(g) ΔH = -41.2 kJ·mol-1

