-
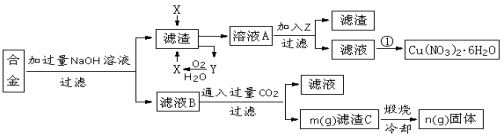
(本题共12分)某兴趣小组用合金铝、铁、铜的废弃合金为原料制取硝酸铜晶体和氢氧化铝,并测定硝酸铜晶体的结晶水含量和氢氧化铝的纯度,设计的主要流程如下:
已知:
Fe2+沉淀的pH范围为7.0~9.0;Fe3+沉淀的pH范围为1.9~3.2;Cu2+沉淀的pH范围为4.7~6.7
回答下列问题:
1.写出合金中加入NaOH溶液后所发生的离子反应方程式_______________________。试剂X的名称为______________。
2.加入Z的作用是调节溶液的pH,pH范围应为_____;下列可作为试剂Z的是_______。
a.铜粉 b.氨水 c.氧化铜 d.硫酸铜
3.实验操作①依次是_________、_________、过滤洗涤即可得硝酸铜晶体。
4.测定硝酸铜晶体的结晶水含量,下列方案中肯定不可行的是 。(选填编号)
a.称量样品→加热→冷却→称量CuO
b.称量样品→加热→冷却→称量Cu(NO3)2
c.称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量
d.称量样品→加过量已知量的NaOH溶液→选用酚酞指示剂用标准盐酸滴定
5.根据流程图内数据计算:滤渣C中氢氧化铝的质量分数为______________________。(用m、n的代数式表示)
6.按该流程的操作步骤,氢氧化铝质量分数的测定结果偏高的可能性是最大的,原因有_______________________________;____________________________________。
-
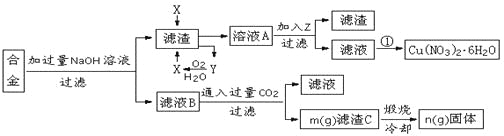
某兴趣小组用合金铝、铁、铜的废弃合金为原料制取硝酸铜晶体和氢氧化铝,并测定硝酸铜晶体的结晶水含量和氢氧化铝的纯度,设计的主要流程如下:
已知:
Fe2+沉淀的pH范围为7.0~9.0;Fe3+沉淀的pH范围为1.9~3.2;Cu2+沉淀的pH范围为4.7~6.7
回答下列问题:
(1)写出合金中加入NaOH溶液后所发生的离子反应方程式_______________________。试剂X的名称为______________。
(2)加入Z的作用是调节溶液的pH,pH范围应为_____;下列可作为试剂Z的是_______。
a.铜粉 b.氨水 c.氧化铜 d.硫酸铜
(3)实验操作①依次是_________、_________、过滤洗涤即可得硝酸铜晶体。
(4)测定硝酸铜晶体的结晶水含量,下列方案中肯定不可行的是______。(选填编号)
a.称量样品→加热→冷却→称量CuO
b.称量样品→加热→冷却→称量Cu(NO3)2
c.称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量
d.称量样品→加过量已知量的NaOH溶液→选用酚酞指示剂用标准盐酸滴定
(5)根据流程图内数据计算:滤渣C中氢氧化铝的质量分数为______________________。(用m、n的代数式表示)
(6)按该流程的操作步骤,氢氧化铝质量分数的测定结果偏高的可能性是最大的,原因有_______________________________;____________________________________。
-
某化学兴 趣小组的同学
趣小组的同学 在实验室中用含有铝、铁、铜的废弃合金为主要原料制取硫酸铝溶液、硝酸铜晶体和无水氯化铁,其实验流程如下图所示。
在实验室中用含有铝、铁、铜的废弃合金为主要原料制取硫酸铝溶液、硝酸铜晶体和无水氯化铁,其实验流程如下图所示。
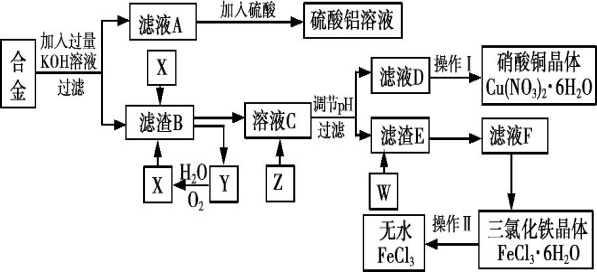
已知:Fe3+沉淀的pH范围为1.9~3.2;Cu2+沉淀的pH范围为4.7 ~6.7。
~6.7。
请回答下列问题:
(1)写出向合金中加入KOH溶液后所发生反应的离子方程式:__________________,若在该反应中转移0.6NA的电子,则获得标准状况下的气体体积为________L。
(2)下列物质中可作为试剂Z的是_______(填序号)。
A.铜粉 B.氨水 C.氧化铜
加入Z后,调节溶液的pH范围应为________________。
(3)实验操作Ⅰ的顺序依次为____________(填序号)。
A.蒸发浓缩 B.过滤 C.冷却结晶
(4)写出滤渣E与W反应的化学方程式______________________。
-
(12分)某粗氧化铜样品中含少量氧化亚铁及不溶于酸的杂质,某化学兴趣小组利用该样品制取胆矾晶体,测定胆矾晶体中结晶水的含量,并计算样品中氧化铜的含量,设计了如下方案进行实验。
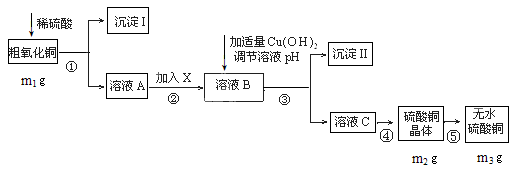
查阅资料知Fe3+、Cu2+、Fe2+在水溶液中形成氢氧化物沉淀的pH范围如下:
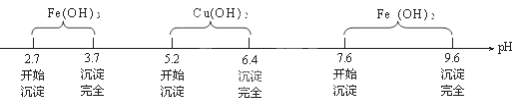
请回答下列问题:
(1)在整个实验过程中,下列仪器中不可能用到的是__________(填编号)。
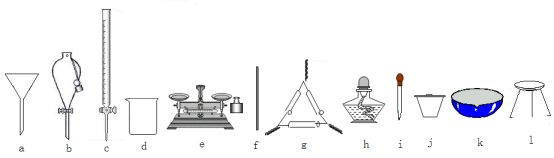
(2)物质X应选用_________(填字母)。
a.氢氧化钠 b.双氧水 c.铁粉 d.高锰酸钾
(3)为保证沉淀Ⅱ沉淀完全,操作③中溶液pH的调节范围为 。
(4)操作④的步骤有 、冷却结晶、 、自然干燥。
(5)在测定所得胆矾(CuSO4·xH2O)中结晶水x值的实验过程中:称量操作至少进行__ 次若测定结果x值偏大,可能的原因是_______________。
a.加热温度过高
b.胆矾晶体的颗粒较大
c.加热后放在空气中冷却
d.加热胆矾晶体时有晶体从坩埚中溅出
(6)该小组一位同学根据实验结果求出样品中CuO的质量分数为 ,另一位同学不同意,其原因是 。
,另一位同学不同意,其原因是 。
-
垃圾是放错地方的资源,工业废料也可以再利用。某化学兴趣小组在实验室中用废弃含有铝、铁、铜的合金制取硫酸铝溶液、硝酸铜晶体和铁红(Fe2O3)。其实验方案如下:
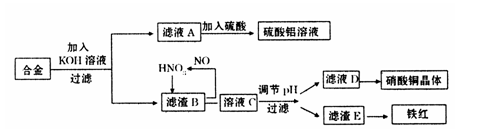
(1)请写出在合金中加入KOH溶液后所发生的离子反应方程式:
________ 。
(2)在滤液A中直接加入硫酸所获得的硫酸铝溶液中会含有杂质(K2SO4),请设计一个更合理的实验方案由滤液A制备纯净的硫酸铝溶液。仿照上图形式画出制备流程图:(提示:在箭头上下方标出所用试剂或实验操作)
(3)已知Fe(OH)3沉淀的pH是2~3.2。溶液C通过调节pH可以使Fe3+沉淀完全。下列物
质中,可用作调整溶液C的pH的试剂是(填序号)
A. 铜粉 B.氨水 C. 氧化铜 D.氢氧化铜
(4)利用滤液D制取硝酸铜晶体,必须进行的实验操作步骤:加热蒸发、冷却结晶、
________ (填操作名称)、自然干燥。
(5)在0.1L的混合酸溶液中,c(HNO3)=2mol·L-1,c(H2SO4)=3mol·L-1。将0.3mol的铜放入并充分反应后,产生的铜盐的化学式是________,被还原的n(HNO3)=________。
-
垃圾是放错地方的资源,工业废料也可以再利用。某化学兴趣小组在实验室中用废弃的含铝、铁、铜的合金制取硫酸铝溶液、硝酸铜晶体和铁红(Fe2O3)。实验方案如下:
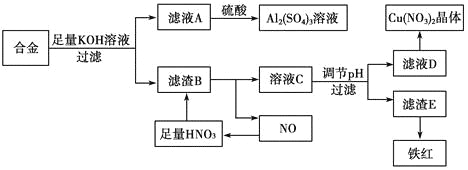
(1)写出滤液A中加入足量硫酸后所发生反应的离子方程式:__________________。
(2)已知Fe(OH)3沉淀的pH是3~4,溶液C通过调节pH可以使Fe3+沉淀完全。下列物质中可用作调整溶液C的pH的试剂是________(填序号)。
(3)常温,若溶液C中金属离子均为1 mol·L-1,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]=2.2×10-20。控制pH=4,溶液中c(Fe3+)=____________,此时________Cu(OH)2沉淀生成(填“有”或“无”)。
(4)将20 mL Al2(SO4)3溶液与等物质的量浓度的Ba(OH)2溶液80 mL混合,反应的离子方程式为_______________。
-
I.垃圾是放错地方的资源,工业废料也可以再利用,某化学兴趣小组在实验室中用废弃的含铝、铁、铜的合金制取硫酸铝溶液,硝酸铜晶体和铁红(Fe2O3)。实验方案如下:
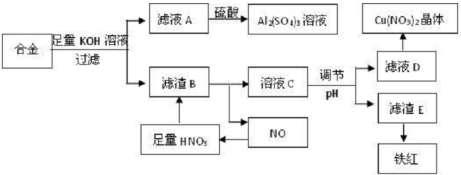
(1)已知Fe(OH)3沉淀的pH范围是3-4,溶液C通过调节pH可以使Fe3+沉淀完全,下列物质中可用作调整溶液C的pH的试剂是______________(填序号)
A.铜粉 B.氨水 C.氢氧化铜 D.碱式碳酸铜
(2)常温下,若溶液C中金属离子均为1mol/L,Ksp[Fe(OH)3]=1.0×10-39,Ksp[Cu(OH)2]=2.2×10-20,控制pH=4,溶液中c(Fe3+)=______________,此时______________(填“有” 或“无”)Cu(OH)2沉淀生成。
(3)将20mLAl2(SO4)3溶液与等物质的量浓度的Ba(OH)2溶液70mL混合,反应的离子方程式为______________。
Ⅱ.工业上以碳酸镁(含少量FeCO3)为原料制取硫酸镁晶体,并测定晶体中,MgSO4的含量,具体过程如下:
将原料完全溶于一定量的稀硫酸中,加足量的H2O2后用氨水调节溶液的pH值,静置后过滤,除去滤渣将滤液结晶得硫酸镁晶体。
(1)加入H2O2的目的是______________(用离子方程式解释)
(2)常采用下列方法测定硫酸镁晶体中MgSO4 的含量:
已知:①在pH为9~10时,Mg2+、Zn2+均能与EDTA(H2Y2+)原形成配合物。
②在pH为5~6时,Zn2+除了与EDTA反应,还能将Mg2+与EDTA形成的配合物中的Mg2+“置换”出来:Zn2++MgH2Y=ZnH2Y+Mg2+
步骤1:准确称取得到的硫酸镁晶体1.5g加入过量的EDTA配成100mLpH 在9~10之间溶液A
步骤2:准确移取25.00mL:溶液A于锥形瓶中,用0.1000mol/LZn2+标准溶液滴定,滴定到终点时,消耗Zn2+标准溶液的体积为20.00mL
步骤3:另外准确移取25.00mL溶液A于另一只锥形瓶中调节pH在5~6,用0.1000mol/LZn2+标准溶液滴定,滴定至终点时,消耗Zn2+标准溶液的体积为30.00mL。
计算该晶体中MgSO4的质量分数为______________。
-
硫酸铜是一种应用极其广泛的化工原料.某课外兴趣小组将适量浓硝酸分多次加到铜粉与稀硫酸的混合物中,加热使之反应完全(装置如图I、图Ⅱ所示),通过蒸发、结晶得到硫酸铜晶体,并同时测定硫酸铜晶体中结晶水的含量.
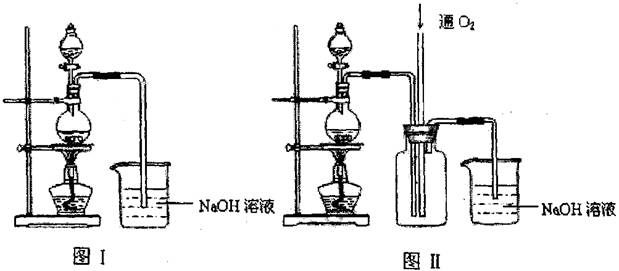
(1)怎样检查图I装置的气密性 ________。
(2)图I中分液漏斗内装的液体是________。
(3)图Ⅱ是图Ⅰ的改进装置,与图I相比,图Ⅱ装置的明显优点是 ,
________,________,(可不答满).
(4)课外兴趣小组同学在测定胆矾(CuSO4·χH2O)晶体中结晶水的含量时.测得有关数据如下表:
| 加热前质量 | 加热后质量 |
| m1(容器) | m2(容器+晶体) | m3(容器+无水CuSO4) |
| 5.4g | 7.9g | 6.8g |
①为完成测定,图Ⅲ中还缺少的仪器名称是________。
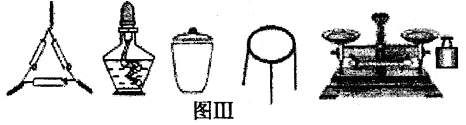
②判断样品已恒重的方法是________。
③测定所得胆矾(CuSO4·χH2O)中结晶水含量的实验中,称量操作至少进行________次。
④课外兴趣小组的测定结果x值(与CuSO4·5H2O相比)________(填“偏高”、“偏低”、“不变”),可能的原因是________。(填字母序号)
a.加热温度过高
b.胆矾晶体的颗粒较大
c.加热后放在空气中冷却
d.胆矾晶体部分风化
| ________学校 姓名________ 考号________ 班级________ |
| ……………………………………………密………………………………………封……………………………………………….线…………………………………………………. |
-
某研究小组在实验室中将某工厂废弃的一块合金,经过一系列的反应,制得氧化铝固体、硝酸铜晶体和铁红。其实验方案如下图。
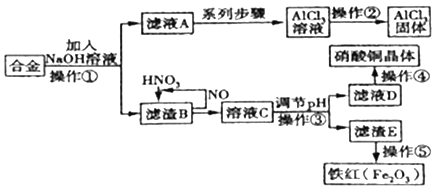
(1)该小组所用的合金中含有的金属为铁、______、______(填名称)。
(2) 操作①、③使用的主要玻璃仪器是___________,操作②的方法:________。操作④实验操作步骤包括:______、_______(填操作名称)、过滤、洗涤、干燥。
(3)写出滤渣B中较活泼金属与足量稀硝酸发生反应的离子方程式:_______。
(4)若该小组通过上述实验流程制得铁红16g,假设实验过程中无质量损失,则合金中铁的质量为________g。
(5)上述实验流程中符合“绿色化学“理念的做法是___________(答出一点即可)。
-
某研究小组在实验室中将某工厂废弃的一块合金,经过一系列的反应,制得氧化铝固体、硝酸铜晶体和铁红。其实验方案如下图。
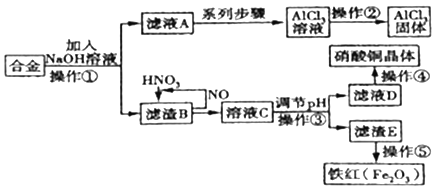
(1)该小组所用的合金中含有的金属为铁、______、______(填名称)。
(2) 操作①、③使用的主要玻璃仪器是___________,操作②的方法:________。操作④实验操作步骤包括:______、_______(填操作名称)、过滤、洗涤、干燥。
(3)写出滤渣B中较活泼金属与足量稀硝酸发生反应的离子方程式:_______。
(4)若该小组通过上述实验流程制得铁红16g,假设实验过程中无质量损失,则合金中铁的质量为________g。
(5)上述实验流程中符合“绿色化学“理念的做法是___________(答出一点即可)。













