-
已知A、B、R、D都是周期表中前四周期的元素,它们的原子系数依次增大。其中A元素基态原子第一电离能比B元素基态原子的第一电离能大,B的基态原子的L层、R基态原子的M层均有2个单电子,D是第Ⅷ族中原子序数最小的元素。
(1)写出基态D原子的电子排布式__________。
(2)已知高纯度R的单质在现代信息技术与新能源开发中具有极为重要的地位。工业上生产高纯度R的单质过程如下:

写出过程③的反应方程式___________,已知RHCl3的沸点是31.5oC,则该物质的晶体类型是__________,中心原子的轨道杂化类型为__________,该物质的空间构型是______。
(3)A的第一电离能比B的第一电离能大的原因是_________,A、B两元素分别与R形成的共价键中,极性较强的是________。A、B两元素间能形成多种二元化合物,其中与A3-互为等电子体的物质的化学式为_______。
(4)已知D单质的晶胞如图所示,则晶体中D原子的配位数为______,一个D的晶胞质量为____,已知D原子半径为r pm,则该晶胞的空间利用率为_____________ (写出计算过程)。

-
已知 、
、 、
、 、
、 、
、 都是元素周期表中前四周期的元素,它们的核电荷数依次增大。其中
都是元素周期表中前四周期的元素,它们的核电荷数依次增大。其中 与
与 、
、 与
与 在周期表中相邻,
在周期表中相邻, 原子核外有两个未成对电子,
原子核外有两个未成对电子, 的第一电离能比同周期相邻两种元素的都大,
的第一电离能比同周期相邻两种元素的都大, 原子在同周期元素原子中半径最大(稀有气体原子除外);
原子在同周期元素原子中半径最大(稀有气体原子除外); 与
与 位于不同周期,
位于不同周期, 原子核外最外层电子数与
原子核外最外层电子数与 相同,其余各电子层均充满电子。请根据以上信息,回答下列问题。
相同,其余各电子层均充满电子。请根据以上信息,回答下列问题。
(1) 、
、 、
、 、
、 四种元素的电负性由大到小的排列顺序为_________。
四种元素的电负性由大到小的排列顺序为_________。
(2) 的氢化物的结构式为_________,其分子的空间构型为________。
的氢化物的结构式为_________,其分子的空间构型为________。
(3) 的某种化合物的结构如图所示,已知微粒间的相互作用包括化学键和分子间作用力,则此化合物中各种粒子间的相互作用力有___________。
的某种化合物的结构如图所示,已知微粒间的相互作用包括化学键和分子间作用力,则此化合物中各种粒子间的相互作用力有___________。

(4) 与
与 的气态氢化物相比,_________(填化学式,下同)的沸点更高;
的气态氢化物相比,_________(填化学式,下同)的沸点更高; 与
与 的气态氢化物相比,________的沸点更高。
的气态氢化物相比,________的沸点更高。
(5) 的稳定氧化物中,中心原子采取________杂化,该氧化物分子的空间构型为______。
的稳定氧化物中,中心原子采取________杂化,该氧化物分子的空间构型为______。
-
已知A、B、R、D都是周期表中前四周期的元素,它们的原子序数依次增大。其中A元素基态原子第一电离能比B元素基态原子的第一电离能大,B的基态原子的L层、R基态原子的M层均有2个单电子,D是第Ⅷ族中原子序数最小的元素。
(1)写出基态D原子的电子排布式 。
(2)已知高纯度R的单质在现代信息技术与新能源开发中具有极为重要的地位。工业上生产高纯度R的单质过程如下:

写出③的反应方程式 ,已知RHCl3的沸点是31.5℃, 则该物质的晶体类型是 ,组成微粒的中心原子的轨道杂化类型为 ,空间构型是 。
(3)A的第一电离能比B的第一电离能大的原因是 ,A、B两元素分别与R形成的共价键中,极性较强的是 。A、B两元素间能形成多种二元化合物,其中与A3-互为等电子体的物质的化学式为 。
(4)已知D单质的晶胞如图所示,则晶体中D原子的配位数为 ,一个D的晶胞质量为 。

-
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A与B同周期、A与D同族,A原子核外有两个未成对电子,B元素的第一电离能比同周期相邻两种元素都大,C原子在同周期原子中半径最大(稀有气体除外);E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满。请根据以上信息回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)E原子核外电子排布式是 。
(2)B的最高价含氧酸根的空间构型为 。
(3)A、B、D三种元素电负性由大到小排列顺序为 。
(4)D单质比化合物DA的熔点 (填“高”或“低”),理由是 。
(5)已知A、C和地壳中含量最多的元素按1∶1∶2的原子个数比可形成某离子化合物,该化合物能使酸性高锰酸钾溶液褪色,写出发生反应的离子方程式 。
-
(13分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A与B同周期、A与D同族,A原子核外有两个未成对电子,B元素的第一电离能比同周期相邻两种元素都大,C原子在同周期原子中半径最大(稀有气体 除外);E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满。请根据以上信息回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)E原子核外电子排布式是 。
(2)B的最高价含氧酸根的空间构型为 ;
(3)A、B、D三种元素电负性由大到小排列顺序为 。
(4)D单质比化合物DA的熔点 (填“高”或“低”),理由是 。
(5)已知A、C和地壳中含量最多的元素按1∶1∶2的原子个数比可形成某离子化合物,该化合物能使酸性高锰酸钾溶液褪色,写出发生反应的离子方程式 。
-
X、Y、Z、W、R、I、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,I的原子序数是W的两倍,Q的最外层只有一个电子,其他电子层电子均处于饱和状态.请回答下列问题:
(1)Q+核外电子排布式为___________,Y的电子排布图为_________________________
(2)化合物ZX3中Z原子的杂化方式为___________,ZW2- 离子的立体构型是___________;
(3)①Y、R的最高价氧化物的沸点较高的是___________(填化学式),原因是___________;
②W与I的简单氢化物中W的熔沸点更高,原因是______________________
(4)向Q元素的硫酸盐溶液中通入足量ZX3,充分反应后溶液呈深蓝色,该反应的离子方程式为__________________________________________________;
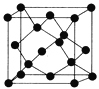
(5)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为___________,Y原子的配位数为___________,若晶胞的边长为a pm,晶体的密度为ρ g/cm3,则阿伏加德罗常数的数值为___________(用含a和ρ的代数式表示)。
-
A、B、X、Y、Z、R、Q为前四周期元素,且原子序数依次增大。A是所有元素中原子半径最小的;B的核外电子排布式为ls22s22p2;X原子单电子数在同周期元素中最多;Y与X同周期,第一电离能比X的低;Z的M层电子数是K层电子数的2倍;R与Y同主族;Q的最外层只有一个电子,其它电子层电子均处于饱和状态。
回答下列问题:
(1)Q+的核外电子排布式为______,Z的价电子轨道表达式(价电子排布图)为_______。
(2)化合物XA3中X原子的杂化方式为______;A3Y+的立体构型为______。
(3)① B、Z的最高价氧化物的沸点较高的是______(填化学式),原因是______。
② Y与R的简单氢化物中Y的熔沸点更高,原因是______。
(4)向Q元素的硫酸盐溶液中通入足量XA3,充分反应后溶液呈深蓝色,该反应的离子方程式为______。
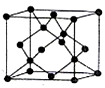
(5)B有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞中B原子数为______,B原子的配位数为______,若晶胞的边长为apm,晶体的密度为ρg/cm3,则阿伏加德罗常数为______(用含a和p的式子表示)。
-
X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态.请回答下列问题:
(1)Q+核外电子排布式为___________;
(2)化合物X2W2中W的杂化方式为___________,ZW2-离子的立体构型是___________;
(3)Y、R的最高价氧化物的沸点较高的是___________(填化学式),原因是___________;
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为___________;
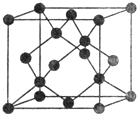
(5)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为___________,Y原子的配位数为___________,若晶胞的边长为a pm,晶体的密度为ρ g/cm3,则阿伏加德罗常数的数值为___________(用含a和ρ的代数式表示)。
-
X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态.请回答下列问题:
(1)Q+核外电子排布式为___________;
(2)化合物X2W2中W的杂化方式为___________,ZW2-离子的立体构型是___________;
(3)Y、R的最高价氧化物的沸点较高的是___________(填化学式),原因是___________;
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为___________;
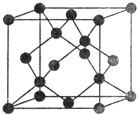
(5)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为___________,Y原子的配位数为___________,若晶胞的边长为a pm,晶体的密度为ρ g/cm3,则阿伏加德罗常数的数值为___________(用含a和ρ的代数式表示)。
-
X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大。X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态。请回答下列问题:
(1)Q+核外电子排布式为_____________________________。
(2)化合物X2W2中W的杂化方式为________________,ZW2-的立体构型是___________。
(3)Y、R的最高价氧化物的沸点较高的是________(填化学式),原因是__________。
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为______________________________________________________________。








