-
C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外电子排布式 。
从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为 。
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为 ,微粒间存在的作用力是 。
(3)氧化物MO的电子总数与SiC的相等,则M为 (填元素符号),MO是优良的耐高温材料,其晶体结构与NaCl晶体相似,MO的熔点比CaO的高,其原因是 。
高二化学填空题中等难度题查看答案及解析
-
C和Si元素在化学中占有极其重要的地位.
(1)写出Si的基态原子核外电子排布式______.从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为______.
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为______,微粒间存在的作用力是______.
(3)氧化物MO的电子总数与SiC的相等,则M为______(填元素符号),MO是优良的耐高温材料,其晶体结构与NaCl晶体相似,MO的熔点比CaO的高,其原因是______.
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同.CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π健.从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π健______.
(5)有A、B、C三种物质,每个分子中都各有14个电子,其中A的分子属于非极性分子,且只有非极性键;B的分子也属于非极性分子,但既有非极性键,又有极性键;C的分子属于极性分子.则可推出:A的电子式是______,B的结构式是______.
(6)已知Si-Si键能为176kJ/mol,Si-O键能为460kJ/mol,O=O键能为497.3kJ/mol.则可计算出1mol硅与足量氧气反应时将放出______kJ的热量.高二化学解答题中等难度题查看答案及解析
-
碳、氧、硅、锗、氟、氯、溴、镍元素在化学中占有极其重要的地位。
(1)第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是________。
(2)从电负性角度分析,碳、氧和硅元素的非金属性由强至弱的顺序为____________________。
(3)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为__________________。
(4)基态锗(Ge)原子的电子排布式是____________,Ge的最高价氯化物分子式是________。该元素可能的性质或应用有________(填字母)。
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.锗的第一电离能高于碳而电负性低于碳
(5)溴与氯能以________键结合形成BrCl,BrCl分子中,________显正电性。BrCl与水发生反应的化学方程式为______________________________________________。
高二化学填空题中等难度题查看答案及解析
-
(6分)现代科技的高度快速发展离不开C和Si元素。
(1)写出Si的基态原子核外电子排布式__________________。
(2)从电负性角度分析,C、Si、O元素的非金属活泼性由强至弱的顺序为______。
(3)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为_____,微粒间存在的作用力是_______。
(4)C、Si为同一主族的元素,CO2 、SiO2的化学式相似,但结构和性质有很大的不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成上述π键,而Si、O原子间不能形成上述π键:_________________________
高二化学填空题困难题查看答案及解析
-
地球上的元素大多数是金属,Na、Mg、Al是常见的主族金属元素,Fe和Cu是常见的过渡金属元素。它们在化学中占有极其重要的地位。
(1)①Na、Mg、Al三种元素第一电离能由大到小的顺序为___________
②金属钠原子的堆积方式是体心立方,其配位数为___________
(2)选修三课本第42页实验2-2:向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
①硫酸铜溶液中呈___________色的物质是水合铜离子,请写出它的结构简式,并标明其中配位键___________
②请写出难溶物溶解得到深蓝色的透明溶液的离子方程式___________
③结构测定的实验证明,无论在氨水溶液中还是在晶体中,深蓝色都是由于存在某种离子,1mol该离子含有___________molσ键。
(3)写出少量Na2O2与氯化铁溶液反应的离子反应方程式:___________(要求:仅写1个总的离子方程式)
高二化学综合题中等难度题查看答案及解析
-
太阳能的开发利用在新能源研究中占据重要地位.单晶硅太阳能电池片在加工时,一般掺杂微置的锎.硼.镓.硒等。回答下列问題:
(1)硒的基态原子的电子排布式为________。已知铜和某元素M的电负性分别是1.9和3.0,则铜与M形成的化合物属于________填“离子”,“共价”)化合物。已知高温下Cu2O比CuO更稳定,试从铜原子核外电子结构变化角度解释________________。
(2)铜与类卤素(SCN)2反应生成Cu(SCN)2,类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H﹣S﹣C≡N )的沸点低于异硫氰酸(H﹣N=C=S)的沸点.其原因是________。
(3)硼元素具有缺电子性,其化合物可与具有孤电子对的分子或离子形成配合物,如BF3能与NH3反应生成BF3·NH3.在BF3·NH3中B原子的杂化方式为________,B与N之间形成配位键,氮原子提供________。写出一种与NH3互为等电子体的离子的化学式______________。
(4)含硼化合物是一种常见的还原剂,结构如图所示。请在图中画出配位键________。

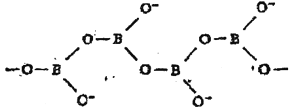
(5)多硼酸根离子可以通过三角形共用原子连接成链状,片状或者三维网状多硼酸根离子。下图是无限长单链结构的多硼酸根离子,其中与原子数之比为 ,化学式为________________
高二化学综合题困难题查看答案及解析
-
1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值。注意阅读分析材料,据此完成下列要求。
元素
H
Li
Be
B
C
N
O
F
电负性
2.1
1.0
1.5
2.0
2.5
3.0
3.5
4.0
元素
Na
Mg
Al
Si
P
S
Cl
K
电负性
0.9
1.2
1.5
1.7
2.1
2.3
3.0
0.8
(1)预测周期表中电负性最大的元素应为________(填元素符号);估计钙元素的电负性的取值范围:________<X<________。
(2)简述元素电负性X的大小与元素金属性、非金属性之间的关系________
________。
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的键一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为________;上表中最易形成离子键的两种元素的电负性之差为________。
高二化学填空题困难题查看答案及解析
-
1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值。注意阅读分析材料,据此完成下列要求。
元素
H
Li
Be
B
C
N
O
F
电负性
2.1
1.0
1.5
2.0
2.5
3.0
3.5
4.0
元素
Na
Mg
Al
Si
P
S
Cl
K
电负性
0.9
1.2
1.5
1.7
2.1
2.3
3.0
0.8
(1)预测周期表中电负性最大的元素应为 (填元素符号);估计钙元素的电负性的取值范围: <X< 。
(2)简述元素电负性X的大小与元素金属性、非金属性之间的关系
。
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的键一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为 ;上表中最易形成离子键的两种元素的电负性之差为 。
高二化学填空题困难题查看答案及解析
-
1932年美国化学家鲍林首先提出了电负性的概念.电负性(用X表示)也是元素的一种重要性质,若 x 越大,其原子吸引电子的能力越强,在所形成的分子中成为带负电荷的一方.下面是某些短周期元素的 x 值:
元素符号
Li
Be
B
C
O
F
Na
Al
Si
P
S
Cl
x 值
0.98
1.57
2.04
2.55
3.44
3.98
0.93
1.61
1.90
2.19
2.58
3.16
⑴通过分析 x 值变化规律,确定N、Mg的 x 值范围:
________<x (N)<________, ________<x (Mg)<________.
⑵某有机化合物结构中含S-N键,其共用电子对偏向________(写原子名称).
⑶经验规律告诉我们:当成键的两原子相应元素的 x 差值△x>1.7时,一般为离子键,当△ x<1.7时,一般为共价键.试推断AlBr3中化学键类型是________.
⑷预测周期表中,x 值最小的元素位于________周期________族.(放射性元素除外)
高二化学填空题困难题查看答案及解析
-
(8分)1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,若 x 越大,其原子吸引电子的能力越强,在所形成的分子中成为带负电荷的一方.下面是某些短周期元素的 x 值:
元素符号
Li
Be
B
C
O
F
Na
Al
Si
P
S
Cl
x 值
0.98
1.57
2.04
2.55
3.44
3.98
0.93
1.61
1.90
2.19
2.58
3.16
(1)通过分析 x 值变化规律,确定N、Mg的 x 值范围:
<x (N)< , <x (Mg)< 。
(2)某有机化合物结构中含S-N键,其共用电子对偏向 (写原子名称)。
(3)经验规律告诉我们:当成键的两原子相应元素的 x 差值△x>1.7时,一般为离子键,当△ x<1.7时,一般为共价键,试推断AlBr3中化学键类型是 。
(4)预测周期表中,x 值最小的元素位于 周期 族。(放射性元素除外)
高二化学填空题中等难度题查看答案及解析