-
已知M、Q、X、Y、Z是前四周期中元素(不包含稀有气体元素),有关性质和相关信息如下表:
元素
相关信息
M
最高价氧化物对应的水化物能按1:1电离出电子数相等的阴、阳离子
Q
所在主族序数与所在周期序数之差为4,非金属性在同周期元素中最强
X
其单质为淡黄色晶体
Y
某种核素原子的质量数为56,中子数为30
Z
X元素的单质在Z元素的单质中燃烧,发出明亮的蓝紫色火焰
(1)下图是不完整的元素周期表,补全元素周期表的轮廓,并将Y的元素符号填在元素周期表中相应的位置上。
(2)M与Z形成的含有共价键的化合物的电子式为 。
(3)M、Q、Z简单离子的半径由大到小的顺序为 (用离子符号表示)。
(4)用一个化学方程式表示证明非金属性Q>X: 。
(5)5.6L标准状况下的X的简单氢化物在足量的Z单质中完全燃烧生成液态水时,放出的热量为356.8kJ。该反应的热化学方程式为 。
(6)在碱性条件下,Q的单质可与YZ2-反应制备一种可用于净水的盐YZ42-,该反应的离子方程式为。
高三化学填空题简单题查看答案及解析
-
X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
元素
相 关 信 息
X
X最高价氧化物的水化物与气态氢化物可以形成一种盐
Y
单质是良好的半导体材料,广泛应用于光电信息领域
Z
Z的一种核素质量数为27,中子数为14
W
最高价氧化物对应的水化物是一种不溶于水的蓝色固体
(1)Z位于元素周期表第__________周期第_________族;Z的原子半径比Y的________, X的第一电离能比Y的________(填“大”或“小”)。
(2)W基态原子的核外电子排布式为____ ____,XH3分子的沸点较高,请解释其原因____ 。
(3)X的氢化物(X2H4)的制备方法之一是将NaClO溶液和XH3反应制得,试写出该反应的离子方程式 。
(4)已知下列数据:4W(s)+ O2(g) = 2W2O(s) △H = -337.2 KJ/mol 2W(s)+ O2(g) = 2WO(s) △H = -314.6 KJ/mol;由W2O和O2反应生成WO的热化学方程式是 。
高三化学填空题困难题查看答案及解析
-
X、Y、Z、U、V是元素周期表前四周期中的五种常见元素,其相关信息如下表:
元素
相关信息
X
地壳中含量最多的金属,其氧化物可用作耐火材料
Y
单质在常温常压下为黄绿色气体
Z
常温常压下,单质是淡黄色固体,常在火山口附近沉积
U
常温下单质遇浓硫酸钝化,其一种核素的质量数为56,中子数为30
V
属短周期元素,原子的最外层电子数是内层电子数的2/5
请回答下列问题:
(1)元素X位于周期表中第________周期第________族,其离子结构示意图为________。
(2)上述元素中最高价氧化物对应的水化物酸性最强的是________(写化学式),非金属气态氢化物还原性最强的是________(写化学式)。
(3)在碱性条件下,Y的单质可与UO2-反应制备一种可用于净水的盐UO42-,该反应的离子方程式是________。
(4)我国首创的海洋电池被大规模用于海洋灯塔。该电池是以X板为负极,铂网为正极,海水为电解质溶液,电池总反应为:4X+3O2+6H2O=4X(OH)3。该电池正极反应为________。
(5)已知25℃时,Ksp[U(OH)3]=2.63×10-39,则该温度下反应U(OH)3+3H+
U3++3H2O的平衡常数K=________。
高三化学推断题极难题查看答案及解析
-
X、Y、Z、W是元素周期表前四周期中的四种常见元素,相关信息如表:
(1)X元素位于周期表中第______周期,第______族,其单质中为原子晶体的名称是______.元素 相关信息 X X的氢化物分子中含10个电子,呈正四面体结构 Y Y与X同周期,其最高价氧化物对应的水化物是一种强氧化性酸 Z 第三周期元素中,Z电负性最小 W W的基态原子核外M能层上填满了电子,N能层只有1个电子
(2)Z的基态原子核外电子排布式为______;工业上电解其氯化物饱和溶液时,阳极上发生的电极反应式为______.
(3)XO、YO是现代城市的主要污染物,在催化剂作用下可以转化为两种无毒物质.
已知:X(s)+O2(g)═XO2(g)△H=-akJ/mol,
2X(s)+O2(g)═2XO(g)△H=-b kJ/mol,
Y2(g)+O2(g)═2YO(g)△H=+ckJ/mol.
则上述转化的热化学方程式为______.
(4)0.3molW的低价氧化物能与含______molY最高价氧化物对应的水化物溶液恰好完全反应(设还原产物只有YO).高三化学解答题中等难度题查看答案及解析
-
X、Y、Z、W、R是元素周期表前四周期中的常见元素,其相关信息如下表:
元素
相关信息
X
组成蛋白质的基础元素,其最高正化合价与最低负化合价的代数和为2
Y
地壳中含量最高的元素
Z
存在质量数为23,中子数为11的核素
W
生活中大量使用其合金制品,工业上可用电解熔融氧化物的方法制备其单质
R
有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色
(1)W在元素周期表中的位置为 ;X、Y、Z、W四种元素的原子半径从大到小的顺序是 (用元素符号表示)。
(2)X与氢两元素按原子数目比1∶3和2∶4构成分子A和B,A的结构式为 ;B的电子式为 。化合物ZY中存在的化学键类型为 。
(3)砷(As)是人体必需的微量元素,与X同一主族,As原子比X原子多两个电子层,则砷的原子序数为 ,其最高价氧化物对应的水化物的化学式为 。该族二、三、四周期元素的气态氢化物的稳定性从大到小的顺序是 (用化学式表示)。
(4)用RCl3溶液腐蚀铜线路板的离子方程式为 。检验溶液中R3+常用的试剂是 ,可以观察到的现象是 。
(5)Z
W合金(Z17W12)是一种潜在的贮氢材料,由Z、W单质在一定条件下熔炼而成。该合金在一定条件下完全吸氢的反应方程式为:Z17W12+17H2
17ZH2+12W,得到的混合物Q(17ZH2+12W)在6.0 mol·L-1HCl溶液中能完全释放出H2。1 mol Z17W12完全吸氢后得到的混合物Q与上述盐酸完全反应,释放出H2的物质的量为 。
高三化学填空题中等难度题查看答案及解析
-
X、Y、Z、W、R是元素周期表前四周期中的常见元素,其相关信息如下表:
元素
相关信息
X
组成蛋白质的基础元素,其最高正化合价与最低负化合价的代数和为2
Y
地壳中含量最高的元素
Z
存在质量数为23,中子数为11的核素
W
生活中大量使用其合金制品,工业上可用电解熔融氧化物的方法制备其单质
R
有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色
(1)W在元素周期表中的位置为 ;X、Y、Z、W四种元素的原子半径从大到小的顺序是 (用元素符号表示)。
(2)X与氢两元素按原子数目比1∶3和2∶4构成分子A和B,A的结构式为 ;B的电子式为 。化合物ZY中存在的化学键类型为 。
(3)砷(As)是人体必需的微量元素,与X同一主族,As原子比X原子多两个电子层,则砷的原子序数为 ,其最高价氧化物对应的水化物的化学式为 。该族二、三、四周期元素的气态氢化物的稳定性从大到小的顺序是 (用化学式表示)。
(4)用RCl3溶液腐蚀铜线路板的离子方程式为 。检验溶液中R3+常用的试剂是 ,可以观察到的现象是 。
(5)Z
W合金(Z17W12)是一种潜在的贮氢材料,由Z、W单质在一定条件下熔炼而成。该合金在一定条件下完全吸氢的反应方程式为:Z17W12+17H2
17ZH2+12W,得到的混合物Q(17ZH2+12W)在6.0 mol·L-1 HCl溶液中能完全释放出H2。1 mol Z17W12完全吸氢后得到的混合物Q与上述盐酸完全反应,释放出H2的物质的量为 。
高三化学填空题困难题查看答案及解析
-
[化学—选修3物质结构与性质] T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
元素
相关信息
T
T元素可形成自然界硬度最大的单质
W
W与T同周期,核外有一个未成对电子
X
X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol
Y
常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质
Z
Z的一种同位素的质量数为63,中子数为34
(1)TY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在 个σ 键。W的最简单氢化物容易液化,理由是 。
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 。
(3)基态Y原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。Y、氧、W元素的第一电离能由大到小顺序为 (用元素符号作答)。
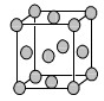
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00 g/cm3,则晶胞边长为 ;ZYO4常作电镀液,其中YO42-的空间构型是 ,其中Y原子的杂化轨道类型是 。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
A.O2是 氧化剂
B.HO2 是氧化产物
C. HO2在碱中能稳定存在
D.1 mol Z参加反应有1 mol电子发生转移
高三化学填空题极难题查看答案及解析
-
[化学—选修3物质结构与性质] T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
元素
相关信息
T
T元素可形成自然界硬度最大的单质
W
W与T同周期,核外有一个未成对电子
X
X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol
Y
常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质
Z
Z的一种同位素的质量数为63,中子数为34
(1)TY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在 个σ 键。W的最简单氢化物容易液化,理由是 。
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 。
(3)基态Y原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。Y、氧、W元素的第一电离能由大到小顺序为 (用元素符号作答)。
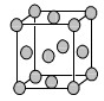
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00 g/cm3,则晶胞边长为 ;ZYO4常作电镀液,其中YO42-的空间构型是 ,其中Y原子的杂化轨道类型是 。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
A.O2是 氧化剂
B.HO2 是氧化产物
C. HO2在碱中能稳定存在
D.1 mol Z参加反应有1 mol电子发生转移
高三化学填空题极难题查看答案及解析
-
[化学—选修3物质结构与性质] T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
元素
相关信息
T
T元素可形成自然界硬度最大的单质
W
W与T同周期,核外有一个未成对电子
X
X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol
Y
常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质
Z
Z的一种同位素的质量数为63,中子数为34
(1)TY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在 个σ 键。W的最简单氢化物容易液化,理由是 。
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 。
(3)基态Y原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。Y、氧、W元素的第一电离能由大到小顺序为 (用元素符号作答)。
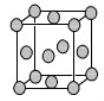
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00 g/cm3,则晶胞边长为 ;ZYO4常作电镀液,其中YO42-的空间构型是 ,其中Y原子的杂化轨道类型是 。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
A.O2是 氧化剂
B.HO2 是氧化产物
C. HO2在碱中能稳定存在
D.1 mol Z参加反应有1 mol电子发生转移
高三化学填空题极难题查看答案及解析
-
【化学——选修3:物质结构与性质】T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
元索
相关信息
T
T元素可形成自然界硬度最大的单质
W
W与T同周期,核外有一个未成对电子
X
X原子的第一离能至第四电离能分别I1="578" kJ/mol; I2=" l817" kJ/mol;I3="2745" kJ/mol;I4=11575kJ/mol
Y
常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质
Z
Z的一种同位素的质量数为63,中子数为34
(1) TY2是一种常用的溶剂,是__________(填“极性分子”或“非极性分子”),分子中存在________个σ键。
(2)W的最简单氢化物容易液化,理由是__________,.放热419 kJ,该反应的热化学方程式为 __________。
(3)基态Y原子中,电子占据的最高能层符号为__________,该能层具有的原子轨道数为_____________、电子数为_________。Y、氧、W元素的第一电离能由大到小的顺序为_________(用元素符号作答)。
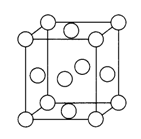
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00 g/cm3,则晶胞边长为___________cm;ZYO4常作电镀液,其中ZYO42-的空间构型是__________,其中Y原子的杂化轨道类型是___________。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z +HCl+O2=ZC1+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
A.O2是氧化剂
B.HO2是氧化产物
C.HO2在碱中能稳定存在
D.1 mol Z参加反应有1 mol电子发生转移
高三化学填空题简单题查看答案及解析