-
有一环保汽车,是以氢气作燃料的,请按题目要求作答:
(1)氢气在发动机内燃烧过程中,生成物只有水蒸气,不会使空气中的______含量偏高,因而能减缓温室效应现象的发生.
(2)如果2g氢气燃烧后生成水蒸气并放出241.8kJ的热量,写出氢气燃烧的热化学方程式:______
(3)已知:H2O(1)=H2O(g);△H=+44.0kJ/mol,则燃0.8g的氢气生成液态水放出的能量为______KJ.高三化学解答题中等难度题查看答案及解析
-
有一环保汽车,是以氢气作燃料的,请按题目要求作答:
(1)氢气在发动机内燃烧过程中,生成物只有水蒸气,不会使空气中的______含量偏高,因而能减缓温室效应现的发生.
(2)如果每mol氢气燃烧后生成水蒸气并放出241.8kJ的热量,写出氢气燃烧的热化学方程式______.高三化学解答题中等难度题查看答案及解析
-
(8分)有一环保汽车,是以氢气作燃料的,请按题目要求作答:
(1)氢气在发动机内燃烧过程中,生成物只有水蒸气,不会使空气中的________含量偏高,因而能减缓温室效应现的发生.
(2)如果每mol氢气燃烧后生成水蒸气并放出241.8kJ的热量,写出氢气燃烧的热化学方程式.
高三化学填空题简单题查看答案及解析
-
(本小题满分15分)
参考下列图表和有关要求回答问题:
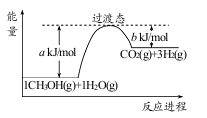
(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种原理是CH3OH(g)和H2O(g)反应生成CO2和H2。右图是该过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,正反应活化能 a的变化是_____________(填“增大”、“减小”、“不变”),反应热△H的变化是_____________(填“增大”、“减小”、“不变”)。请写反应进程出CH3OH(g)和H2O(g)反应的热化学方程式_____________。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的另一种反应原理是:CH3OH(g)+1/2O2(g)
CO2(g)+2H2(g) △H=c kJ/mol又知H2O(g)
H2O(l) △H=d kJ/mol。则甲醇燃烧生成液态水的热化学方程式为_____________。
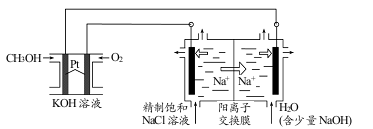
(3)以CH3OH燃料电池为电源电解法制取ClO2。二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
①CH3OH燃料电池放电过程中,通入 O2的电极附近溶液的pH_____________,负极反应式为_____________。
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取 ClO2。阳极产生 ClO2的反应式为_____________。
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多 6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为_____________mol。
高三化学填空题困难题查看答案及解析
-
参考下列图表和有关要求回答问题:
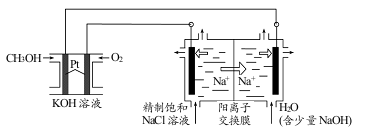
(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种原理是CH3OH(g)和H2O(g)反应生成CO2和H2。右图是该过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,正反应活化能 a的变化是_____ (填“增大”、“减小”、“不变”),反应热△H的变化是_____(填“增大”、“减小”、“不变”)。请写反应进程出CH3OH(g)和H2O(g)反应的热化学方程式_____。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的另一种反应原理是:
CH3OH(g)+1/2O2(g)
CO2(g)+2H2(g) △H=c kJ/mol
又知H2O(g)
H2O(l) △H=d kJ/mol。
则甲醇燃烧生成液态水的热化学方程式为_____。
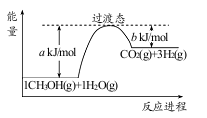
(3)以CH3OH燃料电池为电源电解法制取ClO2。二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
①CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH=_____,负极反应式为_____。
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取 ClO2。阳极产生 ClO2的反应式为_____。
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多 6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为_____mol。
高三化学填空题困难题查看答案及解析
-
(1)发射卫星时可用肼
为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气.已知:
①
,
②
,
.
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:______.
(2)氢气的燃烧热为
。写出表示氢气燃烧热的热化学方程式______。
(3)等质量的下列物质分别完全燃烧,放出热量较多的是反应过程________
填选项字母
。
A.固体硫
硫蒸气
(4)已知:通常条件下,强酸、强碱稀溶液中和生成
放出的热量为中和热。稀溶液中
和足量NaOH恰好反应时放出QkJ热量,则其中和热为________
。
(5)已知
和
反应放热,且断开
键、
键、
键吸收的能量分别为
、
、
,由此推知下列关系正确的是________
填选项字母
。
A.
高三化学填空题中等难度题查看答案及解析
-
(16分)甲醇是新型的汽车动力燃料。工业上可通过H2和CO化合制备甲醇,该反应的热化学方程式为:2H2(g)+CO(g)
CH3OH(g)
(1)已知:
1 mol甲醇气体完全燃烧生成CO
和水蒸气的热化学方程式为________。
(2)下列措施中有利于提高2H2(g)+CO(g)
CH3OH(g)反应速率的是________(双选)。
A.分离出CH3OH B.升高温度 C.减小压强 D.加入合适的催化剂
(3)(3)用H2和CO化合制备甲醇的反应中,若反应的容积为1L的恒容容器,分别在230℃、250℃和270℃下,改变H2和CO的起始组成比(起始时CO的物质的量固定为1mol)进行实验,结果如下图所示(图中曲线上的点都为一定温度下、一定组成下的平衡点):
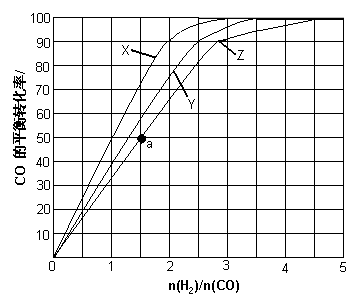
①曲线X对应的温度是________。
②从图中可以得出的结论有________(任写一条)。
(4)若往反应的容积中加入1.5molH2 和1.0molCO,在曲线Z对应温度下反应达平衡。利用上述图中a点对应的CO平衡转化率,计算2H2(g)+CO(g)
CH3OH(g)的平衡常数。(写出计算过程)
高三化学计算题中等难度题查看答案及解析
-
下列有关金属及其化合物的说法正确的是,
A. 钠在空气中燃烧生成白色固体Na2O2
B. Mg在空气中燃烧,其生成物只有MgO
C. 铁在高温下与水蒸气反应生成Fe3O4和H2
D. 铝、铁、铜在潮湿的空气中易生锈生成对应的氧化物
高三化学单选题中等难度题查看答案及解析
-
煤燃烧的反应热可通过以下两个途径来利用:
a.利用煤在充足的空气中直接燃烧产生的反应热;
b.先使煤与水蒸气反应得到氢气和一氧化碳.然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的化学方程式为:
a.C(s)+O2(g)═CO2(g)△H=E1 ①
b.C(s)+H2O(g)═CO(g)+H2(g)△H=E2 ②
H2(g)+
O2(g)═H2O(g)△H=E3 ③
CO(g)+
O2(g)═CO2(g)△H=E4 ④
(1)途径b相比途径a有较多的优点,请写出其中一点: ;
(2)上述四个热化学方程式△H>0的是 (填写序号);
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是
A.a比b多 B.a比b少 C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为 .
高三化学填空题困难题查看答案及解析
-
下列操作或装置能达到实验目的是( )
A. 分离互溶但沸点相差较大的液体混合物

B. 钠在空气中燃烧
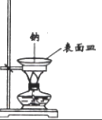
C. 检验铁粉与水蒸气反应生成氢气
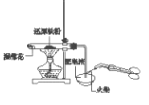
D. 探究碳酸钠与碳酸氢钠的稳定性
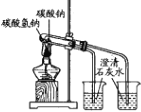
高三化学单选题中等难度题查看答案及解析