-
汽车尾气中含有NO2、NO和CO等有害气体,现取标准状况下22.4 L汽车尾气,研究发现该气体通过催化转化器后,上述三种有害气体可被完全转化为无害的N2和CO2,再取等体积尾气通入0.1 mol/L 50 mL NaOH溶液中,其中的NO2和NO恰好被完全吸收。则尾气中CO的体积分数可能为(说明:汽车尾气中其它成分气体与CO和NaOH溶液均不反应)( )
A.0.4% B.0.8% C.2% D.4%
高三化学单选题中等难度题查看答案及解析
-
汽车尾气中含有NO2、NO和CO等有害气体,现取标准状况下22.4 L汽车尾气,研究发现该气体通过催化转化器后,上述三种有害气体可被完全转化为无害的N2和CO2,再取等体积尾气通入0.1 mol/L 50 mL NaOH溶液中,其中的NO2和NO恰好被完全吸收。则尾气中CO的体积分数可能为(说明:汽车尾气中其它成分气体与CO和NaOH溶液均不反应)( )
A. 0.4% B. 0.8% C. 2% D. 4%
高三化学单选题困难题查看答案及解析
-
下列对于
说法不正确的是( )
A.已知:
,
,要使
与NO混合气体完全被 NaOH 吸收,则混合气体中物质的量:
B.汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为
和
,该装置中的催化剂可降低NO和CO反应的活化能,有利于提高该反应的平衡转化率
C.用
还原
生成N2和H2O,当消耗标况下
时转移
电子
D.装有 4L
与NO混合气体的容器,倒置于盛有水的水槽中,再通入相同条件下
,恰好充满,则
与NO体积比为1:1
高三化学单选题中等难度题查看答案及解析
-
工业制硝酸的尾气因为含有NO、NO2等有害物质而不能直接排放,工业上普遍采用催化还原法将NOx转化成N2和H2O而除去.下列式子是相应物质间的关系式(未配平):CH4+NO+NO2→N2+CO2+H2O有关说法不正确的是( )
A.物质的量之比可能是:CH4:NO:NO2=1:2:1
B.氧化性比较:NO2>NO>CO2
C.NO2既有氧化性又有还原性,在该反应中只有氧化性
D.将反应后的气体通过石灰水可得到纯净的氮气高三化学选择题中等难度题查看答案及解析
-
环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中的氮氧化物(NOx)、CO等有害气体,消除方法有多种。
(1)用稀土等催化剂能将汽车尾气中的CO、NOx、碳氢化合物转化成无毒物质,从而减少汽车尾气污染。已知:
①N2(g)+ O2(g)=2NO(g) △H=180.5 kJ/mol
②2C(s)+ O2(g)=2CO(g) △H=—221kJ/mol
③C(s)+ O2(g)=CO2(g) △H=—393. 5 kJ/mol
写出NO(g)与CO(g)催化转化成N2(g)和CO2(g)的热化学方程式__________________。
(2)①用甲烷催化还原氮的氧化物可消除氮氧化物的污染CH4(g)+4NO(g)
2N2(g)+CO2(g)+2H2O(g) ΔH=QkJ·mol-1,写出上述反应的平衡常数表达式_______,已知该反应的平衡常数K随温度升高而减小,则Q_______0(填“>”或“<”或“=”)。
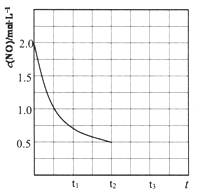
②某温度下,密闭容器中CH4与NO的起始浓度分别为1mol/L、2mol/L,其中c(NO)随时间变化如图所示,t2时达到平衡,保持温度不变在t2时将容器容积压缩到一半,请画出t2-t3 c(CH4)随时间变化的曲线。_______
(3)①为提高反应:CH4(g)+2NO2(g)
N2(g)+CO2(g)+2H2O(g)中的转化率,可以采取在恒压条件下充入稀有气体,解释其原因______________。
②电解吸收法处理氮氧化物废气的基本原理是用硝酸吸收氮氧化物生成NO2-,同时用石墨电极电解将NO2-转化成NO3-,电解条件下循环利用NO3-来处理氮氧化物。写出该法处理NO2总反应的化学方程式_______。
高三化学简答题中等难度题查看答案及解析
-
下列说法不正确的是
A.“煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气
B.汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,有利于提高该反应的平衡转化率
C.2014年诺贝尔化学奖授予美国科学家埃里克·贝齐格、威廉·莫纳和德国科学家斯特凡·黑尔,以表彰他们为发展超分辨率荧光显微镜所作的贡献,利用此类显微镜可以观察病毒以及活细胞内蛋白质等大分子
D.“地沟油”经过加工处理后,可以用来制肥皂和生物柴油,实现厨余废物合理利用
高三化学选择题简单题查看答案及解析
-
(1)汽车尾气中的CO、NO、NO2等有毒气体会危害人体健康,可在汽车尾部加催化转化器,将有毒气体转化为无毒气体。
已知:①2NO(g)+O2(g)=2NO2(g) △H1=-112.3kJ·mol-1
②NO2(g)+CO(g)=NO(g)+CO2(g) △H2=-234kJ·mol-1
③N2(g)+O2(g)=2NO(g) △H3=+179.5kJ·mol-1
请写出CO和NO2生成无污染气体的热化学方程式___。
(2)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g)
N2(g)+2CO2(g) △H=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随n(CO)/n(NO)的变化曲线如图1。
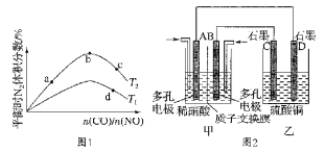
①b点时,平衡体系中C、N原子个数之比接近___;
②a、b、c三点CO的转化率从大到小的顺序为___;a、c、d三点的平衡常数从大到小的顺序为___。
③若n(CO)/n(NO)=0.8,反应达平衡时,N2的体积分数为20%,则CO的转化率为__。
(3)若将NO2与O2通入甲中设计成如图2所示装置,D电极上有红色物质析出,则A电极处通入的气体为____(填化学式);A电极的电极反应式为____;一段时间后,若乙中需加0.2molCu(OH)2使溶液复原,则转移的电子数为___。
(4)已知:25℃时,H2C2O4的电离常数Ka1=5.9×10—2,Ka2=6.4×10-5,则25℃时,0.1mol·L-1NaHC2O4溶液中各离子浓度由大到小的顺序为____,若向该溶液中加入一定量NaOH固体,使c(HC2O4-)=c(C2O42-),则此时溶液呈___(填“酸性”“碱性”或“中性”)。
高三化学综合题中等难度题查看答案及解析
-
CO和NO都是汽车尾气中的有害气体,它们在催化转化器中能反应生成氮气和
,对此反应,下列说法中错误的是( )
A.改变压强不可以改变反应速率 B.使用催化剂能同时增大正、逆反应的速率
C.增加压强能增大反应速率 D.升高温度能增大反应速率
高三化学单选题简单题查看答案及解析
-
下列说法正确的是( )
A.填埋法是垃圾处理的最佳方法
B.酸雨形成的主要原因是汽车尾气的任意排放
C.汽车排气管上的“催化转化器”能减少有害气体排放
D.实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液高三化学选择题中等难度题查看答案及解析
-
下列说法正确的是
A.填埋法是垃圾处理的最佳方法
B.酸雨形成的主要原因是汽车尾气的任意排放
C.汽车排气管上的“催化转化器”能减少有害气体排放
D.实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液
高三化学选择题中等难度题查看答案及解析