-
探究浓度对化学平衡的影响,实验如下:
I.向5mL 0.05mol·L-1 FeCl3溶液中加入5mL 0.05mol·L-1 KI溶液(反应a),平衡后分为两等份
Ⅱ.向一份加入饱和KSCN溶液,变红(反应b);加入CCl4,振荡、静置,下层显极浅的紫色
Ⅲ.向另一份加入CCl4,振荡、静置,下层显紫红色
结合实验,下列说法不正确的是( )
A. 反应a为:2Fe3++ 2I- 2Fe2++I2
2Fe2++I2
B. Ⅱ中,反应a进行的程度大于反应b
C. 实验Ⅱ中变红的原理是:Fe3+ + 3SCN-  Fe(SCN)3
Fe(SCN)3
D. 比较水溶液中c(Fe2+):Ⅱ<Ⅲ
-
下列实验操作能达到实验目的的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 探究浓度对化学平衡的影响 | 向盛有2.5mL 0.005mol/L FeCl3,溶液的试管中加入 2.5mL 0.01 mol/L KSCN溶液,再滴加4滴饱和FeCl3溶液 |
| B | 从AlCl3溶液提取无水AlCl3 | 将AlCl3溶液灼烧蒸干 |
| C | 证明Ksp(AgCl)>Ksp(AgI) | 在2mL 0.01 mol/LAgNO3溶液中滴加1mL 0.1 mol/LNaCl溶液,再滴加lmL 0.1 mol/LKI溶液 |
| D | 配制澄淸的FeCl3浓溶液 | 将FeCl3固体置入少量水中搅拌 |
A. A B. B C. C D. D
-
下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究浓度对化学平衡的影响 | 向盛有2.5mL 0.005mol/L FeCl3,溶液的试管中加入2.5mL 0.015 mol/L KSCN溶液,再滴加4滴饱和FeCl3溶液 |
| B | 从FeCl3溶液提取无水FeCl3 | 将FeCl3溶液灼烧蒸干 |
| C | 证 明 Ksp(AgCl)>Ksp(AgI) | 在2mL 0.01 mol/LAgNO3溶液中滴加1mL0.01 mol/LHCl溶液,再滴加1mL 0.01 mol/LKI 溶液 |
| D | 配制澄清的FeCl3浓溶液 | 将FeCl3固体置入少量水中搅拌 |
A. A B. B C. C D. D
-
已知K2Cr2O7溶液中存在平衡: +H2O
+H2O 2
2 +2H+。K2Cr2O7为橙色,K 2CrO4为黄色。为探究浓度对化学平衡的影响,某兴趣小组设计了如下实验方案。
+2H+。K2Cr2O7为橙色,K 2CrO4为黄色。为探究浓度对化学平衡的影响,某兴趣小组设计了如下实验方案。
| 
5mL0.1mol/LK2Cr2O7溶液 | 序号 | 试剂X |
| ⅰ | 1mL1mol·L-1 K2Cr2O7 溶液 |
| ⅱ | 1mL1 mol·L-1 K2CrO4溶液 |
| ⅲ | 5~15滴浓硫酸 |
| ⅳ | 5~15滴浓盐酸 |
| ⅴ | 5~15滴6 mol·L-1 NaOH溶液 |
Ⅰ.方案讨论
(1)ⅰ~ⅴ中依据减少生成物浓度可导致平衡移动的原理设计的是_____(填序号)。
(2)已知BaCrO4为黄色沉淀。某同学认为试剂X还可设计为Ba(NO3)2溶液,加入该试剂后,溶液颜色将_____。(填“变深”、“变浅”或“不变”)。
Ⅱ.实验分析
| 序号 | 试剂X | 预期现象 | 实际现象 |
| ⅰ | 1 mL1 mol·L-1 K2Cr2O7 溶液 | 溶液变黄 | 溶液橙色加深 |
| ⅱ | 1mL1 mol·L-1 K2CrO4溶液 | 溶液橙色加深 | 溶液颜色变浅 |
| ⅲ | 5~15滴浓硫酸 | 溶液橙色加深 | 溶液橙色加深 |
| ⅳ | 5~15滴浓盐酸 | 溶液橙色加深 | 无明显现象 |
| ⅴ | 5~15滴6mol·L-1NaOH溶液 | 溶液变黄 | 溶液变黄 |
(1)实验ⅰ没有观察到预期现象的原因是_____,实验ⅱ的原因与其相似。
(2)通过实验ⅲ和ⅴ得出的结论为_____。
(3)实验ⅳ无明显现象,可能的原因是____________。
(4)某同学查阅资料发现:K2Cr2O7溶液与浓盐酸可发生氧化还原反应。但实验ⅳ中没有观察到明显现象,小组同学设计了下实验,验证了该反应的发生。
方案:取5 mL浓盐酸,向其中加入15滴0.1mol·L-1 K2Cr2O7溶液,一段时间后,溶液变为绿色(CrCl3水溶液呈绿色),有黄绿色气体生成。写出该变化的化学方程式______。
-
某研究性小组决定用实验探究的方法证明化学反应具有一定的限度。取5mL 0.1mol/L KI溶液于试管中,滴加0.1mol/L FeCl3溶液2mL,发生如下反应:2Fe3++2I- 2Fe2++I2。为证明该反应具有可逆性且具有限度,他们设计了如下实验:
2Fe2++I2。为证明该反应具有可逆性且具有限度,他们设计了如下实验:
①取少量反应液,滴加AgNO3溶液,发现有少量黄色沉淀(AgI),证明反应物没有反应完全;
②再取少量反应液,加入少量CCl4,振荡,发现CCl4层显浅紫色,证明萃取到I2,即有I2生成。综合①②的结论,他们得出该反应具有一定的可逆性,在一定条件下会达到反应限度。
(1)老师指出他们上述实验中①不合理,你认为是_____________________________;在不改变反应物用量的前提下,改进的方法是_____________________________________________。
(2)有人认为步骤②适合检验生成I2较多的情况下,还有一种简便方法可以灵敏地检验是否生成了I2,这种方法是______________________________。
(3)控制适合的条件,将反应2Fe3++2I- 2Fe2++I2,设计成如图所示的原电池。
2Fe2++I2,设计成如图所示的原电池。
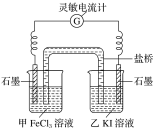
①反应开始时,乙中石墨电极上发生____________(填“氧化”或“还原”)反应,电极反应式为_________________________。
②电流计读数为0时,反应达到平衡状态。此时在甲中加入FeCl2固体,发现电流计又发生偏转,则甲中的石墨作_______(填“正”或“负”)极,该电极的电极反应式为_________________________。
-
下列实验不正确的是
| 序号 | 实验内容 | 实验目的 |
| A | 向5mL0.1mol/LK2Cr2O7溶液中滴加5滴浓硫酸 | 探究反应物浓度增大对化学平衡的影响 |
| B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶 液 | 说明一种沉淀能转化为另 一种溶解度更小的沉淀 |
| C | 室温下,用pH计测定浓度为0.1mol·L−1NaClO溶液和0.1mol·L−1CH3COONa溶液的pH | 比较 HClO 和 CH3COOH 的 酸性强弱 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
A. A B. B C. C D. D
-
下列实验不正确的是
| 序号 | 实验内容 | 实验目的 |
| A | 向5mL0.1mol/LK2Cr2O7溶液中滴加5滴浓硫酸 | 探究反应物浓度增大对化学平衡的影响 |
| B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶 液 | 说明一种沉淀能转化为另 一种溶解度更小的沉淀 |
| C | 室温下,用pH计测定浓度为0.1mol·L−1NaClO溶液和0.1mol·L−1CH3COONa溶液的pH | 比较 HClO 和 CH3COOH 的 酸性强弱 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
A. A B. B C. C D. D
-
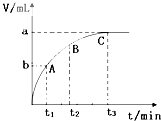
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
| 编号 | 操 作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中. | 试管A中不再产生气泡,试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL
10%H2O2溶液. | 试管A、B中均未见气泡产生 |
(1)过氧化氢分解的化学方程式为______ 2H2O+O2↑
-
将5mL 0.005mol/L FeCl3溶液和5mL 0.015mol/L KSCN溶液混合,达到平衡后呈红色。再将混合液分为5份,分别进行如下实验:下列说法不正确的是( )
| 
| 实验①:滴加4滴水,振荡 |
| 实验②:滴加4滴饱和FeCl3溶液,振荡 |
| 实验③:滴加4滴1 mol/L KCl溶液,振荡 |
| 实验④:滴加4滴1 mol/L KSCN溶液,振荡 |
| 实验⑤:滴加4滴6 mol/L NaOH溶液,振荡 |
A.对比实验①和②,为了证明增加反应物浓度,平衡发生正向移动
B.对比实验①和③,为了证明增加反应物浓度,平衡发生逆向移动
C.对比实验①和④,为了证明增加反应物浓度,平衡发生正向移动
D.对比实验①和⑤,为了证明减少反应物浓度,平衡发生逆向移动
-
为证明化学反应有一定的限度,进行如下探究活动:
I.取5mL0.1mol/L的KI溶液,滴加5至6滴FeCl3稀溶液;
Ⅱ.继续加入2mLCCl4振荡;
Ⅲ.取萃取后的上层清液,滴加KSCN溶液。
(1)探究活动I的实验现象为____________,探究活动Ⅱ的实验现象为_______________。
(2)为了测定探究活动I中的FeCl3稀溶液的浓度,现进行以下操作:
①移取20.00mLFeCl3稀溶液至锥形瓶中,加入___________用作指示剂,再用c mol/LKI标准溶液进行滴定,达到滴定终点时的现象是__________________________________________。
②重复滴定三次,平均耗用cmol/LKI标准溶液VmL,则FeCl3溶液物质的量浓度为_________mol/L。
③若滴定前滴定管尖嘴中无气泡,滴定后有气泡,则测定结果_________(填“偏高”或“偏低”或“不变”)。
Ⅳ.探究活动Ⅲ的意图是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色。对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+ 猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察,为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大;
信息二:Fe3+可与[Fe(CN)6]4—反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高。
结合新信息,现设计以下实验方案验证猜想:
①完成下表
| 实验操作 | 现象和结论 |
| 步骤一:取萃取后的上层清液滴加______________ | 若___________________________,则猜想一不成立。 |
| 步骤二:往探究Ⅲ所得溶液中加入少量乙醚,充分振荡、静置分层 | 若____________________________,则猜想二成立。 |
②写出实验操作“步骤一”中的反应离子方程式:_____________________________________。
2Fe2++I2
Fe(SCN)3



