-
MnO2在酸性溶液中具有强氧化性,可被还原为Mn2+,它还对H2O2的分解具有良好的催化效果.某兴趣小组通过实验研究MnO2性质.
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是________.
A.把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B.把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C.把MnO2固体加入到Na2SO3溶液中,再加入BaCl2溶液,观察是否有白色沉淀生成
D.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比实验:
①该小组从上述对比实验中,可以得出的结论是________.实验 外加试剂 现象 A 1滴0.2mol/LNaOH溶液 不变色 B 1滴水 缓慢变浅棕褐色 C 1滴0.1mol/L硫酸 迅速变棕褐色
②写出在酸性条件下MnO2氧化I-的离子方程式________.
(3)为了探究MnO2的催化效果,需要用30%的H2O2溶液(密度按1g/cm3)配制浓度为3%的H2O2溶液(密度按1g/cm3)100mL.配制过程中除了用到量筒、烧杯、100mL容量瓶外,还需用到的玻璃仪器名称是________,需用量筒量取________mL30%的H2O2溶液.MnO2催化H2O2分解的化学方程式为________,反应结束后将液体与MnO2分离的实验操作名称叫________.
(4)实验室用MnO2制取氯气的化学方程式为________.高三化学填空题中等难度题查看答案及解析
-
锰的化合物种类较多,也大多具有广泛的用途。
I. MnO2是H2O2分解的良好的催化剂,它也具有较强的氧化性。某化学兴趣小组通过实验探究MnO2的性质。
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是____________。
A.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
B.把MnO2固体加入到H2O2溶液中,观察是否有气泡产生
C.Na2SO3溶液中,加入MnO2固体,再滴加BaCl2溶液,观察是否有白色沉淀生成
D.FeSO4溶液中滴加几滴KSCN溶液,再加入MnO2固体,观察溶液是否变红
(2)为研究溶液中MnO2的氧化能力与溶液酸碱性的关系,该小组同学设计了如下的对比实验:在室温下,取A、B、C三支试管,用同浓度同体积的KI溶液和质量、颗粒大小相同的MnO2固体反应,然后分别加入1mL 0.2mol/L NaOH溶液、1mL水、1mL 0.1mol/L硫酸。现象记录如下:

①从以上实验中,我们可以得出的结论是_________________________________。
②写出C试管中发生反应的离子方程式:_________________________________。
Ⅱ,铁酸锰( MnFe2O4)可用于热化学循环分解水制氢,可有效缓解能源危机。MnFe2O4的制备工艺流程如下图:
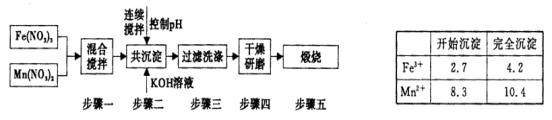
已知Fe3+、Mn2+沉淀的pH为上表所示。
①步骤一中投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比理论上应为_____________________。
②步骤二中需控制pH的范围是 ___________ 。
③步骤三中是否洗涤干净的判断方法是 _______________ 。
高三化学实验题极难题查看答案及解析
-
锰的化合物种类较多,也大多具有广泛的用途。
I.MnO2是H2O2分解的良好的催化剂,它也具有较强的氧化性。某化学兴趣小组通过实验探究MnO2的性质。
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是_____________。
A.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
B.把MnO2固体加入到H2O2溶液中,观察是否有气泡产生
C.Na2 SO3溶液中,加入MnO2固体,再滴加BaCl2溶液,观察是否有白色沉淀生成
D.FeSO4溶液中滴加几滴KSCN溶液,再加入MnO2固体,观察溶液是否变红
(2)为研究溶液中MnO2的氧化能力与溶液酸碱性的关系,该小组同学设计了如下的对比实验:在
室温下,取A、B、C三支试管,用同浓度同体积的KI溶液和质量、颗粒大小相同的MnO2固体反应,然后分别加入1mL 0.2mol/L NaOH溶液、1mL水、1mL 0.1mol/L硫酸。现象记录如下:
试管编号
实验现象
A
溶液不变色
B
溶液缓慢变浅棕褐色
C
溶液迅速变棕褐色
从以上实验中,我们可以得出的结论是____________。
②写出C试管中发生反应的离子方程式:________________。
Ⅱ,铁酸锰( MnFe2O4)可用于热化学循环分解水制氢,可有效缓解能源危机。MnFe2O4的制备工艺流程如下图:
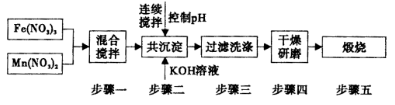
已知Fe3+、Mn2+沉淀的pH如表所示。
开始沉淀
完全沉淀
Fe3+
2.7
4.2
Mn2+
8.3
10.4
①步骤一中投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比理论上应为___________________。
②步骤二中需控制pH的范围是_______________
③步骤三中是否洗涤干净的判断方法是_____________.
高三化学填空题简单题查看答案及解析
-
研究催化剂对化学反应有重要意义。为探究催化剂对双氧水分解的催化效果,某研究小组做了如下实验:
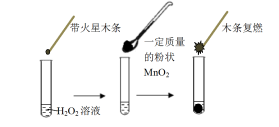
(1)甲同学欲用右图所示实验来证明MnO2是H2O2分解反应的催化剂。该实验 (填“能”或“不能”)达到目的,原因是 。
(2)为探究MnO2的量对催化效果的影响,乙同学分别量取50 mL 1% H2O2加入容器中,在一定质量范围内,加入不同质量的MnO2,测量所得气体体积,数据如下:
MnO2的质量/g
0.1
0.2
0.4
40s末O2体积/mL
49
61
86
由此得出的结论是 ,原因是 。
(3)为分析Fe3+和Cu2+对H2O2分解反应的催化效果,丙同学设计如下实验(三支试管中均盛有10 mL 5% H2O2 ) :
试管
Ⅰ
Ⅱ
Ⅲ
滴加试剂
5滴0.1 mol·L-1 FeCl3
5滴0.1 mol·L-1 CuCl2
5滴0.3 mol·L-1 NaCl
产生气泡情况
较快产生细小气泡
缓慢产生细小气泡
无气泡产生
结论是 ,实验Ⅲ的目的是 。
(4)① 查阅资料得知:将作为催化剂的FeCl3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的化学方程式分别是 和 (按反应发生的顺序写)。
② 在上述实验过程中,分别检测出溶液中有二价锰、二价铁和一价铜,由此得出选择作为H2O2分解反应的催化剂需要满足的条件是 。
高三化学实验题困难题查看答案及解析
-
某小组研究Na2S溶液与KMnO4溶液反应,探究过程如下。

资料:ⅰ.
在强酸性条件下被还原为Mn2+,在近中性条件下被还原为MnO2。
ⅱ. 单质硫可溶于硫化钠溶液,溶液呈淡黄色。
(1)根据实验可知,Na2S具有________性。
(2)甲同学预测实验I中S2–被氧化成
。
①根据实验现象,乙同学认为甲的预测不合理,理由是________。
②乙同学取实验I中少量溶液进行实验,检测到有
,得出S2–被氧化成
的结论,丙同学否定了该结论,理由是________。
③同学们经讨论后,设计了如下实验,证实该条件下
的确可以将S2–氧化成
。

a.右侧烧杯中的溶液是________。
b.连通后电流计指针偏转,一段时间后,________(填操作和现象)。
(3)实验I的现象与资料i存在差异,其原因是新生成的产物(Mn2+)与过量的反应物(
)发生反应,该反应的离子方程式是________。
(4)实验II的现象与资料也不完全相符,丁同学猜想其原因与(3)相似,经验证猜想成立,他的实验方案是______。
(5)反思该实验,反应物相同,而现象不同,体现了物质变化不仅与其自身的性质有关,还与________因素有关。
高三化学实验题中等难度题查看答案及解析
-
研究发现某些金属离子如Fe3+、Cu2+等对H2O2的分解也具有催化作用,为了比较MnO2与Fe3+和Cu2+的催化效果,某同学设计了如图甲、乙所示的实验.请回答相关问题:
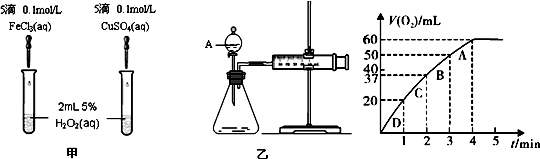
(1)定性分析:图甲可通过观察______,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3或者将CuSO4改为CuCl2更为合理,其理由是______.
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略.检查乙装置气密性的方法是______,实验中需要测量的数据是______.
(3)加入0.10mol MnO2粉末于50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示.
①写出H2O2在二氧化锰作用下发生反应的化学方程式______ 2H2O+O2↑高三化学解答题中等难度题查看答案及解析
-
(8分)经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
(1)定性分析:如图甲可通过观察___________________________________定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是____________________,
写出H2O2在二氧化锰作用下发生反应的化学方程式:
_____________________________________________________。

(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为________,实验中需要测量的数据是_________________。
高三化学实验题简单题查看答案及解析
-
经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验.回答相关问题:
(1)如图甲可通过观察______,比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是______.写出H2O2在二氧化锰作用下发生反应的化学方程式:______ 2H2O+O2↑
高三化学解答题中等难度题查看答案及解析
-
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)

已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g。
实验流程:
①往装置A中加入2.7mL(2.3 g)甲苯和125 mL水,然后分批次加入8.5 g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热。
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品。
③纯度测定:称取1.220g白色样品,配成100mL苯甲酸溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示。
第一次
第二次
第三次
第四次
体积(mL)
24.00
24.10
22.40
23.90
请回答:
(1)装置A的名称 。若不用温度计,本实验控制反应温度的措施为 。
(2)白色粗产品中除了KCl外,其他可能的无机杂质为____ 。
(3)操作②中趁热过滤的目的是 ,操作I的名称 。
(4)步骤③中用到的定量仪器有分析天平, ,50mL酸式、碱式滴定管。
(5)样品中苯甲酸纯度为 。
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果将 (填“偏大”、“偏小”或“不变”)。
高三化学实验题极难题查看答案及解析
-
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)

已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g。
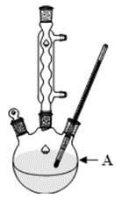
实验流程:
①往装置A中加入2.7mL(2.3 g)甲苯和125 mL水,然后分批次加入8.5 g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热。
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品。
③纯度测定:称取1.220g白色样品,配成100mL,甲醇溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示列举:
第一次
第二次
第三次
第四次
体积(mL)
24.00
24.10
22.40
23.90
请回答:
(1)装置A的名称________________________________________________________________________ 。若不用温度计,本实验控制反应温度的措施为________________________________________________________________________。
(2)白色粗产品中除了KCl外,其他可能的无机杂质为________________________________________________________________________________________________ 。
(3)操作I的名称________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
(4)步骤③中用到的定量仪器有________________________________________________________________________________________________________________________ ,100mL容量瓶,50mL酸式、碱式滴定管。
(5)样品中苯甲酸纯度为 ________________________________________________________________________________________________________________________________________________________________________。
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果________________________ ________________________________________(填“偏大”、“偏小”或“不变”)。
高三化学实验题中等难度题查看答案及解析