298K时,在20mLbmol·L-1氧氧化钠溶液中滴入0.10mol·L-1的醋酸,溶液的pH与所加醋酸的体积关系如图所示。下列有关叙述正确的是

A. a<20
B. C点溶液中:c(CH3COO-)+c(CH3C00H)=c(Na+)
C. A、B、C、D四点水的电离程度大小顺序为:D>B>C>A
D. 醋酸的电离平衡常数Ka=2.0×10-7/(0.la-2)
高三化学选择题困难题
298K时,在20mLbmol·L-1氧氧化钠溶液中滴入0.10mol·L-1的醋酸,溶液的pH与所加醋酸的体积关系如图所示。下列有关叙述正确的是

A. a<20
B. C点溶液中:c(CH3COO-)+c(CH3C00H)=c(Na+)
C. A、B、C、D四点水的电离程度大小顺序为:D>B>C>A
D. 醋酸的电离平衡常数Ka=2.0×10-7/(0.la-2)
高三化学选择题困难题
298K时,在20mLbmol·L-1氧氧化钠溶液中滴入0.10mol·L-1的醋酸,溶液的pH与所加醋酸的体积关系如图所示。下列有关叙述正确的是

A. a<20
B. C点溶液中:c(CH3COO-)+c(CH3C00H)=c(Na+)
C. A、B、C、D四点水的电离程度大小顺序为:D>B>C>A
D. 醋酸的电离平衡常数Ka=2.0×10-7/(0.la-2)
高三化学选择题困难题查看答案及解析
298K时,在20.0mL 0.10mol氨水中滴入0.10 mol
的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol
氨水的电离度为1.32%,下列有关叙述正确的是
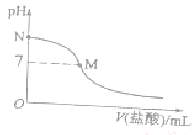
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D.N点处的溶液中pH<12
高三化学选择题困难题查看答案及解析
298K时,在20.0mL0.10mol·L-1氯水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。己知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是
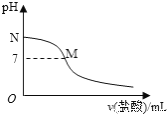
A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. N点处的溶液中pH<12
高三化学选择题困难题查看答案及解析
已知298K时,某碱MOH的电离平衡常数Kb=1.0×10-5;电离度a= 。在20.00mL0.1000mol/LMOH溶液中滴加0.10mol/L盐酸,测得溶液的pH、温度与所加盐酸的体积的关系如图所示。下列说法不正确的是
。在20.00mL0.1000mol/LMOH溶液中滴加0.10mol/L盐酸,测得溶液的pH、温度与所加盐酸的体积的关系如图所示。下列说法不正确的是
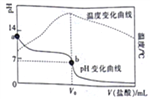
A. a点对应的溶液中:c(OH-)=(M+)+<(H+)
B. b点对应的V。=20.00mL
C. 298K时,0.1000mol/LMOH溶液中,MOH的电离度a=1%
D. 298K时,将0.1molMOH和0.1moMCl溶于水配制成1L混合溶液,溶液的pH>9
高三化学单选题困难题查看答案及解析
已知298K时,某碱MOH的电离平衡常数Kb=1.0×10-5;电离度a= 。在20.00mL0.1000mol/LMOH溶液中滴加0.10mol/L盐酸,测得溶液的pH、温度与所加盐酸的体积的关系如图所示。下列说法不正确的是
。在20.00mL0.1000mol/LMOH溶液中滴加0.10mol/L盐酸,测得溶液的pH、温度与所加盐酸的体积的关系如图所示。下列说法不正确的是
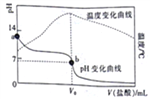
A. a点对应的溶液中:c(OH-)=(M+)+<(H+)
B. b点对应的V。=20.00mL
C. 298K时,0.1000mol/LMOH溶液中,MOH的电离度a=1%
D. 298K时,将0.1molMOH和0.1moMCl溶于水配制成1L混合溶液,溶液的pH>9
高三化学单选题困难题查看答案及解析
已知298K时,某碱MOH的电离平衡常数Kb=1.0×10-5;电离度a= 。在20.00mL0.1000mol/LMOH溶液中滴加0.10mol/L盐酸,测得溶液的pH、温度与所加盐酸的体积的关系如图所示。下列说法不正确的是
。在20.00mL0.1000mol/LMOH溶液中滴加0.10mol/L盐酸,测得溶液的pH、温度与所加盐酸的体积的关系如图所示。下列说法不正确的是
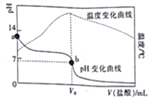
A. a点对应的溶液中:c(OH-)=(M+)+<(H+)
B. b点对应的V。=20.00mL
C. 298K时,0.1000mol/LMOH溶液中,MOH的电离度a=1%
D. 298K时,将0.1molMOH和0.1moMCl溶于水配制成1L混合溶液,溶液的pH>9
高三化学单选题困难题查看答案及解析
25℃时,将 0.10 mol•L-1的NaOH溶液逐滴滴入到20.00 mL 0.10 mol• L-1醋酸溶液中,溶液中的pH曲线与NaOH溶液体积的关系如图所示:
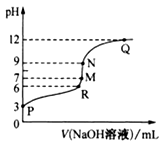
下列有关判断错误的是( )
A. 该温度下,醋酸的Ka的数量级为l0-5 B. N点对应的NaOH溶液体积可能为20.0mL
C. 溶液中,水的电离程度N点比Q点大 D. R点所示溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
高三化学选择题中等难度题查看答案及解析
25℃时,分别向20.00mL 0.10mol·L-1的氨水、醋酸铵溶液中滴加0.10mol·L-1的氢碘酸,溶液pH与加入氢碘酸体积的变化关系如图所示。下列说法正确的是

A.A点与B点由水电离产生的氢氧根浓度A点大于B点
B.M点,c(NH3·H2O)>c(OH-)>c(H+)>c(NH4+)
C.N点,c(I-)=c(NH3·H2O)+c(NH4+)
D.P点,c(H+)+c(CH3COOH)=c(OH-)+c(I-)+c(NH3·H2O)
高三化学多选题中等难度题查看答案及解析
常温下,向20mL0.10mol•L-1醋酸溶液中滴加0.10mol•L-1NaOH溶液,滴加过程中测得pH与NaOH溶液体积(V)的关系如图所示。下列说法正确的是( )
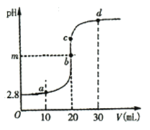
A.m=7
B.由水电离出的c(H+):a>b>c>d
C.由图可知,醋酸Ka的数量级为10-6
D.b与d之间的任意一点c都有:
高三化学单选题中等难度题查看答案及解析
室温下,用0.10 mol·L-1盐酸分别滴定20.00 mL 0.10 mol·L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示。下列说法不正确的是
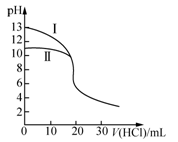
A.Ⅱ表示的是滴定氨水的曲线,当V(HCI)=20 mL时,有:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.当pH=7时,滴定氨水消耗的V(HCl)=20 mL,且c(NH4+)=c(Cl-)
C.滴定氢氧化钠溶液时,若V(HCl)>20 mL,则一定有:c(Cl-)>c(Na+)>c(H+)>c(OH-)
D.当滴定氨水消耗V(HCl)=10 mL时,有:2[c(OH-)-c(H+)]=c(NH4+)-c(NH3·H2O)
高三化学选择题极难题查看答案及解析