-
氮的重要化合物,如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等在生产、生活中具有重要作用。
(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
N2(g)+O2(g)=2NO(g) ΔH1=+229.3 kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH2=-906.5 kJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(g) ΔH3
则ΔH3 = kJ·mol-1
(2)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程产生的气体无毒,写出该反应的离子方程式
(3)在微电子工业中,NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示。
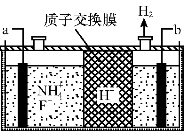
氮化硅的化学式为
a电极为电解池的 (填“阴”或“阳”)极,写出该电极的电极反应式
-
氮的重要化合物如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用。
(1) 利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g) △H1=44.0 kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2=229.3 kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-906.5 kJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H4
则△H4= kJ·mol-1。
(2) 使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
① 写出该反应的离子方程式: 。
② 在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为: ;为抑制肼的分解,可采取的合理措施有 (任写一种)。
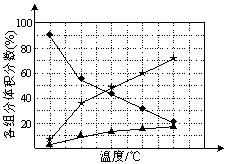
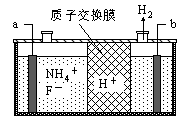
图1 图2
(3) 在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。
① 氮化硅的化学式为 。
② a电极为电解池的 (填“阴”或“阳”)极,写出该电极的电极反应式: ;电解过程中还会生成少量氧化性极强的气体单质,该气体的分子式是 。
-
(15分)氮的重要化合物如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用。
(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g) △H1=44.0 kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2=229.3 kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-906.5 kJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H4
则△H4= kJ·mol-1。
(2)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
①写出该反应的离子方程式: 。
②在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为: ;为抑制肼的分解,可采取的合理措施有 (任写一种)。
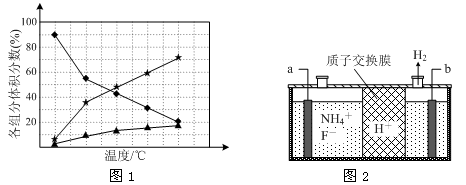
(3)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。
①氮化硅的化学式为 。
②a电极为电解池的 (填“阴”或“阳”)极,写出该电极的电极反应式: ;电解过程中还会生成少量氧化性极强的气体单质,该气体的分子式是 。
-
氮的重要化合物如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用.
(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g)△H1=44.0kJ•mol-1
N2(g)+O2(g)=2NO(g)△H2=229.3kJ•mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-906.5kJ•mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H4
则△H4=_____________kJ•mol-1.
(2)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
①写出该反应的离子方程式:_____________;
②在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝.若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为:_____________;为抑制肼的分解,可采取的合理措施有_____________(任写一种)。
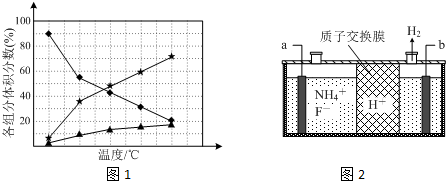
(3)在微电子工业中NF3常用作半导体、液晶和薄膜太阳能电池等生产过程的蚀刻剂,在对硅、氮化硅等材料进行蚀刻时具有非常优异的蚀刻速率和选择性,在被蚀刻物表明不留任何残留物,对表面物污染。工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。
①a电极为电解池的_____________(填“阴”或“阳”)极,写出该电极的电极反应式:_____________;
②以NF3对氮化硅(Si3N4)材料的蚀刻为例,用反应方程式来解释为什么在被蚀刻物表面不留任何残留物_____________。
③气体NF3不可燃但可助燃,故气体NF3应远离火种且与还原剂、易燃或可燃物等分开存放,结构决定性质,试从结构角度加以分析_____________。
④能与水发生反应,生成两种酸及一种气态氧化物,试写出相应的化学方程式_____________。
-
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。回答下列问题:
(1)肼(N2H4)是一种良好的火箭燃料,拉希格法是制备肼的传统方法,该方法是在5℃条件下,NaClO与NH3反应生成NH2Cl与NaOH,然后在140℃左右的条件下,将上述反应后混合物与氨混合,反应生成肼。上述两步反应中,氧化产物是______________(写化学式)。
(2)机动车尾气已成为城市大气的主要污染源,机动车尾气中的主要有害物质为氮的氧化物。目前科技工作者正在探索用甲烷等燃料气体将氮氧化物还原为N2和水,涉及到的反应有:
CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g) ΔH1=−574 kJ·mol−1
4NO(g)+CO2(g)+2H2O(g) ΔH1=−574 kJ·mol−1
CH4(g)+2NO2(g) CO2(g)+2H2O(g)+N2(g) ΔH2=−867 kJ·mol−1
CO2(g)+2H2O(g)+N2(g) ΔH2=−867 kJ·mol−1
写出CH4还原NO生成N2的热化学方程式:____________________________。
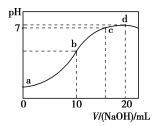
(3)变质的蔬菜类食物中含有亚硝酸盐,一定温度下,形成该盐的亚硝酸(HNO2)的电离常数Ka=4.0×10−4。在20 mL 0.01 mol·L−1的亚硝酸中逐滴滴加0.01 mol·L−1的NaOH溶液,测得混合液的pH变化如图,则图中a点的值为______,b点溶液呈酸性,其原因是__________________,d点溶液呈碱性,原因是______________________________。(已知lg2≈0.3)
(4)工业合成氨的反应原理为:N2(g)+ 3H2 (g) 2NH3(g) ΔH=a kJ·mol−1。保持反应体系的容积不变,在其中加入一定量的H2和N2,体系中各物质浓度随时间变化如图所示:
2NH3(g) ΔH=a kJ·mol−1。保持反应体系的容积不变,在其中加入一定量的H2和N2,体系中各物质浓度随时间变化如图所示:
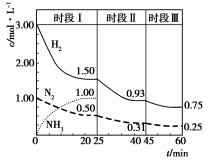
①若上述反应体系的容积为2 L,则0~20 min时间内,ν(H2)= ______________,该过程中放出的热量为94.4 kJ,则a=______________。
②25 min时将NH3从反应体系中完全分离出去,45 min时改变温度,在原图中画出25 min~60 min的NH3浓度变化曲线。
-
氮及其化合物在生产、生活中有极其重要的作用。
(1)我国长征系列运载火箭用肼(N2H4)作燃料。N2H4与NH3有相似的化学性质。
①写出肼与盐酸反应的离子方程式:____________。
②在火箭推进器中装有液态肼和双氧水,当它们混合时迅速反应生成氮气和水蒸气,写出反应的化学方程式:_ 。
③火箭发射时以肼为燃料,也可以用一氧化氮作氧化剂,反应过程中若转移2 mol电子, 则消耗燃料肼的质量为_ 。
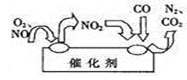
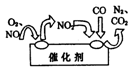
(2)汽车尾气中的氮氧化物是形成酸雨、酸雾的有毒气体之一,为了 减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。写出写出净化过程中总反应的化学方程式:_ 。
-
氮及其化合物在生产、生活中有极其重要的作用。
(1)我国长征系列运载火箭用肼(N2H4)作燃料。N2H4与NH3有相似的化学性质。
①写出肼与盐酸反应的离子方程式:_______________。
②在火箭推进剂中装有液态肼和双氧水,当它们混合时迅速反应生成氮气和水蒸气,写出反应的化学方程式:______________。
③火箭发射时以肼为燃料,也可以用一氧化氮作氧化剂,在此反应过程中若转移2 mol电子,则消耗燃料肼的质量为__________。
(2)汽车尾气中的氮氧化物是形成酸雨、酸雾的有毒气体之一,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。写出净化过程中总反应的化学方程式:_______________。
-
N2H4(联氨又称肼)一种无色发烟的、具有腐蚀性和强还原性的无色油状液体,它是一种重要的化工试剂,在生产和生活中有着重要的作用。
(1)推测有关N2H4的性质,下列说法正确的是
A.具有高度吸湿性、可燃性
B.有微弱的氨味,与甲醇,乙醇互溶,但不溶于乙醚、氯仿和苯
C.N2H4的水溶液呈弱碱性,
D.联氨的水溶液既有氧化性又有还原性,酸性溶液以氧化性为主,还原产物是N2,碱性溶液以还原性为主,氧化产物是NH4+
E.高温加热时分解为氮气、氢气和氨气。
(2)请写出N2H5+的电子式:__________________________
(3)在高锰酸钾催化剂存在下,尿素(CO(NH2)2)和次氯酸钠-氢氧化钠溶液反应制得联氨,它和水能按任意比例互相混溶,形成稳定的水合肼N2H4·H2O写出反应的离子方程式:______________________
(4)发射卫星可用肼为燃料,用NO2作氧化剂,二者发生反应生成氮气和水蒸气。已知:
N2(g)+2O2(g)=2NO2 (g) H=+67.7kJ•mol-1,N2H4(g)+O2(g)=N2(g)+2H2O(g) H=-534kJ•mol-1,
写出气态肼和NO2反应的热化学方程式__________。
(5)肼--空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,负极电极反应式是____________________________
-
氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因是:____________________________________________。
(2)在恒温条件下,1 mol NO2和足量C发生反应2NO2(g)+2C(s) N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
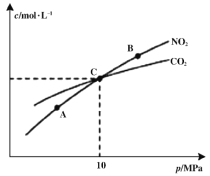
①A、B两点的浓度平衡常数关系:Kc(A) ___________Kc(B)(填“<”或“>”或“=”)
②A、B、C三点中NO2的转化率最高的是___________(填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp=___________MPa(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)已知:亚硝酸(HNO2)性质和硝酸类似,但它是一种弱酸。常温下亚硝酸的电离平衡常数Ka=5.1×10-4;H2CO3的Ka1=4.2×10-7,Ka2=5.61×10-11。在常温下向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小的顺序是______________________。
(4)已知:常温下甲胺(CH3NH2)的电离常数为Kb,且pKb=-lgKb=3.4水溶液中有CH3NH2+H2O⇌CH3NH3++OH-。常温下向CH3NH2溶液滴加稀硫酸至c(CH3NH2)=c(CH3NH3+)时,则溶液pH=_______。
(5)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下:
①CaSO4(s)+CO(g) ⇌CaO(s)+SO2(g)+CO2(g) △H=+210.5kJ· mol-1
②CaSO4(s)+4CO(g) ⇌CaS(s)+ 4CO2(g) △H=-189.2 kJ· mol-1
反应CaO(s)+3CO(g)+SO2(g) ⇌CaS(s)+3CO2(g) △H=___________ kJ· mol-1
-
氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因 。
(2)在恒温条件下,1 mol NO2和足量C发生反应:2NO2(g)+2C(s) N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
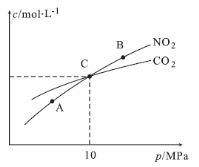
①A、B两点的浓度平衡常数关系:Kc(A) Kc(B)(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最高的是 (填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp= (列出表达式并计算结果。Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)亚硝酸的电离平衡常数Ka=5.1×10-4(298K)。它的性质和硝酸很类似。
①已知298K 时,H2CO₃的Ka1=4.2×10-7 ;Ka2=5.61×10-11。向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小是 。
②将10mL0.1mol/L的亚硝酸溶液加入到10mL0.1mol/L氨水(已知在25℃时,一水合氨的Ki= 1.8×10-5)中,最后所得溶液为________(填“酸性”、“碱性”或者“中性”)。
(4)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下:
①CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g)△H = +210.5kJ•mol-1
CaO(s)+SO2(g)+CO2(g)△H = +210.5kJ•mol-1
②CaSO4(s)+ 4CO(g) CaS(s)+ 4CO2(g) △H = -189.2kJ•mol-1
CaS(s)+ 4CO2(g) △H = -189.2kJ•mol-1
反应CaO(s)+3CO(g)+SO2(g)  CaS(s)+3CO2(g) △H= kJ•mol-1;
CaS(s)+3CO2(g) △H= kJ•mol-1;
(5)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10 mol·L-1H2S溶液中,通人HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。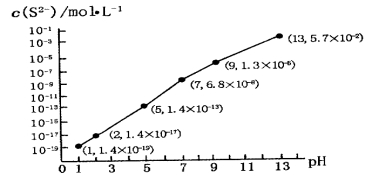
①pH=13时,溶液中的c(H2S)+c(HS-)=__________mol·L-1;
②某溶液含0.010 mol·L-1Fe2+和0.10 mol·L-1H2S,当溶液pH=______时,Fe2+开始沉淀。【已知:KSP(FeS)=1.4×10-19】











