10克Fe2O3、SiO2、Al2O3混合物加入足量的100 mL x mol/L稀硫酸中,过滤,然后加入10 mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积如图。以下叙述错误的是
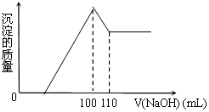
A.滤出的物质为SiO2
B.可求出x的值
C.可求出Al2O3的质量分数
D.可求出Fe2O3的质量分数
高三化学选择题中等难度题
10克Fe2O3、SiO2、Al2O3混合物加入足量的100 mL x mol/L稀硫酸中,过滤,然后加入10 mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积如图。以下叙述错误的是

A.滤出的物质为SiO2
B.可求出x的值
C.可求出Al2O3的质量分数
D.可求出Fe2O3的质量分数
高三化学选择题中等难度题
向10 g Fe2O3、SiO2和Al2O3的混合物中,加入100 mL x mol/L稀硫酸,过滤后,向滤液中加入10 mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示。下列叙述错误的是( )
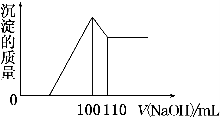
A.混合物和稀硫酸反应时,稀硫酸过量
B.可求出x的值
C.可求出Al2O3的质量分数
D.可求出Fe2O3的质量分数
高三化学选择题中等难度题查看答案及解析
10克Fe2O3、SiO2、Al2O3混合物加入足量的100 mL x mol/L稀硫酸中,过滤,然后加入10 mol/LNaOH溶液,产生沉淀的质量和加入NaOH溶液体积如下图。以下叙述错误的是
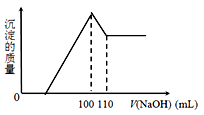
A.滤出的物质为SiO2
B.可求出x的值
C.可求出Al2O3的质量分数
D.可求出Fe2O3的质量分数
高三化学选择题困难题查看答案及解析
10克Fe2O3、SiO2、Al2O3混合物加入足量的100 mL x mol/L稀硫酸中,过滤,然后加入10 mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积如图。以下叙述错误的是

A.滤出的物质为SiO2
B.可求出x的值
C.可求出Al2O3的质量分数
D.可求出Fe2O3的质量分数
高三化学选择题中等难度题查看答案及解析
将10 g Fe2O3、SiO2、Al2O3的混合物加入足量的100 mL x mol/L稀硫酸中,过滤,然后加入10 mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液的体积关系如图所示。下列叙述错误的是
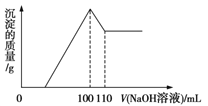
A.滤出的物质为SiO2
B.可求出x的值
C.可求出Al2O3的质量分数
D.可求出Fe2O3的质量分数
高三化学单选题中等难度题查看答案及解析
将1.0g Al2O3和MgO的混合物,溶解在过量的100mL浓度为0.5mol/L的硫酸溶液中,然后向其中加入NaOH溶液,使Al3+、Mg2+刚好全部转化为沉淀,所用100mLNaOH溶液的物质的量浓度为
A.0.5mol/L B.1.0mol/L C.1.5mo l/L D.2.0 mo l/L
高三化学选择题简单题查看答案及解析
有一包固体粉末是Fe2O3和Al2O3的均匀混合物。
(1)取4.22g样品,加入某浓度的盐酸100mL,恰好完全反应,该盐酸的物质的量浓度范围是:_____________________.。
(2)配制该浓度的盐酸需37%密度为1.19g/cm3浓盐酸,浓盐酸的物质的量浓度为。(保留2位小数)
(3)另取4.22g样品,加入2.0 mol/ L盐酸90ml恰好完全反应,则n(Fe2O3)和n(Al2O3)的物质的量之比是________。
(4)另取2.11g样品,加入pH=0的硫酸150ml中,样品完全溶解。在反应后的溶液中,逐滴加入2mol/ L的NaOH溶液。
① 当滴入amL时,开始产生沉淀,则amL。
②当生成沉淀的物质的量为0.025mol时,滴加氢氧化钠溶液的体积为________mL。
高三化学计算题困难题查看答案及解析
用含有Al2O3及少量Fe2O3和SiO2的铝土矿制备净水剂——液体聚合硫酸铝铁,工艺流程如下(部分操作和条件略):
I.向铝土矿中加入过量H2SO4后,加热、搅拌、过滤。
II.向滤液中加入一定量的FeSO4·7H2O和双氧水。
III.向溶液中加入Ca(OH)2固体,调节溶液的pH约为1,过滤。
IV.加入稳定剂,加热,得到产品。
(1)Fe2O3与H2SO4反应的离子方程式是___________。
(2)步骤I中过滤得到的滤渣成分是________(填化学式)。
(3)步骤I 中H2SO4的浓度与反应温度会影响铁与铝的浸出率。根据下图分析,步骤I 中H2SO4浓度的适宜范围是__________,反应的适宜温度是_________。
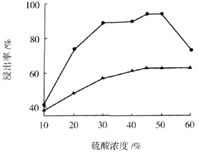
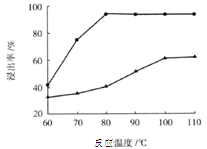
(4)步骤II中增大n(Fe3+)的离子方程式是_________。
(5)步骤III得到碱式硫酸铝铁[AlFe(OH)n(SO4)m]的溶液,则步骤II中应增大n(Fe3+)到
n(Al3+)﹕n(Fe3+)=________。
(6)研究表明,液体聚合硫酸铝铁的纯度越高,净水效果越好。已知:
一些物质在20℃时的溶解度
| 物质 | Ca(OH)2 | CaSO4 | Na2SO4 |
| 溶解度/g | 0.153 | 0.258 | 19.5 |
结合表中数据,解释步骤III中使用Ca(OH)2而不用NaOH的原因__________。
(7)铝土矿也可用于冶炼金属Al。以金属Al作阳极,稀硫酸作电解液,通过电解会使金属Al的表面生成致密坚硬的氧化膜,其电极反应式是_________。
高三化学填空题困难题查看答案及解析
(8分)某科研小组,用含有少量的CaO和Fe2O3的高岭土(主要成分:Al2O3·2SiO2·2H2O)来研制新型净水剂,其实验方案如下:将土样和纯碱混合均匀,加热熔融,冷却后用水浸取熔块,过滤弃去残渣,滤液用盐酸酸化,经过滤,分别得到沉淀和溶液,溶液即是净水剂。
(1)土样和纯碱混合均匀,加热熔融时,土样中的主要成分与纯碱反应的化学方程式为:
①________;②Al2O3+Na2CO32NaAlO2+CO2↑。
(提示:NaAlO2易溶于水并转化为Na[Al (OH)4])
(2)最后得到的沉淀物是________,生成沉淀的离子方程式为________。
(3)实验室中常备的坩埚有瓷坩埚,氧化铝坩埚和铁坩埚,本实验熔融土样时应选用________坩埚。
高三化学选择题简单题查看答案及解析
向盛有100 mL HCl溶液的烧杯中加入一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,充分反应后过滤,向滤液中加入5 mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如下图所示。则原HCl物质的量浓度是
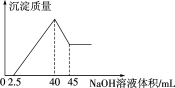
A.4mol/L B.3mol/L
C.2mol/L D.1mol/L
高三化学选择题困难题查看答案及解析
向盛有100 mL HCl溶液的烧杯中加入一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,充分反应后过滤,向滤液中加入5 mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如下图所示。则原HCl物质的量浓度是
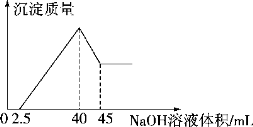
A.1mol/L B.2mol/L C. 3mol/L D.4mol/L
高三化学选择题困难题查看答案及解析