-
氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O = 2NaOH + H2↑ ②2Na2O2 + 2H2O = 4NaOH + O2↑
③Na2O + H2O =2NaOH ④2H2O 2H2↑+ O2↑ ⑤2F2 + 2H2O = 4HF + O2
2H2↑+ O2↑ ⑤2F2 + 2H2O = 4HF + O2
(1)其中不属于氧化还原反应的是____________(填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是___________(填编号);水只作还原
剂的反应是___________(填编号);水既作氧化剂,又作还原剂是_________(填编号);水既不作氧化剂,又不作还原剂是___________(填编号)。
(3)根据你的理解,氧化还原反应的特征是_____。
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O=2HNO3+NO是否属于氧化还原反应?______(填“是”或“不是”),若是,这个反应的氧化剂是_________,氧化产物是________,被氧化的氮元素与被还原的氮元素的物质的量之比是______;如果3mol的NO2完全反应,应转移____________个电子。
(Ⅱ)现有以下物质:(填序号)
① 铜 ② CO2 ③ 水 ④ CaCO3固体 ⑤ 蔗糖
以上物质中能导电的是______________,以上物质中属于电解质的是____________,以上物质中属于非电解质的________________。
-
氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O = 2NaOH + H2↑ ②2Na2O2 + 2H2O = 4NaOH + O2↑
③Na2O + H2O =2NaOH ④2H2O 2H2↑+ O2↑ ⑤2F2 + 2H2O = 4HF + O2
2H2↑+ O2↑ ⑤2F2 + 2H2O = 4HF + O2
(1)其中不属于氧化还原反应的是____________(填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是___________(填编号);水只作还原
剂的反应是___________(填编号);水既作氧化剂,又作还原剂是_________(填编号);水既不作氧化剂,又不作还原剂是___________(填编号)。
(3)根据你的理解,氧化还原反应的特征是_____。
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O=2HNO3+NO是否属于氧化还原反应?______(填“是”或“不是”),若是,这个反应的氧化剂是_________,氧化产物是________,被氧化的氮元素与被还原的氮元素的物质的量之比是______;如果3mol的NO2完全反应,应转移____________个电子。
(Ⅱ)现有以下物质:(填序号)
① 铜 ② CO2 ③ 水 ④ CaCO3固体 ⑤ 蔗糖
以上物质中能导电的是______________,以上物质中属于电解质的是____________,以上物质中属于非电解质的________________。
-
氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题。
(Ⅰ)下列一组有水参与的反应
①2Na+2H2O=2NaOH+H2↑
②2Na2O2+2H2O=4NaOH+O2↑
③Na2O+H2O=2NaOH
④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O  2H2↑+O2↑
2H2↑+O2↑
⑥2F2+2H2O=4HF+O2
(1)其中不属于氧化还原反应的是_____________(填编号)。
(2)在这些氧化还原反应中,水既作氧化剂,又作还原剂是___________(填编号),水既不作氧化剂,又不作还原剂是__________(填编号)。
(3)请你运用所学知识分析3NO2+H2O=2HNO3+NO是否属于氧化还原反应?___________(填“是”或“不是”),若是,这个反应的氧化剂和还原剂的质量比是________;
(Ⅱ)写出下列反应的离子方程式
①铜片与稀硝酸的反应_____________________________________;
②往氯化铝溶液中加入过量的NaOH溶液______________________;
(Ⅲ)写出下列反应的化学方程式
①二氧化硫发生催化氧化反应_________________________________;
②制漂白液的反应____________________________。
-
氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na+2H2O=2NaOH+H2↑
②2Na2O2+2H2O=4NaOH+O2↑
③Na2O+H2O=2NaOH
④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O 2H2↑+O2↑
2H2↑+O2↑
⑥2F2+2H2O=4HF+O2
(1)其中不属于氧化还原反应的是________(填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是________(填编号)
水只作还原剂的反应是________(填编号)水既作氧化剂,又作还原剂是________(填编号)
水既不作氧化剂,又不作还原剂是________(填编号)
(3)根据你的理解,氧化还原反应的实质是________
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O=2HNO3+NO是否属于氧化还原反应?________(填“是”或“不是”),若是,这个反应的氧化剂是________,还原剂是________.
(Ⅱ)写出下列反应的离子方程式:
①往氯化铁溶液加入铁粉:________
②过量二氧化碳通入澄清石灰水:________
③往氯化铝溶液中加入足量的NaOH溶液:________
(Ⅲ)写出下列反应的化学方程式:
①二氧化硫发生催化氧化反应:________
②氯气与氢氧化钠溶液反应:________
③铜片与稀硝酸的反应:________.
-
氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na+2H2O=2NaOH+H2↑
②2Na2O2+2H2O=4NaOH+O2↑
③Na2O+H2O=2NaOH
④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O 2H2↑+O2↑
2H2↑+O2↑
⑥2F2+2H2O=4HF+O2
(1)其中不属于氧化还原反应的是________(填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是________(填编号)
水只作还原剂的反应是________(填编号)水既作氧化剂,又作还原剂是________(填编号)
水既不作氧化剂,又不作还原剂是________(填编号)
(3)根据你的理解,氧化还原反应的实质是________
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O=2HNO3+NO是否属于氧化还原反应?________(填“是”或“不是”),若是,这个反应的氧化剂是________,还原剂是________.
(Ⅱ)写出下列反应的离子方程式:
①往氯化铁溶液加入铁粉:________
②过量二氧化碳通入澄清石灰水:________
③往氯化铝溶液中加入足量的NaOH溶液:________
(Ⅲ)写出下列反应的化学方程式:
①二氧化硫发生催化氧化反应:________
②氯气与氢氧化钠溶液反应:________
③铜片与稀硝酸的反应:________.
-
氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O = 2NaOH + H2↑ ②2Na2O2 + 2H2O = 4NaOH + O2↑
③Na2O + H2O =2NaOH ④2H2O 2H2↑+ O2↑ ⑤2F2 + 2H2O = 4HF + O2
2H2↑+ O2↑ ⑤2F2 + 2H2O = 4HF + O2
(1)其中不属于氧化还原反应的是____________(填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是___________(填编号);水只作还原
剂的反应是___________(填编号);水既作氧化剂,又作还原剂是_________(填编号);水既不作氧化剂,又不作还原剂是___________(填编号)。
(3)根据你的理解,氧化还原反应的特征是_____。
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O=2HNO3+NO是否属于氧化还原反应?______(填“是”或“不是”),若是,这个反应的氧化剂是_________,氧化产物是________,被氧化的氮元素与被还原的氮元素的物质的量之比是______;如果3mol的NO2完全反应,应转移____________个电子。
(Ⅱ)现有以下物质:(填序号)
① 铜 ② CO2 ③ 水 ④ CaCO3固体 ⑤ 蔗糖
以上物质中能导电的是______________,以上物质中属于电解质的是____________,以上物质中属于非电解质的________________。
-
(方程式每空2分,其余每空1分,共20分。)氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O = 2NaOH + H2↑ ②2Na2O2 + 2H2O = 4NaOH + O2↑
③Na2O + H2O =2NaOH ④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O 2H2↑+ O2↑ ⑥2F2 + 2H2O = 4HF + O2
2H2↑+ O2↑ ⑥2F2 + 2H2O = 4HF + O2
(1)其中不属于氧化还原反应的是 (填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是 (填编号)
水只作还原剂的反应是 (填编号)
水既作氧化剂,又作还原剂是 (填编号)
水既不作氧化剂,又不作还原剂是 (填编号)
(3)根据你的理解,氧化还原反应的实质是( )
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O = 2HNO3+NO是否属于氧化还原反应? (填“是”或“不是”),若是,这个反应的氧化剂和还原剂的质量比是 。
(Ⅱ)写出下列反应的离子方程式:
①铜片与稀硝酸的反应:
②过量二氧化碳通入澄清石灰水:
③往氯化铝溶液中加入过量的NaOH溶液:
(Ⅲ)写出下列反应的化学方程式:
①二氧化硫发生催化氧化反应:
②制漂白液的反应:
③雕刻花玻璃的反应:
-
(方程式每空2分,其余每空1分,共21分。)氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O =" 2NaOH" + H2↑
②2Na2O2 + 2H2O =" 4NaOH" + O2↑
③Na2O+ H2O ="2NaOH"
④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O 2H2↑+ O2↑
2H2↑+ O2↑
⑥2F2 + 2H2O =" 4HF" + O2
(1)其中不属于氧化还原反应的是________(填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是________(填编号)
水只作还原剂的反应是________(填编号)水既作氧化剂,又作还原剂是________(填编号)
水既不作氧化剂,又不作还原剂是________(填编号)
(3)根据你的理解,氧化还原反应的实质是( )
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O = 2HNO3+NO是否属于氧化还原反应?________(填“是”或“不是”),若是,这个反应的氧化剂是________,还原剂是________。
(Ⅱ)写出下列反应的离子方程式:
①往氯化铁溶液加入铁粉:________
②过量二氧化碳通入澄清石灰水:________
③往氯化铝溶液中加入足量的NaOH溶液:________
(Ⅲ)写出下列反应的化学方程式:
①二氧化硫发生催化氧化反应:________
②氯气与氢氧化钠溶液反应:________
③铜片与稀硝酸的反应:________
-
(12分)离子反应是中学化学中重要的反应类型。回答下列问题:
(1)人们常用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下左图。下右图为离子反应、氧化还原反应和置换反应三者之间的关系,则表示离子反应、氧化还原反应、置换反应的字母分别是________

(2)将NaBr溶液加入AgC1沉淀中,产生AgBr黄色沉淀。从离子反应发生的条件分析,AgCl与AgBr相比较,溶解度较大的是________。
(3)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点。反应物从下列物质中选取:Ca(OH)2、Fe、H2O、CO2、H2SO4、HCl、NaOH、Ba(OH)2、CuCl2、
| 错误观点 | “否定的”离子方程式 |
| ① | 所有碱溶液与CO2反应均可以表示为: 2OHˉ+CO2 =H2O+ CO32— | |
| ② | 所有酸碱中和反应均可表示为: H++OHˉ=H2O | |
-
Ⅰ.离子反应和氧化还原反应都是高中化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有______。(填序号)
①单质 ②化合物 ③氧化物 ④酸 ⑤碱 ⑥盐 ⑦电解质
人们常用图示法表示不同反应类型之间的关系,如化合反应和氧化还原反应的关系可用图1表示。图2为离子反应、氧化还原反应和置换反应三者之间的关系,则表示置换反应的是____(填字母),请写出符合图2阴影部分的一个离子方程式______。
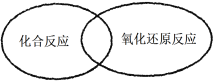
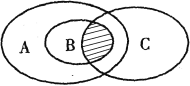
图1 图2
Ⅱ.现有失去标签的四瓶无色溶液A,B,C,D,只知它们是K2CO3,K2SO4,Na HSO4和Ba(NO3)2,为鉴别它们,进行如下实验:
①A+D→溶液+气体 ②B+C→溶液+沉淀
③B+D→溶液+沉淀 ④A+B→溶液+沉淀
⑤将④得到的沉淀物加入③所得的溶液中,沉淀很快溶解并产生无色无味的气体。
根据以上实验事实,请完成如下问题:
(3)写出各物质化学式:A__________;B__________;C__________;D__________。
(4)写出实验③中反应中相关的离子方程式。____________________________。
(5)书写离子方程式
①NaHCO3溶液与H2SO4溶液混合:_________________________。
②向石灰水中通入过量二氧化碳________________________________。
③氢氧化亚铁和浓盐酸反应____________________________________。
④醋酸溶液和碳酸镁悬浊液混合生成气体并得到澄清溶液______________________________。
2H2↑+ O2↑ ⑤2F2 + 2H2O = 4HF + O2


