-
硫代硫酸钠(Na2S2O3)俗称大苏打,主要用于照相业作定影剂。Na2S2O3易溶于水,在酸性溶液中会迅速分解,具有较强的还原性。
(1)Na2S2O3溶液与足量氯水反应的离子方程式为______________________________________________。(S元素被氧化为SO42-)
(2)硫代硫酸钠(Na2S2O3)露置在空气中易氧化变质,其可能的变质后生成物如下:
假设一:________
假设二: 只有Na2SO4固体
假设三:________
(3)现有一瓶Na2S2O3固体,可能混有Na2SO4固体。设计实验验证该假设,写出实验步骤、预期现象和结论。限选试剂: 1mol·L-1 H2SO4、1mol·L-1HNO3、1mol·L-1HCl、1mol·L-1NaOH、0. 1 mol·L-1BaCl2、0.01 mol·L-1 KMnO4、蒸馏水。
实验步骤
预期现象和结论
步骤1:取少量固体于试管中,加蒸馏水溶解。
步骤2:
步骤3:
高三化学填空题简单题查看答案及解析
-
硫代硫酸钠(Na2S2O3)俗称大苏打,照相业中用作定影剂。Na2S2O3易溶于水,在酸性溶液中与酸反应有单质硫和SO2生成。
(1)Na2S2O3溶液与稀硫酸混合反应可用于探究外界条件对反应速率的影响,完成有关的实验设计表(已知各溶液体积均为5 mL):
实验编号
T/K
c(Na2S2O3)/ mol·L-1
c(H2SO4)/ mol·L-1
实验目的
①
298
0.1
0.1
实验①和②探究温度对该反应速率的影响;实验①、③和④探究反应物浓度对该反应速率的影响
②
308
③
0.2
④
0.1
(2)Na2S2O3还具有很强的还原性,Na2S2O3溶液与足量氯水反应的化学方程式为:
________________ (提示:S元素被氧化为SO)。
(3)现有一瓶Na2S2O3固体,可能含有Na2SO4固体,请设计实验验证,写出实验步骤、预期现象和结论。限选试剂: 1 mol·L-1 H2SO4、1 mol·L-1 HNO3、1 mol·L-1 HCl、1 mol·L-1 NaOH、0.1 mol·L-1 BaCl2、0.01 mol·L-1 KMnO4、蒸馏水。
实验步骤
预期现象和结论
步骤1:取少量固体于试管中,加蒸馏水溶解
步骤2:
步骤3:
高三化学实验题极难题查看答案及解析
-
硫代硫酸钠(Na2S2O3)俗称大苏打,照相业中用作定影剂。Na2S2O3易溶于水,在酸性溶液中与酸反应有单质硫和SO2生成。
(1)Na2S2O3溶液与稀硫酸混合反应可用于探究外界条件对反应速率的影响,完成有关的实验设计表(已知各溶液体积均为5 mL):
实验编号
T/K
c(Na2S2O3)/ mol·L-1
c(H2SO4)/ mol·L-1
实验目的
①
298
0.1
0.1
实验①和②探究温度对该反应速率的影响;
实验①和③探究反应物浓度对该反应速率的影响
②
308
③
0.2
(2)Na2S2O3还具有很强的还原性,Na2S2O3溶液与足量氯水反应的化学方程式为:
________________ (提示:S元素被氧化为SO42-)。
(3)现有一瓶Na2S2O3固体,可能含有Na2SO4固体,请设计实验验证,写出实验步骤、预期现象和结论。限选试剂:1 mol·L-1 H2SO4、1 mol·L-1 HNO3、1 mol·L-1 HCl、1 mol·L-1 NaOH、0.1 mol·L-1 Ba(NO3)2、0.1 mol·L-1 BaCl2、0.01 mol·L-1 KMnO4、蒸馏水。
实验步骤
预期现象和结论
步骤1:取少量固体于试管A中,加蒸馏水溶解。
步骤2:向试管A加入________
________
________
步骤3:取步骤2的少量上层清液于试管B中,________
________
________
________
高三化学实验题困难题查看答案及解析
-
硫代硫酸钠(Na2S2O3·5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。它易溶于水,难溶于乙醇,加热、易分解,在酸性溶液中不能稳定存在。工业上常用亚硫酸钠法、硫化碱法等制备。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如下图:
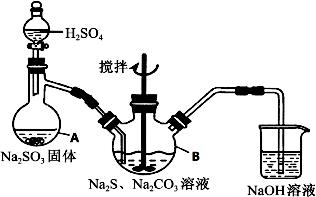
实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体。
③趁热过滤,将滤液加热浓缩,冷却析出Na2S2O3·5H2O。
④再经过滤、洗涤、干燥,得到所需的产品。
(1) 步骤④中洗涤时,为了减少产物的损失用的试剂可以是 。
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液pH<7,请用离子方程式表示原因 。
(3)写出三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式 。
(4)常用Na2S2O3溶液测定废水中Ba2+ 浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时全部转化为Cr2O72-;再加过量KI溶液,充分反应后得混合溶液V mL,将其平均分成4等份,加入淀粉溶液作指示剂,用0.0010 mol.L-1 的Na2S2O3溶液进行滴定,反应完全时,相关数据记录如下表所示:
编号
1
2
3
4
消耗Na2S2O3标准溶液的体积/mL
18.02
17.98
18.00
20.03
部分反应离子方程式为:
① Cr2O72-+6I-+14H+
2Cr3++3I2+7H2O; ②I2+2S2O32-
2I-+S4O62-。
①判断达到滴定终点的现象是__ _____________
②从表格所给数据计算:一份待测溶液消耗Na2S2O3溶液的平均体积为 ml
③废水中Ba2+的物质的量浓度__________________。
(5)Na2S2O3常用作脱氯剂,在溶液中易被Cl2氧化成SO42-,该反应的离子方程式为_________________。
高三化学实验题困难题查看答案及解析
-
硫代硫酸钠(Na2S2O3),又名大苏打、海波,主要用于照相业作定影剂、作鞣革时重铬酸盐的还原剂,易溶于水,遇酸易分解。其工艺制备流程如下:

某化学兴趣小组同学模拟该流程设计了如下实验装置:
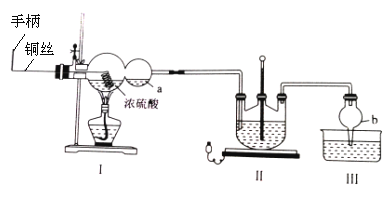
回答下列问题:
(1)a处可用来检验I中的反应是否发生,选用的试剂是______________,若要停止I中的化学反应,除停止加热外,还要采取的操作是________________________。
(2)加热I,使反应完全,发现浸入液面下的铜丝变黑,甲同学对黑色生成物提出如下假设:①可能是Cu2O ②可能是CuO;③可能是CuS;④_______。乙同学提出假设①一定不成立,该同学的依据是______;丙同学做了如下实验来验证黑色物质的组成:
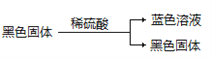
基于上述假设分析,黑色物质的组成为__________________________(填化学式)。
(3)II中发生反应的化学方程式为_____________________,实验中通入的SO2不能过量,可能的原因是______________________。
(4)为检验制得的硫代硫酸钠产品的纯度,该小组称取5.0g产品配成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:向锥形瓶中加入25.00mL 0.01mol·L-1的KIO3溶液,再加入过量的KI溶液并酸化,发生反应的离子方程式为___________,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应I2 + 2S2O32- == 2I- + S4O62-,当达到滴定终点时,消耗Na2S2O3溶液20.00mL,则该产品的纯度是____________(保留3个有效数字)。
(5)丁同学提出上述实验装置的设计存在不足,建议在I上__________;在I、II之间增加_____________。
高三化学实验题中等难度题查看答案及解析
-
硫代硫酸钠(Na2S2O3),又名大苏打、海波,主要用于照相业作定影剂、作鞣革时重铬酸盐的还原剂,易溶于水,遇酸易分解。其工艺制备流程如下:

某化学兴趣小组同学模拟该流程设计了如下实验装置:

回答下列问题:
(1)a处可用来检验I中的反应是否发生,选用的试剂是______________,若要停止I中的化学反应,除停止加热外,还要采取的操作是________________________。
(2)加热I,使反应完全,发现浸入液面下的铜丝变黑,甲同学对黑色生成物提出如下假设:①可能是Cu2O ②可能是CuO;③可能是CuS;④_______。乙同学提出假设①一定不成立,该同学的依据是______;丙同学做了如下实验来验证黑色物质的组成:

基于上述假设分析,黑色物质的组成为__________________________(填化学式)。
(3)II中发生反应的化学方程式为_____________________,实验中通入的SO2不能过量,可能的原因是______________________。
(4)为检验制得的硫代硫酸钠产品的纯度,该小组称取5.0g产品配成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:向锥形瓶中加入25.00mL 0.01mol·L-1的KIO3溶液,再加入过量的KI溶液并酸化,发生反应的离子方程式为___________,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应I2 + 2S2O32- == 2I- + S4O62-,当达到滴定终点时,消耗Na2S2O3溶液20.00mL,则该产品的纯度是____________(保留3个有效数字)。
(5)丁同学提出上述实验装置的设计存在不足,建议在I上__________;在I、II之间增加_____________。
高三化学实验题中等难度题查看答案及解析
-
硫代硫酸钠(Na2S2O3·5H2O),又名大苏打、海波,主要用于照相业作定影剂、作鞣革时重铬酸盐的还原剂,易溶于水,遇酸易分解。其工艺制备流程如下:
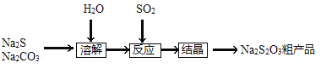
某化学兴趣小组同学模拟该流程设计了如下实验装置:
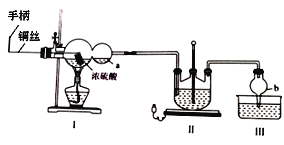
回答下列问题:
(1)双球管a处的液体可用来检验I中的反应是否发生,选用的试剂是______(填字母)
a、品红溶液 b、NaOH溶液 c、稀硫酸
若要停止I中的化学反应,除停止加热外,还要采取的操作是___________________。
(2)加热I,使反应完全,发现浸入液面下的铜丝变黑,甲同学对黑色生成物提出如下假设:①可能是Cu2O;②可能是CuO;③可能是CuS;④CuS和CuO的混合物。乙同学提出假设①一定不成立,该同学的依据是____________________________________;丙同学做了如下实验来验证黑色物质的组成:
基于上述假设分析,原黑色物质的组成为____________________(填化学式)。
(3)II中发生反应的化学方程式为_____________________,实验中通入的SO2不能过量,可能的原因是______________________________________________________。
(4)丁同学提出上述实验装置的设计存在不足,建议在I上_____________;在I、II之间增加_____________。
高三化学实验题中等难度题查看答案及解析
-
(15分)硫代硫酸钠(Na2S2O3·5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。它易溶于水,难溶于乙醇,加热、遇酸均易分解。工业上常用亚硫酸钠法、硫化碱法等制备。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如下图:

实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体。
③趁热过滤,将滤液加热浓缩,冷却析出Na2S2O3·5H2O。
④再经过滤、洗涤、干燥,得到所需的产品。
(1)写出仪器A的名称 步骤④中洗涤时,为了减少产物的损失用的试剂可以是 。
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液pH<7,请用离子方程式解释原因 。
(3)写出三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式 。
(4)最后得到的产品中可能含有Na2SO4杂质。请设计实验检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论: 。
(5)测定产品纯度
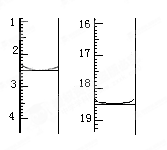
准确称取1.00 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。反应原理为2S2O32-+I2===S4O
+2I-。滴定起始和终点的液面位置如图:则消耗碘的标准溶液体积为_______mL。产品的纯度为 %。
(6)Na2S2O3常用作脱氯剂,在溶液中易被Cl2氧化成SO42-,该反应的离子方程式为__________________。
高三化学实验题极难题查看答案及解析
-
硫代硫酸钠(Na2S2O3·5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。它易溶于水,难溶于乙醇,加热、遇酸均易分解.工业上常用亚硫酸钠法、硫化碱法等制备.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图1:
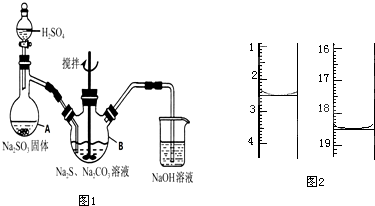
实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的SO2气体较均匀地
通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸.
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体.
③趁热过滤,将滤液加热浓缩,冷却析出Na2S2O3•5H2O.
④再经过滤、洗涤、干燥,得到所需的产品.
(1)写出仪器A的名称_____________,步骤④中洗涤时,为了减少产物的损失用的试剂可以是
___________;
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液pH<7,请用离子方程式解释原因___________;
(3)写出三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式___________;
(4)最后得到的产品中可能含有Na2SO4杂质.请设计实验检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论___________;
(5)测定产品纯度 准确称取1.00g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol•L-1碘的标准溶液滴定.反应原理为2S2O32-+I2═S4O62-+2I-.滴定起始和终点的液面位置如图2:则消耗碘的标准溶液体积为___________ mL,产品的纯度为___________。
高三化学实验题极难题查看答案及解析
-
(15分)硫代硫酸钠俗称保险粉,又名“大苏打”。可用于照相业作定影剂、纸浆漂白作脱氯剂,也可用于氰化物、砷、汞、铅、铋、碘等中毒的治疗,也是一种常用的实验试剂。
I.已知:Na2S2O3 + H2SO4 = Na2SO4 + S↓+ SO2 + H2O,某研究小组依据该反应探究外界条件对反应速率的影响,设计实验如下:
实验
编号
实验温度
/℃
Na2S2O3
H2SO4
蒸馏水体积
/mL
体积/mL
浓度/ mol·L-1
体积/mL
浓度/ mol·L-1
①
25
10
0.1
10
0.1
0
②
25
5
0.1
10
0.1
5
③
25
5
0.2
10
0.2
5
④
50
5
0.1
10
0.1
5
⑤
50
10
0.2
5
0.2
5
下列有关说法正确的是
A.实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响
B.实验①和③溶液变浑浊的时间相同
C.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和⑤
D.该同学在实验中采用的研究方法是实验比较法
II.实验室用SO2通入Na2S和Na2CO3的混合溶液中来制备硫代硫酸钠。反应原理为:
2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2
本实验对Na2S纯度要求较高,利用图1所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯过程为:将已称量好的工业级Na2S放入圆底烧瓶中,加入一定质量的酒精和少量水。按图1所示装配所需仪器,向冷凝管通入冷却水,同时水浴加热。待烧瓶中固体不再减少时,停止加热。将烧瓶取下,立即趁热过滤,再冷却结晶,过滤。将所得固体洗涤、干燥,得到Na2S·9H2O晶体。
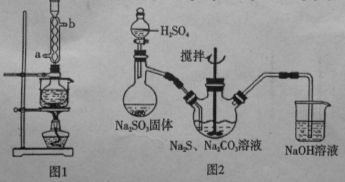
(1)在提纯过程中“趁热过滤”操作的目的是 ;
(2)用图2所示装置制取Na2S2O3,其中盛放Na2SO3固体的玻璃仪器名称是 ,NaOH溶液的作用是 。
(3)保险粉样品中Na2S2O3·5H2O的纯度(质量分数)可通过氧化还原滴定法测定,相关反应方程式为
2Na2S2O3+I2=2NaI+Na2S4O6。
准确称取W g样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用0.1000 mol•L¯1碘的标准溶液进行滴定。
请回答:
①到达滴定终点的标志 ;
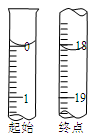
②滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为 mL,产品的纯度为 (设Na2S2O3•5H2O相对分子质量为M)。
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的纯度的测量结果 (填“偏高”、“偏低”或“不变”)。
高三化学实验题极难题查看答案及解析