-
实验室有质量分数为98%的浓硫酸,密度为1.84 g·cm-3。现要配制0.5 mol/L的稀硫酸450 mL,试回答下列问题:
(1)该浓硫酸的物质的量浓度为_________。配制稀硫酸时,应选用规格为______mL的容量瓶,经计算需要__________mL浓硫酸。
(2)在量取浓硫酸后,进行了下列操作,其正确顺序是________________(填序号)。
a. 待稀释硫酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
b. 往容量瓶中小心加蒸馏水至液面离刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的凹液面与刻度标线相切。
c. 用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
d. 将浓硫酸慢慢注入盛蒸馏水的烧杯中,边倒边用玻璃棒搅动,使其混合均匀。
e. 将容量瓶盖紧,反复上下颠倒,摇匀。
(3)下列操作会导致所配硫酸浓度偏低的是______。
A.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
B.用量筒量取浓硫酸时,俯视读数
C.定容时仰视容量瓶刻度线
D.定容摇匀后有少量溶液外流
E. 定容摇匀后,发现液面下降,继续加水至刻度线
高二化学实验题中等难度题查看答案及解析
-
某同学用质量分数为98%、密度为1.84 g/cm3的浓硫酸,配制100 mL 2 mol/L H2SO4溶液,并进行有关的实验。试回答下列问题:
(1)计算所需浓硫酸的体积。
(2)从下列仪器中选出实验所需要的仪器________(填序号)。
A.10 mL量筒 B.20 mL量筒 C.100 mL烧杯 D.100 mL容量瓶
E.托盘天平 F.分液漏斗 G.玻璃棒 I.胶头滴管
(3)该同学为测定某碳酸钠样品的纯度,取2.5 g该碳酸钠样品,加入足量上述稀硫酸。碳酸钠完全反应(杂质不反应),生成二氧化碳气体448mL(标准状况)。求该碳酸钠样品中Na2CO3的质量分数。
高二化学计算题简单题查看答案及解析
-
实验室需用0.1mol/L的 H2SO4溶液480mL,欲用质量分数98%、密度为1.84g/cm3的浓硫酸配制,请回答下列问题:
(1)需要使用的主要仪器除烧杯、玻璃棒、量筒外,还需要____________。
(2)其操作步骤可分解为以下几步:
①完成下述步骤中的空白处
A.用酸式滴定管量取_______mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌。
B.用适量蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都移入容量瓶里。
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里。
D.检查容量瓶是否漏水。
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm处。
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液,倒入试剂瓶,贴好标签。
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切。
请据此填写:
②完成正确的操作顺序(用字母填写):______________________________。
③移液的操作方法是_____________________________________________________。
(3)试分析下列操作对所配溶液的浓度有何影响(填“偏高”、“偏低”、无影响”)
①量取浓H2SO4时,倒出浓H2SO4后的量筒中还残留少量液体未处理:_________;
②定容时俯视容量瓶刻度线,会导致所配溶液浓度_________。
③若用酸式滴定管量取浓硫酸时,先仰视后俯视,会导致所配溶液浓度_________。
高二化学实验题困难题查看答案及解析
-
(16分,每空2分)用质量分数为98%,密度为1.84 g•cm-3的浓硫酸配制100mL物质的量浓度为1mol/L的稀硫酸。
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、________、________。
(2)其操作步骤可分解为以下几步:
A.用量筒量取________mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌
B.用约30mL蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都倒入容量瓶里
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里
D.检查100mL容量瓶,是否漏水
E.将蒸馏水直接加入容量瓶,至液面接近刻度线________
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切
请据此填写:
①完成上述步骤中的空白处。
②正确的操作顺序是(用字母填写):
( )→( )→( )→( )→( )→( )→( )。
③进行A步操作时,选用量筒的规格是________。(选填字母)
A.10mL B.50mL C.100mL D.1000mL
④如果对装有浓硫酸的量筒仰视读数,配制的稀硫酸浓度将________(选填“偏高”、“偏低”、“无影响”)。
⑤A步骤操作完成时,必须________后,才能进行后面的操作。
高二化学实验题简单题查看答案及解析
-
用98%的浓硫酸(密度为1.84 g·cm-3)配制 250 mL浓度为0.5 mol·L-1的H2SO4溶液,选用的仪器正确的是( )
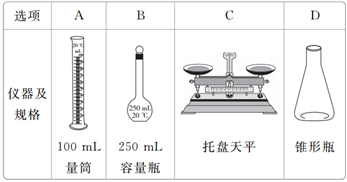
A. A B. B C. C D. D
高二化学选择题中等难度题查看答案及解析
-
用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸,下列操作正确的是
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.必需的定量仪器有50 mL量筒、250 mL容量瓶和托盘天平
C.量取浓硫酸的体积为25.0 mL
D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
高二化学单选题中等难度题查看答案及解析
-
CuSO4 是一种重要化工原料,其制备和有关性质如图所示。
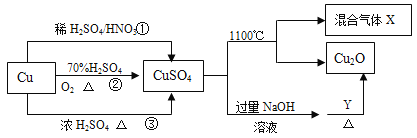
(1)现要用密度为 1.84g/mL,质量分数为 98%的浓硫酸来配制步骤①中所需要的 2mol/L 的稀硫酸480mL,需要用这种浓硫酸的体积为_____mL。
(2)配制该稀硫酸所用到的玻璃仪器除玻璃棒、量筒外还有_____。
(3)下列操作会使所配溶液浓度偏高的是_____。
A. 硫酸转移至容量瓶后,没有洗涤烧杯
B. 未冷却至室温就转移至容量瓶
C. 容量瓶中存在少量蒸馏水
D. 定容时俯视刻度
E. 用量筒量取浓硫酸后洗涤量筒
(4)制取硫酸铜的途径①②③中,不用_____途径,原因是_____。
高二化学实验题中等难度题查看答案及解析
-
(2分)将质量分数为98%,密度为1.84 g·cm-3的浓硫酸,用蒸馏水稀释到9.2 mol/L的硫酸,则其质量分数________49%(填>、<、=)。
高二化学填空题简单题查看答案及解析
-
将密度为1.84 g / cm3、质量分数为98%的浓硫酸稀释成1 000 mL、物质的量浓度为2 mol /L、密度为1.20 g / cm3的稀硫酸。求:
(1)所需浓硫酸的体积;
(2)所需水的体积。
高二化学计算题中等难度题查看答案及解析
-
(4分)实验室需要0.1mol/L硫酸950ml,某同学用98%的浓硫酸(密度为1.84g·cm-3)配制:
(1)需选用________容量瓶。
A.50m B.100ml C.250ml D.1000ml
(2)需量取浓硫酸________ml。
(3)配制溶液时下列操作使所配溶液浓度偏大的是________。
A.容量瓶中原有少量蒸馏水 B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
C.定容时观察液面俯视 D.溶液未经冷却即注入容量瓶
(4)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤量取 ⑥转移溶液 ⑦定容
正确的操作顺序是________(填序号)。
高二化学实验题简单题查看答案及解析